제조공정








탄소 포집 및 저장 기술
격리(CCS)라고도 하는 탄소 포집 및 저장은 고갈된 오일 및 가스 저장소, 지각 깊숙이 위치한 육상 및 해상 염수 대수층, 소금 동굴 또는 채광 불가능한 석탄층. 이는 온실 가스(GHG) 배출을 줄이기 위한 수단일 뿐만 아니라 기존 석유 및 가스 운영에서 생산을 향상시키기 위한 접근 방식입니다.
CCS는 화석 연료 기반 에너지 활용에 추가적인 대안을 제공하는 동시에 에너지 시스템이 재생 가능 에너지와 같이 탄소 감소 또는 제로 C 연료로 이동할 수 있는 추가 전환 시간을 제공합니다. CCS에는 (i) 대기로의 CO2 배출량 감소를 통한 잠재적으로 위험한 기후 변화 완화, (ii) 혁신, 첨단 기술에 대한 접근, 일자리 창출 및 지속적이고 보다 지속 가능한 경제 개발, (iii) 포집 및 저장되는 GHG의 배출이 국제 시장에서 판매될 수 있는 거래 가능한 상품으로 전환될 수 있는 2차 수익원, (iv) 잠재적으로 유해한 오염 물질로 인한 대기 오염 감소 CO2 포집 및 향상된 오일 및 가스 회수 기회를 수용하기 위해 제거됩니다.
CCS 배포에는 몇 가지 문제가 있습니다. CCS에 대한 몇 가지 과제에는 (i) 포집 비용 절감 및 포집 프로세스 확장, (ii) 포집의 환경적 영향 식별, (iii) 저장소 형성에서 압력 축적의 영향 결정, (iv) ) 대체된 물이 대규모 주입으로 들어가는 위치와 지하수에 대한 위험 결정, (v) CO2 플룸의 크기와 이동하는 위치를 안정적으로 예측하는 방법, (vi) 부지 선택에 대한 확신을 얻는 방법, (vii) 비용 효율적인 모니터링 전략 및 탐지 한계 개발, (viii) 금융 및 보험 산업 참여, (ix) 모든 수준의 정부에서 규제 및 정치적 확실성 강화, (x) 대규모 배치를 위한 인력 교육, (xi) 대중의 인식과 수용을 향상시킵니다.
CCS 기술은 석탄 및 가스 화력 발전, 천연 가스 처리 및 비료 생산을 포함한 대규모 배출 공정과 철강, 시멘트, 펄프 및 종이와 같은 산업 자재 제조에 적용할 수 있습니다. 등. 이러한 공정에 CCS 기술을 적용하면 GHG 배출을 줄이는 데 중요한 역할을 할 수 있습니다. 탄소 분리 및 포집 기술은 수십 년 동안 천연 가스 및 비료 산업에서 대규모로 운영되어 왔습니다. CCS 시스템에 관련된 기술에는 (i) 포획, (ii) 수송, (iii) 주입 및 (iv) 모니터링이라는 4가지 구성요소가 있습니다.
포집은 폐수 흐름에서 CO2를 분리하고 액체 또는 초임계 상태로 압축하는 것입니다. 오늘날 대부분의 경우 CO2 농도는 99% 이상이지만 더 낮은 농도는 허용될 수 있습니다. 포집은 일반적으로 CO2를 경제적으로 수송하고 저장하는 데 필요합니다.
운송은 소스에서 저장 저장소로의 CO2 운송으로 구성됩니다. CO2는 건조되고 일반적으로 저장소로 운송되기 전에 압축됩니다. 압축은 가스 수송을 보다 효율적으로 만듭니다. CO2는 여러 산업, 특히 음료 산업에서 상업적으로 사용되며 저수지에서 오일을 회수(향상된 오일 회수)하는 데 사용하기 위해 대규모로 운송되었습니다. 트럭, 기차 및 선박으로 운송하는 것이 모두 가능하지만 대량의 CO2를 운송하는 것은 파이프라인을 통해 가장 경제적으로 달성됩니다. CCS를 대규모로 구현하려면 주요 파이프라인 인프라를 구축해야 하며 이는 과제를 안겨줍니다.
주입은 저장 저장소에 CO2를 침전시키는 것으로 구성됩니다. 지하 저장 저수지는 지질 구조에 따라 다릅니다. CO2 저장의 안전은 가장 중요합니다. CO2 저장의 국부적 위험에는 (i) 저장 위치의 CO2 누출, (ii) 지하수 및 식수의 화학적 성질 변경, (iii) CO2가 저장되는 저장소에 있을 수 있는 잠재적으로 위험한 유체의 변위가 포함됩니다. 잠재적인 저장소에는 심해, 해양 퇴적물 또는 광물화(CO2를 광물로 전환)가 포함됩니다. CO2의 일부 상업적 이용은 가능하지만 배출되는 CO2의 양에 비해 사용할 수 있는 양은 매우 적습니다.
CO2가 주입되면 저장소에 CO2가 남아 있는지 확인하기 위해 저장 장소를 모니터링해야 합니다. CO2는 독성도 가연성도 아니므로 최소한의 환경, 건강 및 안전 위험만 제기합니다. 모니터링의 주요 목적은 격리 작업이 효과적인지 확인하는 것입니다. 즉, 거의 모든 CO2가 수세기 동안 대기에서 벗어나 있습니다. 모니터링 프로그램은 기준 데이터를 설정하기 위해 주입 전에 시작됩니다. 작동 단계 중 모니터링은 CO2가 주입될 때 저장소 내에서 CO2의 동적 거동을 기록하기 위한 것입니다. 주입이 중단된 후 모니터링 프로그램은 CO2 저장이 요구되는 환경 및 안전 조건을 충족하는지 확인하도록 설계되어야 합니다. 모니터링 프로그램은 세 가지 모니터링 영역, 즉 (i) 지하 영역(저수지), (ii) 표면 근처 영역(얕은 영역 및 토양), (iii) 우물, 단층 및 단층을 포함한 대기 영역을 다룹니다. 기타 지질학적 특징.
CO2 포집 기술
CO2는 천연 가스 생산 시설(이 과정의 일부로 CO2가 이미 다른 가스와 분리되어 있는 곳), 화석 연료 화력 발전소, 철강 공장, 시멘트 공장 및 일부 화학 공장과 같은 대규모 고정 배출원에서 포집될 수 있습니다. . CCS의 다른 두 가지 구성요소인 운송 및 지층 저장과 달리 CCS의 첫 번째 구성요소인 CO2 포집은 거의 전적으로 기술에 의존하며 가장 비용이 많이 드는 단계입니다. 이러한 소스에서 CO2를 포집하는 기술은 현재 천연 가스 산업 및 암모니아(NH3) 생산과 같은 산업에서 사용되는 CO2 분리 기술과 공기 분리 산업에서 사용되는 기술에서 채택되고 있습니다. 새로운 기술도 개발 중입니다.
현재 CO2를 포집하기 위한 주요 분리 기술은 (i) 액체 용매를 사용하여 CO2를 흡수(흡수), (ii) 고체 물질을 사용하여 CO2를 표면으로 끌어당겨 다른 가스와 분리됩니다(흡착), (iii) 다른 가스로부터 CO2를 분리하기 위해 멤브레인을 사용합니다. 기타 기술에는 화학적 루프 기술(금속 산화물이 연료와 반응하여 금속 입자, CO2 및 수증기 생성), 저온 또는 극저온 분리 공정(다양한 가스를 분리하기 위해 다양한 상 변화 온도에 의존) 및 재생 가능한 건식 고체가 포함됩니다. 프로세스.
화석 연료 사용으로 인한 CO2 포집을 위한 주요 경쟁 기술은 (i) 연소 기반 플랜트의 연도 가스로부터의 연소 후 포집(PCC), (ii) 가스화 기반 플랜트의 합성 가스로부터의 연소 전 포집 및 (iii) 산소 연료를 산소로 직접 연소시키는 연소. 현재 연소 공정의 대부분은 공기를 사용하며 생성된 연도 가스는 일반적으로 낮은 농도의 CO2(20% 미만)를 포함하므로 연소 후 포집 기술에 더 적합합니다.
연소 후 포집 기술
연소 후 포집은 배가스 정화의 한 형태로 간주될 수 있습니다. 공정은 다른 오염 제어 시스템 이후에 공장의 백엔드에 추가됩니다. 비용 효율적이려면 플랜트와의 열 통합이 필요합니다.
EPRI(Electric Power Research Institute)는 2009년에 여러 물리적/화학적 공정 유형으로 그룹화할 수 있는 연소 후 CO2 포집 개념이 50개 이상 있다고 결정했습니다. 이러한 공정 유형 그룹에는 (i) 화학적 흡수, (ii) 흡착, (iii) 막, (iv) 생물학적 및 (v) 기타가 있습니다. 이러한 서로 다른 그룹 각각은 서로 다른 상황에 적용할 수 있을 뿐만 아니라 서로 다른 장점과 단점을 가지고 있습니다. 처음 두 그룹과 관련하여 상당한 발전이 있습니다.
화학 흡수 과정 – 모노에탄올아민(MEA) 기반 용매와 고성능 아민(활성화된 메틸디에탄올아민, aMDEA) 등과 같은 흡수제의 수용액과 CO2 사이에 하나 이상의 가역적인 화학 반응이 포함됩니다. 제품을 가열하면, 흡수제와 CO2 사이의 결합이 깨져 CO2가 풍부한 스트림을 생성할 수 있습니다. 연도 가스에서 CO2를 분리하기 위한 화학적 흡수 공정은 가스 처리 산업에서 차용했습니다. 아민 기반 공정은 공정 가스 스트림에서 산성 가스 불순물(CO2 및 H2S)을 제거하기 위해 상업적으로 사용됩니다. 따라서 입증되고 잘 알려진 기술입니다.
모노에탄올아민의 공식은 H2NCH2CH2OH입니다. 아민은 하나 이상의 H2 원자를 유기 라디칼로 대체하여 암모니아(NH3)에서 파생된 것으로 간주할 수 있는 유기 화합물 그룹입니다. 치환기(R)는 알킬, 아릴 또는 아라릴일 수 있다. (R)이 알킬인 경우 아민을 알칸올아민이라고 합니다. 일반적으로 수산기는 증기압을 낮추고 수용성을 높이는 역할을 하는 반면, 아미노기는 수용액에서 산성 가스를 흡수하는 데 필요한 알칼리성을 제공한다고 생각할 수 있습니다. 아카놀아민은 CO2와 알칸올아민의 아민 작용기의 발열 반응을 통해 폐가스 스트림에서 CO2를 제거합니다. CO2를 포집하기 위한 상업적 관심의 아민은 수용성입니다.
아민은 (i) 1개의 H2 원자가 대체된 1차 아민(RNH2), (ii) 2개의 H2 원자가 대체된 2차 아민(R2NH)과 같은 라디칼로 대체된 암모니아의 H2 원자 수에 따라 분류됩니다. (iii) 3개의 H2 원자가 모두 대체된 3차 아민(R3N).
1차 아민에는 모노에탄올아민(MEA)과 디글리콜아민(DGA)이 있습니다. MEA는 일반적으로 CO2 흡수 및 산성 가스 제거를 위해 선택되는 전통적인 용매였습니다. MEA는 알칸올아민 중에서 가장 저렴합니다. 그것의 반응 속도는 빠르고 낮은 압력과 낮은 CO2 농도에서 잘 작동합니다. 그러나 몇 가지 단점이 있습니다.
첫째, CO2와 반응열이 높아 재생단계에서 높은 에너지를 공급해야 한다. 둘째, CO2를 포함하는 MEA의 흡수율이 높지 않습니다. 1차 및 2차 알칸올아민의 경우 카바메이트(RNHCOO-)의 형성이 주요 반응입니다. 반응 방정식은 CO2 + 2RNH2 =RNHCOO- + RNH3+입니다. 이 반응에서 1몰의 CO2를 포집하기 위해 2몰의 MEA가 사용되어야 합니다. 셋째, 부식 문제로 인해 MEA의 전체 상부 흡수 용량이 실제로 실현되지 않습니다. 부식 효과는 용해된 CO2로 인한 것이며 사용된 아민에 따라 다릅니다.
O2가 있는 상태에서 수성상의 MEA 농도는 20중량%로 제한됩니다. 또한 MEA는 알칸올아민 중 가장 높은 증기압을 가지며 가스 흐름에서 CO2를 제거하는 동안 및 재생 단계에서 높은 용매 캐리오버가 발생할 수 있습니다. 용매 손실을 줄이기 위해 일반적으로 정제된 가스 흐름의 물 세척이 필요합니다. 또한 MEA는 COS 및 CS2와 같은 경미한 불순물과 비가역적으로 반응하여 용매 분해를 유발합니다. 불순물 축적으로 인한 흡수 액체 MEA의 거품도 문제가 될 수 있습니다.
현재의 MEA 흡수기 시스템의 경우 흡착 및 탈착 속도가 상당히 높기 때문에 반응 속도가 좋습니다. 그러나 흡수기(효율적인 물질 전달을 용이하게 하기 위한 접촉기)의 패킹은 상당한 비용을 수반하며 연소 가스에서 CO2 포집을 위해 에너지 소비도 상당합니다. 또한, 스트립핑 온도는 너무 높지 않아야 합니다(약 150℃). 그렇지 않으면 카바메이트의 이량체화가 일어나 MEA의 흡수 능력이 저하될 수 있습니다.
2차 아민에는 디에탄올아민(DEA), 디이소프로필아민(DIPA)이 포함됩니다. 2차 아민은 1차 아민보다 장점이 있습니다. CO2와의 반응열은 1차 아민의 경우 455칼로리/그램에 비해 낮습니다(360칼로리/그램). 이는 2차 아민이 1차 아민보다 재생 단계에서 더 적은 열을 필요로 함을 의미합니다. 그러나 1차 아민의 다른 모든 문제를 가지고 있습니다.
3차 아민에는 트리에탄올아민(TEA) 및 메틸디에탄올아민(MDEA)이 포함됩니다. 3차 아민은 1차 및 2차 아민보다 CO2와 더 느리게 반응하므로 1차 및 2차 아민에 비해 CO2를 제거하기 위해 더 높은 액체 순환 속도가 필요합니다. 이것은 프로모터를 사용하여 개선할 수 있습니다. 3차 아민의 주요 이점은 CO2 함유 용매로부터 CO2 유리를 위한 낮은 열 요구사항입니다. 3차 아민은 1차 및 2차 아민보다 사용 중 분해 생성물을 형성하는 경향이 낮고 재생이 더 쉽습니다. 또한, 3차 아민은 1차 및 2차 아민에 비해 부식 속도가 낮습니다. 가장 큰 단점은 반응 속도가 너무 느리다는 것입니다.
연도 가스에서 CO2를 회수하기 위한 일반적인 화학 흡수 공정 흐름도가 그림 1에 나와 있습니다. 아민 흡수 작업 동안 폐가스 흐름과 액체 아민 용액은 흡수탑(또는 흡수기)의 역류 흐름에 의해 접촉됩니다.
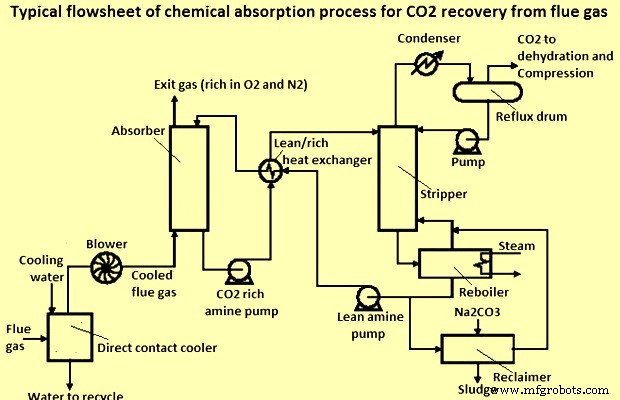
그림 1 연도 가스에서 CO2 회수를 위한 화학 흡수 공정의 일반적인 흐름도
굴뚝에서 나오는 연소 연도 가스는 뜨겁고(약 240℃) 대기압입니다. 고온에서 흡수기에 유입되는 연도 가스는 용매 분해 및 흡수 효율 감소로 이어질 수 있습니다. 연도 가스는 흡수기로 유입되는 50℃의 물 이슬점으로 냉각되어야 합니다. 흡수기는 일반적으로 50℃ 미만에서 작동합니다. 이것은 직접 접촉 냉각기에서 냉각수를 분사하여 이루어집니다.
연도 가스의 CO2는 흡수기로 들어가기 전에 냉각되어 탄산 암모늄과 반응하여 중탄산 암모늄을 형성합니다. NH3는 CO2가 흡수될 때 용매 용액에서 가스로 방출되며, 이를 최소화하기 위해 온도를 낮게 유지합니다. 흡수기를 떠나는 가스는 암모니아를 제거하기 위해 물 세척을 통과합니다. 중탄산암모늄은 재생기에서 가열되어 CO2를 분리합니다. 탄산 암모늄 용매는 흡수기로 되돌아갑니다. 물과 NH3는 스트리퍼 컬럼을 떠나는 CO2 스트림에서 제거됩니다.
송풍기가 설치되어 연도 가스가 흡수-탈착 시스템을 통과하기에 충분한 압력을 가합니다. CO2로 스크러빙되는 폐가스는 일반적으로 하단의 흡수기로 들어가 위로 흘러 상단으로 떠나는 반면, 용매는 흡수기의 상단으로 들어가서 아래로 흐르고(가스와 접촉) 하단으로 나옵니다. 순환하는 아민을 물로 희석하여 순환액의 점도를 낮춥니다. 점도가 높은 유체는 펌핑하고 순환을 제공하는 데 더 많은 전력이 필요합니다. 흡수된 가스를 함유한 액체 아민 용액은 가열되고 산성 가스가 방출되는 재생 장치(스트리퍼)로 흐릅니다. 용매 재생은 액체에서 CO2의 탈착을 향상시키기 위해 낮은 압력에서 수행할 수 있습니다. 일부 아민 용액은 일반적으로 재생 단계의 산성 가스 흐름으로 운반되고 아민 용액은 과도한 용매 손실을 피하기 위해 응축기를 사용하여 회수됩니다. 그런 다음 뜨거운 린 아민 용액은 열 교환기를 통해 흐르고 여기서 접촉 타워의 풍부한 아민 용액과 접촉하고 거기에서 린 아민 용액은 가스 접촉 타워, 즉 흡수기로 되돌아갑니다.
고성능 아민(활성화된 메틸디에탄올아민, aMDEA)을 사용하는 아민 스크러버 공정의 경우 전체 공정(아민 및 110kg/sq cm 압력으로 압축)에는 CO2 톤당 약 1.6톤의 저압 증기와 160kWh의 전력이 필요합니다. 캡처했습니다.
아민 기반 공정에는 몇 가지 제한 사항이 있으며 이로 인해 기술 발전이 이루어졌습니다. 과거 아민 스크러빙 기술은 천연 가스 부문의 H2S(황화수소) 제거에 중점을 두었습니다. 그러나 배가스에서 CO2를 회수하는 경우 요구사항이 다릅니다. 한 가지 문제는 CO2 흡수를 위한 연도 가스의 낮은 압력입니다. 또한, O2, 황산화물(SO2,SO3), 질소 산화물 및 입자상 물질과 같은 연도 가스의 불순물은 분리 과정에서 특별한 문제를 야기합니다.
요약하면, 연소 연도 가스에서 CO2를 회수하려면 용매 흡수 단계에서 오염을 방지하기 위해 상당한 양의 전처리 처리가 필요합니다. 이는 CO2 포집 비용을 추가합니다. 그러나 이를 관리하기 위해 흡수 아민 및 기액 접촉기의 조성을 최적화하는 측면에서 용매 흡수 공정에서 상당한 개선이 이루어질 수 있습니다.
물리적 흡수 – 물리적 흡수의 경우 CO2는 헨리의 법칙에 따라 용매에 물리적으로 흡수됩니다. CO2에 대한 유기 또는 무기 용매의 흡수 능력은 압력이 증가하고 온도가 감소함에 따라 증가합니다. CO2의 흡수는 CO2의 높은 분압과 낮은 온도에서 발생합니다. 그런 다음 용매는 가열 또는 감압에 의해 재생됩니다. 이 방법의 장점은 비교적 적은 에너지가 필요하다는 것입니다. 그러나 CO2는 높은 분압에 있어야 합니다.
고체 물리적 흡착 – 흡착 공정은 (i) 흡착 및 (ii) 탈착의 두 가지 주요 단계로 구성됩니다. 공정의 기술적 실행 가능성은 흡착 단계에 의해 결정되는 반면 탈착 단계는 경제적 실행 가능성을 제어합니다. 흡착은 흡착제와 가스 혼합물(이 경우 CO2)에서 제거할 성분 사이에 강한 친화력이 필요합니다. 그러나 친화력이 강할수록 CO2를 탈착하기가 더 어려워지고 다음 사이클에서 재사용을 위해 흡착제를 재생하는 데 소비되는 에너지가 높아집니다. 따라서 탈착 단계는 전체 프로세스가 성공하기 위해 흡착 단계와 매우 신중하게 균형을 이루어야 합니다.
흡착 공정은 흡착제의 용량이 낮고 SO2 및 H2O와 같은 오염 물질이 분리 공정에 미치는 영향과 같은 단점에도 불구하고 CO2 포집 메커니즘에 매우 매력적입니다. 가용성, 유연성, 공정의 완전 자동화 작업 및 고순도 제품 생산과 같은 이 공정의 장점도 있습니다. 분리는 압력 스윙 흡착(PSA)(그림 2), 진공 압력 스윙 흡착(VPSA), 온도 스윙 흡착(TSA), 압력-온도 스윙 흡착(PTSA) 또는 전기 스윙 흡착(ESA)에 의해 수행될 수 있습니다. 프로세스. 설비의 베드는 고체 흡착제로 채워져 있습니다. 선택성은 흡착 평형 또는 흡착 속도의 차이에 따라 달라지며 유효성(농도 및 회수)은 사이클 구성, 흡착 시간, 흡착 및 탈착 압력, 공정 중 온도 및 적용된 흡착제의 종류에 따라 중요합니다.
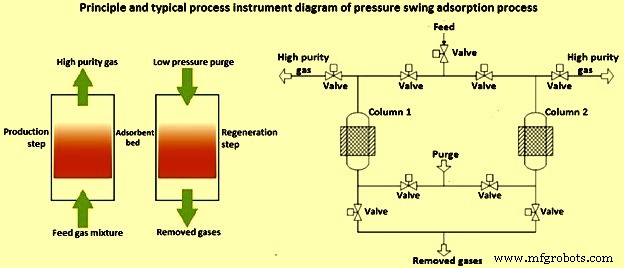
그림 2 압력 변동 흡착 과정
화학적 흡수에 비해 물리적 흡착의 주요 이점은 간단하고 에너지 효율적인 작동 및 재생이며, 이는 압력 변동 또는 온도 변동 주기(공정이 흡수-탈착 주기를 거쳐 순서대로 진행될 때 압력 또는 온도의 변동)로 달성할 수 있습니다. 분리를 달성하기 위해). 압력 변동 흡착은 H2 생산에서 H2 및 CO2 혼합물로부터 H2 분리를 위한 상업적 공정입니다.
연도 가스에서 CO2를 제거하기 위한 흡착제 개발에 상당한 발전이 있었습니다. 사용된 주요 흡착 물질은 제올라이트였습니다. 제올라이트는 CO2보다 극성이 낮은 종에서 CO2를 분리하는 데 더 효과적이므로 연도 가스 흐름에 물과 SOx가 존재하면 문제가 발생합니다.
탄소, 메조포러스 규소-알루미네이트(예:제올라이트 이미다졸레이트 프레임워크, ZIF) 및 금속 유기 프레임워크(MOF)와 같은 새로운 흡착제가 고려되고 개발되었습니다. 탄소 기반 흡착제는 전압(ESA)을 인가하여 재생될 가능성이 있습니다. 연구 중인 새로운 재료에는 층상 이중 수산화물 유도체(LDH 및 LDO)가 포함됩니다. 다른 발전에는 CO2 부하를 증가시키기 위해 아민을 통합함으로써 흡착제 물질의 기공을 기능화하는 것이 포함됩니다. 이 경우 CO2는 화학 흡착 과정을 통해 분리됩니다.
높은 습도의 연도 가스 흐름과 불순물을 처리하기 위한 새로운 공정이 개발되고 있습니다. 여기에는 다층 흡착 베드가 포함됩니다. 다층 베드는 CO2 선택성이 높은 흡착제를 사용할 수 있지만 물이 있는 경우 크게 저하됩니다.
연소 전 포집 기술
연소 전 포집 기술에는 열 회수(증기 사용) 또는 전력 또는 H2 생산을 위해 연소되기 전에 화석 연료의 상류 처리에서 오염 물질과 CO2를 제거하는 것이 포함됩니다.
연소 후 C 포집의 단점은 연도 가스의 낮은 CO2 농도로 인해 상대적으로 높은 에너지 패널티와 C 포집 비용이 높다는 것입니다. 사전 연소는 남아 있는 H2가 풍부한 연료를 연소시키기 전에 CO2가 풍부한 공정 흐름을 탈탄소화하여 이러한 페널티를 줄이기 위해 노력합니다. 탄화수소 연료의 탈탄소화를 달성하기 위해 먼저 O2(또는 공기)를 사용한 연료의 가스화를 통해 합성 가스로 전환됩니다. 합성가스는 전환 과정과 연료 및 기타 성분에 따라 CO(일산화탄소), H2, CO2 및 물의 혼합물입니다.
합성가스는 중간 생성물로 변환되어 (i) H2, (ii) 물-가스 전환 반응을 사용하여 통합 전력, 또는 (iii) 다음을 포함한 다양한 에너지 생성물이 존재할 수 있는 다중 발전을 생산할 수 있습니다. 전력, 열, H2 및 합성 연료 및 기타 화학 물질. 이러한 최종 에너지 제품 각각과 관련된 프로세스는 아래에 설명되어 있습니다.
메탄 개질에 의한 H2 생성 – H2를 생산하기 위해 오늘날 가장 널리 사용되는 방법은 메탄(CH4)의 촉매 증기 개질에 의한 것입니다. CH4와 H2 전환의 개질 반응 O에서 CO 및 H2는 흡열입니다. 반응은 CH4를 연료로 하는 직접 가열로에서 고온의 Ni(니켈) 촉매를 통해 수행됩니다. 촉매는 S(황)에 의해 중독되므로 공급물에 존재하는 모든 S는 제거되어야 합니다. 합성가스는 차례로 촉매 물 전환 변환기를 통과하며, 여기서 CO는 증기와 발열 반응하여 H2와 CO2 부산물을 생성합니다. 그런 다음 이러한 부산물은 시스템에서 제거됩니다. 배기 가스는 여전히 상당한 발열량을 포함하므로 증기나 전력을 생산하기 위해 연소됩니다.
석탄 가스화 – 가스화 기술은 CO2가 높고 중간 압력에서 가스 흐름을 생성할 수 있습니다. 공급 석탄은 합성 가스를 생산하기 위해 O2(또는 공기)에서 기화됩니다. 합성 가스는 고온 및 저온 증기를 생성하는 합성 가스 냉각기에서 200℃로 냉각됩니다. 그런 다음 저온 수성 가스 시프트 반응기에서 더 시프트됩니다. 수성 가스 전환 반응기는 CO가 증기와 반응하여 더 많은 H2와 CO2를 생성하는 촉매 반응기입니다. 그런 다음 산성 가스 제거를 위해 가스를 35℃로 냉각합니다. H2S의 대략 99%는 물리적 흡수에 의해 합성 가스에서 제거되고 황 원소로 전환됩니다. PSA 장치를 사용하여 S-free 합성 가스에서 H2의 85%를 분리할 수 있습니다. H2는 약 60kg/sq cm 및 고순도(99.99% 이상)를 남깁니다. CO2는 S 포집 시스템의 합성가스 다운스트림에서 제거될 수 있습니다. PSA 퍼지 가스는 가스터빈 결합 사이클에서 압축 및 연소되어 전력을 생산합니다.
가스화 기술은 H2 생산을 위해 잘 확립되어 있습니다. 상업용 공장은 다양한 탄화수소 공급원료를 기반으로 정유 및 화학 제조(예:NH3 및 메탄올 생산)를 위한 H2를 생산하기 위해 건설 및 성공적으로 운영되었습니다.
통합 전력 – H2 함량이 높은 합성 가스는 터보 팽창기에서 연소되어 복합 사이클 설정에서 전력을 생산할 수 있습니다. 합성 가스가 가스화를 사용하여 생산되는 경우 이 계획을 IGCC(통합 가스화 복합 사이클)라고 합니다. IGCC는 전력을 고효율로 생산할 수 있습니다. 가스 터빈의 손상을 방지하기 위해 가스를 청소해야 하기 때문에 IGCC는 환경 배출이 매우 낮습니다. 또한 IGCC 플랜트는 물을 덜 사용합니다. IGCC는 현재 전력, H2 및 증기를 제공하기 위해 석유 잔류물의 가스화에 의해 전 세계적으로 많은 공장에서 상업적으로 사용되고 있습니다.
석탄 가스화기의 세 가지 주요 유형은 (i) 이동층, (ii) 유동층 및 (iii) 동반 유동입니다. 그러나, CO2 포집을 위해 고려되는 대부분의 가스화기는 현재 연행식 가스화기를 기반으로 합니다. 석탄 기반 IGCC의 상업적 적용은 상대적으로 높은 비용, 열악한 발전소 가용성 및 미분탄 발전소와의 경쟁으로 인해 제한되었습니다. IGCC에서 CO2 포집 비용은 가스화기 유형에 따라 크게 달라집니다.
위에서 언급했듯이 CO2가 포집될 수 있도록 연료 가스는 대부분의 CO가 증기에 의해 반응하여 H2와 CO를 생성하는 촉매 전환 반응기에 공급되어야 합니다. 슬러리 공급 가스화기의 경우 충분한 증기가 이미 내부에 존재합니다. 석탄 슬러리 물의 증발과 가스화기 제품 가스의 급냉 냉각으로 인한 연료 가스. 그러나 건식 공급 가스화기의 경우 증기 사이클에서 증기를 가져와 변속 변환기로의 연료 가스 공급에 추가해야 합니다.
IGCC는 두 경우 모두 CO2 포집이 없는 기존 미분탄 연소보다 전기 생산에 더 비싸다는 점에 유의해야 합니다.
다중 생성 – Syngas는 광범위한 에너지 제품을 생산하는 데 사용할 수 있으므로 좋은 빌딩 블록입니다. 제공되는 가장 큰 유연성은 단일 공장 단지에서 '합성 가스'가 증기, 전력, H2 및 화학 물질(예:메탄올, Fischer-Tropsch 액체)을 생성할 수 있는 다중 발전입니다.
용매, 흡착제 및 멤브레인 기술을 비롯한 다양한 분리 기술을 적용하여 가스화 제품에서 CO2를 분리할 수 있습니다.
흡수 – 기존 기술은 H2S를 제거한 다음 CO2를 포집하는 2단계 공정의 물리적 흡수입니다. 그러나 수성 가스 전환 반응 후에 가스를 냉각한 다음 전력을 생산하기 전에 재가열해야 합니다. 이는 효율성을 감소시키고 비용을 증가시킵니다.
흡착 – 흡착제는 수성 가스 전환 반응의 하류에서 연소 후 연도 가스 스트림에서 CO2를 분리하는 데 사용할 수 있습니다. 온도 변동 흡착(TSA)과 진공/압력 변동 흡착(VSA/PSA) 모두 흡착제에서 CO2를 회수하는 데 사용할 수 있습니다. CO2는 VSA/PSA를 통해 회수될 때 낮은 압력에 있으며 저장을 위해 압축해야 합니다.
막 – 가스 전환 반응과 H2 분리를 한 단계로 결합하는 고급 멤브레인 기반 가스 분리 시스템이 현재 개발 중입니다. 멤브레인 기반 시스템은 합성 가스를 이동하고 H2를 추출하기 위해 수성 가스 이동 H2 분리막 반응기(HSMR)를 사용합니다. 약 475°C의 최대 온도는 빠른 화학 동역학을 보장하고 H2 제품의 지속적인 제거를 통해 우수한 수성 가스 이동 평형 성능을 얻습니다.
무기 H2 투과성 막에는 (i) 세라믹 분자 체질, (ii) 조밀한 세라믹 이온 수송, (iii) 조밀한 금속이라는 세 가지 주요 부류가 있습니다.
사전 연소(탈탄소)의 장점과 단점 – 사전 연소(탈탄소)의 장점은 (i) 용매 흡수를 통한 CO2 분리 또는 PSA가 입증되었습니다. 배기 가스는 높은 압력에서 발생하고 높은 CO2 농도는 포집 비용을 크게 줄입니다. (ii) CO2가 중간 압력에서 생성될 수 있으므로 압축 비용은 연소 후 소스보다 낮습니다. (iii) 이 기술은 낮은 SOx 및 NOx 배출을 제공합니다. , (iv) 주요 제품은 합성가스로, 다른 상업적 용도나 제품에 사용할 수 있으며, (v) 광범위한 탄화수소 연료를 가스, 오일, 석탄, 석유 코크스 등과 같은 공급원료로 사용할 수 있습니다. 단점은 (i) 공급 연료가 먼저 연료를 합성가스로 전환하는 것, (ii) 가스터빈, 히터, 보일러를 H2 연소를 위해 개조해야 하고, (iii) 더 높은 비용과 더 큰 기술 위험이 있다는 점, (iv) 개조를 위해 기존 공장에 대한 주요 수정이 필요합니다.
산소 연료 연소
순산소 연소는 배출이 거의 없고 깨끗한 화석 연료 연소에 대한 새로운 접근 방식을 나타냅니다. 그것은 공기 대신 순수한 O2에서 연료를 연소함으로써 달성됩니다. 연소 과정에서 N2(질소)를 제거함으로써 연도 가스 흐름의 배기 가스는 N2 없이 주로 물과 CO2로 구성됩니다. 고순도 CO2는 물의 응축으로 회수할 수 있습니다. 그러나 연료가 순수한 O2에서 연소될 때 화염 온도는 일반 송풍 버너보다 훨씬 높으며 기존의 버너 구성 재료는 이 높은 온도를 견딜 수 없습니다. 따라서 구성 재료를 개선하거나 화염 온도를 낮추어야 합니다. 고온 내성 재료의 개발은 주요 R&D(연구 및 개발) 사업이기 때문에 더디게 진행되었습니다. 화염 온도를 조절하는 데 사용할 수 있는 여러 가지 방법이 있으며 가장 일반적인 방법은 CO2 재활용입니다. CO2 재활용에서는 CO2가 풍부한 연도 가스 흐름의 일부가 버너로 다시 재활용되어 일반 공기 송풍 버너와 유사한 화염 온도를 낮춥니다. 또 다른 방법은 CO2 재활용 대신 물 주입을 사용하여 화염 온도를 제어하는 것입니다. 이것을 흔히 '하이드록시 연료' 연소라고 합니다. 효과적으로, 이 두 가지 옵션을 사용하면 새로운 고온 내성 재료가 개발될 때까지 기존 내화 재료를 계속 사용할 수 있습니다.
A primary benefit of oxy-fuel combustion is the very high-purity CO2 stream which is produced during combustion. After trace contaminants are removed, this CO2 stream is more easily purified and removed than post-combustion capture. There are other benefits also such as reduction in NOx formation etc. When burning oil or coal, only two unit operations are needed for the combined removal of all other pollutants namely an electrostatic precipitator (ESP) or bag filter and a condensing heat exchanger (CHX)/reagent system. It is also possible to simplify the reagent system in the CHX to achieve total removal of SO2 with the CO2 stream for geologic storage. This further reduces the cost of unit operations for pollution abatement. The CHX increases the thermal efficiency of the boiler depending on the type of fossil fuel combusted, being the lowest for high rank bituminous coal and highest for natural gas.
Another benefit is the significant reduction in the size and capital cost of all plant equipment compared to conventional air-based combustion systems. This is due to the almost 5-fold decrease in the fire box volume and exit flue gas flow rates as N2 is eliminated in the combustion process.
The major disadvantage of oxy-fuel combustion is the high capital cost (primarily due to O2 requirements) and large electric power requirement inherent in conventional cryogenic air separation units required to generate O2. Oxy-fuel combustion is not currently used in typical large combustion systems because the air separation system is expensive and flue gas recycling is needed to be practiced in order to moderate flame temperature.
제조공정
카본 아크 용접이란 무엇입니까? 탄소 아크 용접(CAW)은 비소모성 탄소(흑연) 전극과 공작물 사이의 아크로 금속을 가열하여 금속의 유착을 생성하는 공정입니다. 탄소-아크 용접에서 탄소 전극은 전극과 접합되는 재료 사이에 전기 아크를 생성하는 데 사용됩니다. 이것은 개발된 최초의 아크 용접 공정이었지만 오늘날에는 트윈 탄소 아크 용접 및 기타 변형으로 대체되어 많은 응용 분야에 사용되지 않습니다. 아크 용접의 목적은 분리된 금속 사이에 결합을 형성하는 것입니다. 이 아크는 3,000°C를 초과하는 온도를 생성합니다. 이 온도에
탄소 섬유 (CF)는 직경이 약 5-10마이크로미터이고 대부분 탄소 원자로 구성된 섬유입니다. 탄소 섬유에는 몇 가지 장점이 있습니다. 높은 강성 , 높은 인장 강도 , 저중량 그리고 높은 내화학성 . 이 게시물을 읽고 나면 주요 분류를 알게 될 것입니다. 탄소 섬유의 원료 자세한 제조 프로세스에 대해 알아보세요. 즉, 탄소 섬유 제품의 품질을 빠르게 구별하고 전체 제조 공정을 보다 효율적으로 파악할 수 있습니다. 1. 탄소 섬유의 일반 분류 아. 인장 계수 기준 인장 계수 탄소 섬유를 분류하는 핵심 기준은 섬유입