나노물질








금 나노클러스터(AuNC)는 독특한 화학적 및 물리적 특성으로 인해 이미징, 검출 및 치료에서 생물의학 응용을 위한 형광 프로브로 광범위하게 적용되었습니다. AuNC의 형광 프로브는 높은 상용성, 우수한 광안정성 및 우수한 수용해도를 나타내어 장기 이미징, 고감도 검출 및 표적 특이적 치료를 위한 놀라운 생물의학 응용을 초래했습니다. 최근에는 다양한 생물의학 응용을 위한 형광 프로브로서 AuNC의 개발에 많은 노력을 기울이고 있습니다. 이 리뷰에서 우리는 소분자, 폴리머, 생체거대분자를 포함한 다양한 리간드에 의해 준비된 형광 AuNC를 수집하고 이미징, 검출 및 치료를 위한 생물의학 응용 분야에서 AuNC의 현재 성과를 강조했습니다. 이러한 발전에 따라 우리는 근본적인 조사와 실용적인 생물 의학 응용을 위한 AuNC의 현재 과제와 미래 전망에 대한 결론을 추가로 제공했습니다.
<섹션 데이터-제목="배경">최근의 생물의학 응용은 나노과학 및 나노기술의 발전에서 나노물질의 중요한 역할을 밝혀냈습니다[1,2,3,4,5,6,7,8,9,10]. 벌크 재료와 비교하여 나노재료는 독특한 물리적 및 화학적 특성을 나타내어 유망한 빌딩 블록이 되었습니다[11,12,13,14,15,16,17,18]. 다양한 나노 물질 중에서 특정 유형의 금 나노 물질, 최대 수백 개의 금 원자 크기를 갖는 금 나노 클러스터(AuNC)는 잘 정의된 구조, 손쉬운 표면 변형 및 매우 안정적인 광학 특성으로 인해 생물 의학 응용 분야에서 광범위하게 조사되었습니다. [19,20,21,22,23,24,25,26,27,28,29,30,31,32,33,34]. 뚜렷한 표면 플라즈몬 공명 없이 AuNC는 긴 수명과 큰 Stokes 이동으로 가시광선에서 근적외선까지 넓은 영역에서 형광을 나타냅니다[35,36,37]. 이미징, 검출 및 치료 분야의 생물 의학 응용 분야에서 형광 프로브로 AuNC를 사용하기 위해 많은 노력을 기울였습니다[38,39,40]. 유기 형광단 및 양자점과 비교하여 형광 AuNC는 장기 이미징, 고감도 검출 및 표적 특이적 처리에 대해 높은 상용성, 우수한 광안정성 및 우수한 수용해도를 보였다[41,42,43,44,45, 46,47,48,49]. 형광 프로브로서 AuNC의 집중적인 개발은 이미징, 검출 및 치료의 응용에 상당한 영향을 가져왔습니다.
최근 몇 년 동안 생물 의학 응용 분야에서 AuNC의 광범위한 개발이 이루어졌습니다. 분석 응용의 관점에서 AuNC의 여러 뛰어난 검토 논문은 약물, 환경 오염 물질 및 생물학적 샘플의 분석에 중점을 두었습니다[50,51,52,53]. 이 리뷰에서 우리는 이미징, 검출 및 치료 응용 분야에서 소분자, 폴리머 및 생체 거대 분자를 포함한 세 가지 유형의 리간드와 접합된 AuNC의 사용에 대한 최근의 발전을 강조했습니다. 기초 연구 및 생물 의학 응용을 위한 AuNC의 관련 과제와 미래 전망도 "결론"에서 제공되었습니다.
소분자는 AuNC를 준비하기 위한 리간드로 광범위하게 적용되었습니다. 표면에 있는 작은 분자의 접합으로 AuNC는 이미징 및 감지에 대해 다른 기능을 나타냅니다. 예를 들어, d-penicillamine conjugated with gold nanoclusters(DPA-AuNCs)는 작은 크기, 높은 콜로이드 안정성 및 밝기와 같은 꽤 좋은 특성을 가지고 있어 형광 프로브로서 엄청난 관점을 부여하므로 생물학적 이미징에 활용할 수 있습니다. 인간 암(HeLa) 세포는 DPA-AuNC의 내재화에 의해 이미지화되었습니다. 그런 다음 DPA-AuNC와 함께 암세포를 2시간 배양한 후 공초점 현미경을 사용하여 2광자 여기 기술로 세포를 이미징했습니다[54]. 멤브레인 염료 DiD를 기준으로 사용했으며 DPA-AuNC와 DiD 염료의 발광 강도를 각각 녹색과 빨간색으로 수집했습니다. 나노 입자의 섭취로 인해 HeLa 세포에서 방출되는 밝은 발광은 그림 1a에 나와 있습니다. 또한 3D 재구축을 위해 그림 1b[55]와 같이 다양한 z-위치에서 서로 다른 이미지를 촬영했습니다.
<그림>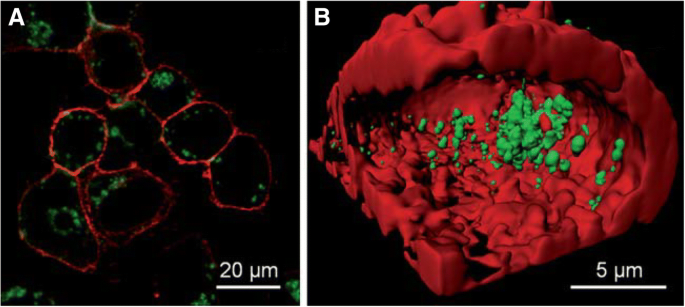
아 공초점 현미경으로 2시간 동안 DPA-AuNC와 배양한 후의 HeLa 세포 이미지. ㄴ 단면 보기에서 내부화된 DPA-AuNC를 표시하는 3D 이미지 [55]. DPA-AuNC와 멤브레인 염료 DiD의 색상은 각각 녹색과 빨간색으로 표시됩니다.
디하이드로리포산(DHLA)-AuNC는 처음으로 형광 수명 이미징(FLIM) 응용 프로그램을 조사하기 위해 HeLa 세포에 내재화되었습니다. DHLA-AuNC가 없는 Hela 세포는 수명이 1.5~4ns인 자동 형광을 나타냈습니다. Hela 세포의 강도 및 수명 이미지는 그림 2a, b에 나와 있습니다. 그러나 Hela 세포를 1시간 동안 DHLA-AuNC에 노출시킨 후 세포는 500~800ns의 긴 형광 수명을 나타내는 현저한 발광 방출을 보였습니다. DHLA-AuNC가 있는 Hela 세포의 강도 및 FLIM 이미지가 그림 2c, d에 나와 있습니다[56].
<그림>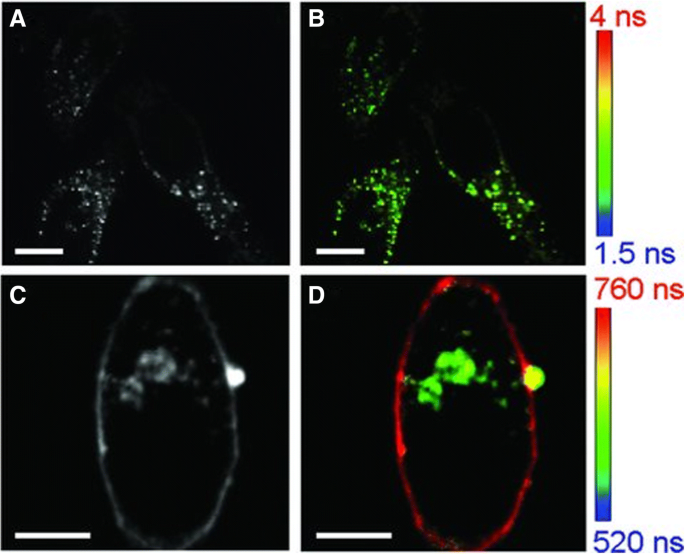
강도(a , ㄷ ) 및 FLIM(b , d ) Hela 세포의 이미지만(a , b ) 및 DHLA-AuNC와 함께 1시간 동안 배양된 Hela 세포(c , d ). 모든 눈금 막대는 10μm[56]
Wang et al. HepG2(인간 간암 세포주), K562(백혈병 세포주)와 같은 암 세포주가 마이크로몰 농도의 염화금산(생체적합성 분자 Au(III) 종) 용액과 함께 배양될 때 AuNC가 이들 세포에 의해 자발적으로 생합성된다는 것을 발견했습니다. 라인 [57]. 그러나 대조군으로 활용한 비암성 세포주인 L02(인간 배아 간세포)에서는 이러한 현상이 일어나지 않았다. 결과적으로, 위에서 언급한 방법은 종양의 생체내 자가-바이오 이미징을 위한 새로운 방법으로 승화될 수 있다. 근적외선 형광을 갖는 또 다른 트립신 안정화 금 나노클러스터(try-AuNCs)는 Liu et al. 이중 목적을 위해; 적용 가능성 중 하나는 표면 플라즈몬 강화 에너지 전달(SPEET)을 기반으로 하는 헤파린의 바이오센싱을 포함하고 다른 하나는 생체 내 암 형광 이미징을 위한 엽산(FA) 변형 try-AuNC를 포함합니다(그림 3). try-AuNCs가 가지고 있는 SPEET 모드와 높은 표적화 능력을 가진 생체 내 암 영상은 생체 감지 생체 분자를 위한 다기능 생체 재료로서 엄청난 잠재력을 보여주었습니다[58].
<그림>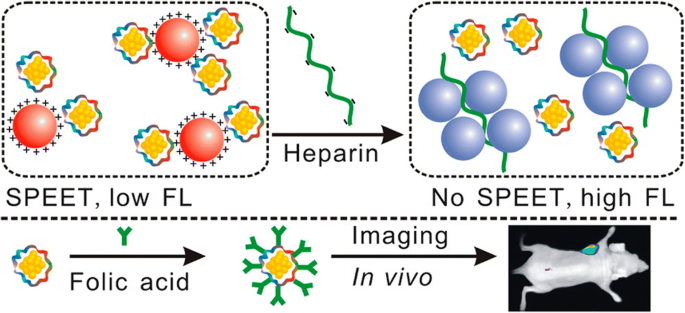
표면 플라즈몬 강화 에너지 전달 바이오센서 및 생체 내 암 이미징 바이오프로브로서의 근적외선 형광 try-AuNCs [58]
o-퀴논 함유 리간드는 철(Fe 3+ ) 이온 [59, 60]. 따라서 리간드로 도파퀴논을 포함하는 AuNC가 Ho et al.에 의해 개발되고 평가되었습니다. Fe 3+ 감지용 Fe 3+ 사이의 복합체 형성 메커니즘 기반 용액에서 도파퀴논의 이온 및 o-퀴논 부분. Fe 3+ 존재하에서 AuNC의 응집을 통해 500nm 이상의 치수를 갖는 큰 복합체가 형성된다는 연구 결과가 발견되었습니다. 이온. 따라서 AuNC는 Fe 3+ 검출에 사용할 수 있습니다. 물 및 기타 액체의 이온 [61].
산성 작용기는 금속 이온 및 바이오티올과 안정한 착물을 형성하는 것으로 보고되었습니다. 유사하게, 11-mercaptoundecanoic acid-conjugated gold nanoclusters(MUA-AuNCs)는 Hg 2+ 를 감지하는 것으로 생각되었습니다. AuNC의 감지 적용 가능성 중 하나로 간주될 수 있는 용액 및 비티올의 이온 [62, 63]. Hg 2+ 복합체에서 MUA-AuNC의 형광 강도 이온은 그림 4에 나와 있습니다[64]. 또한, Hg 2+ 의 복합체 -티올은 Hg 2+ 보다 더 안정적인 것으로 보고되었습니다. -COOH 복합체 [65]. 따라서 MUA-AuNC의 복합체는 다양한 용액에서 금속 이온을 감지하는 또 다른 응용으로 간주될 수 있는 비티올을 감지하는 데 사용되었습니다[64].
<그림>
아 170μM Hg 2+ 가 없을 때 MUA-AuNC의 형광 강도 . ㄴ Hg 2+ 응집 170μM Hg 2+ 가 있는 상태에서 COOH 그룹의 MUA-AuNC 사용 . ㄷ B의 샘플에 10mM 시스테인을 첨가한 후 형광 강도 [64]
반코마이신 안정화 금 나노클러스터(Van-AuNCs)는 Yu et al.에 의해 설계 및 합성되었습니다. Fe 3+ 검출용 수돗물, 호수 물, 강물 및 해수에서 환경 샘플 분석에 응용 프로그램 중 하나로 [66]. 키토산 기능화 금 나노클러스터(AuNCs@Chi)는 황화수소(H2 S) Förster 공명 에너지 전달(FRET) 메커니즘 사용[67]. 연구원들이 H2를 검출한 이유 S는 황화수소가 혈관 확장 [68, 69], 항염 [70, 71] 및 신경 전달 [72]을 포함한 많은 생물학적 과정에 관여한다는 것입니다.
Liu et al. 라이신과 시스테인(아미노산)의 검출 및 감지에 활용되는 높은 선택성, 빠른 반응, 우수한 광안정성을 갖는 글루타티온(GSH) 안정화 금 나노클러스터(GSH-AuNCs) 합성 기반 마련 [73] . 최근에는 Yu et al.에 의해 FRET(Forster Resonance Energy Transfer) 어셈블리가 개발되었습니다. 글루타티온으로 덮인 금 나노클러스터 사용(AuNCs@GSH). 어셈블리는 미래에 시스테인 관련 질병 진단에 사용될 수 있는 아미노산 시스테인에 대해 매우 선택적인 것으로 밝혀졌습니다[74]. 시스테인이 풍부한 단백질 주형 AuNC는 은(I) 이온을 사용하여 제조되었습니다. 케라틴은 모발, 양모, 깃털 등에 풍부하게 발견되는 시스테인이 풍부한 구조 단백질입니다. 따라서 은 이온 기반 케라틴 주형 AuNC를 합성하고 수은 이온(Hg 2+ ) [75]. 수은 이온(Hg 2+)의 민감한 검출을 위한 비율 측정 형광 센서인 디티오트레이톨(DTT)로 기능화된 이중 방출 탄소 점-금 나노클러스터(C-AuNC) 기반 물 샘플에서 최근 보고되었습니다[76]. AuNC의 위에서 보고된 두 가지 응용 프로그램은 수질 모니터링에 매우 중요한 역할을 할 수 있습니다. Cyclodextrin으로 덮인 AuNC가 코발트 이온(Co 2+ ) 및 디스플레이 형광 기반 선택적 및 민감한 Co 2+ 이온 감지. AuNC의 세포 내재화는 Co 2+ 감지 중에도 관찰되었습니다. 이온 [77].
최근 GSH의 생체적합성 표면 리간드와 결합된 초소형 AuNC가 암 방사선 치료를 위한 대사 가능하고 효율적인 방사선 과민제로 합성되었다[78]. GSH-AuNCs의 초소형 나노구조물은 Au 코어로부터의 강력한 방사선 요법 향상 및 표면 코팅 GSH로부터의 우수한 생체적합성을 포함하는 매력적인 특성을 드러냈습니다. 더욱이, GSH-AuNC는 향상된 투과성 및 체류 효과를 통해 종양에 우선적으로 축적되어 훨씬 더 큰 금 나노 입자보다 암 방사선 요법에 대한 강력한 향상을 가져옵니다. 향상된 방사선 요법은 Au25의 광전 효과 및 Compton 산란으로 인한 DNA 손상에 기인할 수 있습니다. 나노 클러스터. U14 종양의 부피와 무게의 현저한 감소는 GSH-AuNC를 방사선 과민제로 사용함으로써 달성되었습니다. 또한, 치료 후 GSH-AuNCs는 신장에서 효율적으로 제거될 수 있어 Au25 축적으로 인한 잠재적인 부작용을 최소화할 수 있습니다. 동물 모델의 나노클러스터.
폴리머는 또한 생물의학 응용에서 AuNC의 준비를 위한 중요한 리간드로 등장했습니다. 예를 들어, AuNC는 높은 광안정성 후보로 밝혀졌으며 정상(제대혈 단핵 세포, CBMC) 및 조혈 세포를 표지하는 데 사용된 여러자리 티오에테르 말단 폴리(메타크릴산)(PTMP-PMAA) 리간드로 캡핑하여 제조되었습니다. (K562 암세포) (그림 5) [79]. 암세포가 이들 분자를 정상세포보다 훨씬 더 많이 섭취한다는 결과가 밝혀졌다[80]. 금 나노입자는 조혈계의 일부인 과립구 및 림프구와 같은 보다 성숙한 세포에 쉽게 침투할 수 있다고 보고되었다[81]. 유사하게, AuNC는 조혈계 및 만성 골수성 백혈병과 같은 관련 암의 선택적 라벨링, 영상화 및 표적 약물 전달에도 적용할 수 있습니다.
<그림>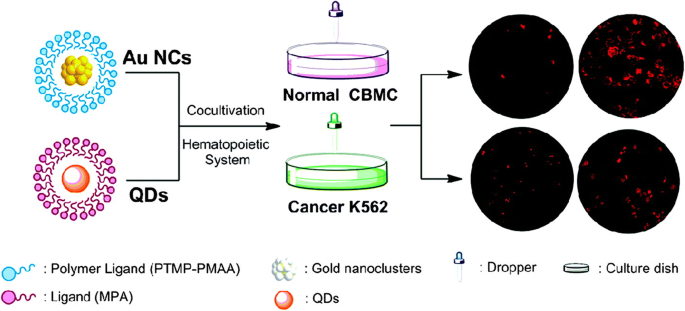
AuNC 및 양자점(QD)을 사용한 정상 및 암 세포의 라벨링 [79]
Aldeek et al. 폴리(에틸렌 글리콜) 단쇄 또는 양쪽성 이온 그룹과 결합된 리포산 고정 그룹으로 만들어진 두자리 리간드를 사용하여 형광 폴리에틸렌 글리콜 및 양쪽성 이온 기능화된 금 나노클러스터를 설계했습니다[82]. 생물학에서 이러한 나노클러스터의 역할을 결정하기 위해 과량의 염이 존재할 때 pH 의존적 안정성 및 안정성과 같은 다양한 테스트가 수행되었습니다. 저자가 제시한 가설은 이러한 테스트가 생물학에서 이미징 및 감지를 위한 형광 플랫폼으로 이러한 AuNC를 사용하는 것과 관련이 있음을 보여줍니다. 다양한 생물학적 이상이 pH와 관련되어 암 전이, 만성 피로 및 우울증과 같은 여러 질병의 진행에 대한 지표를 제공할 수 있다는 보고서에 추가로 설명되어 있습니다[83, 84]. 이 클러스터는 또한 단백질과 핵산의 물리적 거동을 관리하는 것으로 생각됩니다[85,86,87]. 이러한 클러스터의 추가 이점 중 하나는 생체 내(심부 조직) 이미징에서 사용한다는 것입니다. Chen et al. 엽산 과발현 암 세포의 검출 및 치료를 포함하는 진단 활동을 위한 나노복합체 형태로 광안정하고 생체적합성인 것으로 밝혀진 발광 AuNC를 포함하는 pH 의존성 양친매성 고분자 시스템을 개발했습니다[88]. 발광 AuNC는 양친매성 공중합체(poly(DBAM-co-NASco-HEMA)(PDNH))로 억제되어 L-nAuNC/FA-변형 PDNH(또는 L-AuNC/FA-PDNH) 나노복합체를 형성했습니다. 또한, 소수성 약물인 파클리탁셀은 L-AuNCs/FA-PDNH와 조립되어 암의 영상화 및 치료에 모두 활용될 수 있습니다(그림 6).
<그림>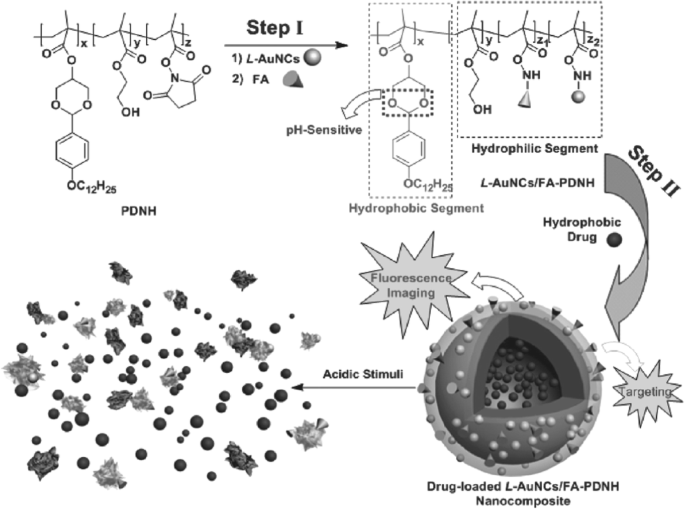
영상 및 치료를 위한 L-AuNCs/FA-PDNH 나노복합체 제작 [88]
폴리양이온 기능화된 수용성 폴리에틸렌이민 금 나노클러스터(PEI-AuNCs)는 세포 이미징과 함께 적절하고 안전한 유전자 치료 응용을 위해 설계 및 합성되었습니다[89]. PEI-AuNC의 매혹적인 광학적 특성으로 인해 이러한 클러스터는 PEI-AuNC와 함께 암세포주(HepG2)를 배양하여 확인된 바이오 이미징의 유망한 후보로 보고되었으며 놀라운 광발광과 강한 강렬한 적색 형광을 제공하는 세포를 보여주었습니다. 엽산(표적 리간드)(FA-Ova-AuNCs)과 단일중합체 N에 연결된 오브알부민(형광 프로브)으로 보호되는 금 나노클러스터 -acryloxysuccinimide를 링커로 사용하여 Qiao et al.에 의해 개발 중입니다. 암세포 영상을 통한 암 진단에 활용하였다(Fig. 7). 엽산 수용체가 HeLa 세포에서 과발현되기 때문에 Hela 세포가 FA-Ova-AuNC를 섭취하는 것으로 생각됩니다. 이 작업에서 FA-Ova-AuNC에 의한 HeLa 세포의 특정 염색이 입증되었습니다[90].
<그림>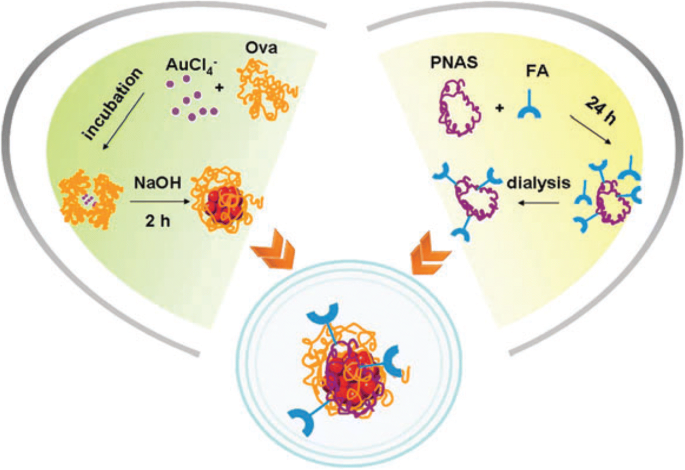
암세포 영상화를 위한 FA-Ova-AuNC의 형성 개략도 [90]
검출에 적용하기 위해, 거대다공성 폴리머 필름의 고인광성 분자 금(I) 클러스터가 비색 검출 기술을 통한 시안화물 검출을 위해 설계 및 합성되었습니다. 금 나노클러스터는 적포도주, 커피, 주스 및 토양에서 시안화물 이온을 감지하는 데 사용할 수 있습니다. 시안화물은 극도로 유독하고 위험하며 사망에 이를 수 있기 때문에[91] 환경, 물 및 식품의 시안화물 수준을 결정하는 데 도움이 될 수 있는 매우 선택적이고 민감하며 비용 효율적인 센서를 찾을 필요가 있었습니다[92] . 따라서 이 금 나노클러스터는 많은 생명을 구하는 데 도움이 될 수 있는 축복의 역할을 할 수 있습니다[93].
티올기가 있는 생체거대분자는 또한 다른 생물의학 응용에서 AuNC를 준비하기 위해 일반적으로 사용되는 리간드로 적용되었습니다. 최근 트랜스페린(Tf) 기능화된 금 나노클러스터(Tf-AuNCs)/그래핀 옥사이드(GO) 나노복합체(Tf-AuNCs/GO)가 생체 영상화에 활용할 수 있는 턴온 근적외선(NIR) 형광 프로브로 제조되었습니다. 암세포와 작은 동물의 [94]. 암세포에 대한 Tf 수용체(TfR)를 영상화하기 위한 NIR 형광 프로브의 능력은 두 개의 다른 암세포주, 즉 Hela(TfR의 높은 발현 수준) 및 HepG-2(낮은 발현 수준)와 하나의 정상 마우스 세포주를 사용하여 평가되었습니다. (3T3) 그림 8과 같이 TfR의 수준이 다릅니다. 형광 프로브는 분명히 Hela 세포에서만 섭취되었으며, 4시간 배양 후에 눈에 띄는 형광이 관찰되었습니다.
<그림>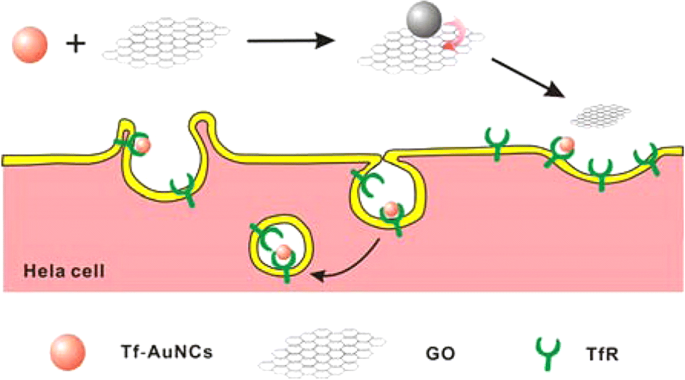
TfR 과발현이 있는 암세포의 생체 영상을 위한 턴온 NIR 형광 프로브로서 Tf-AuNCs/GO 접합의 제작 [94]
Sahoo et al. 은 중합효소연쇄반응(PCR)에서와 같이 단일 가열 및 냉각 주기를 사용하여 DNA에서 고광도 AuNC의 빠른 1단계 녹색 합성(2분)을 개발했습니다. 발광 나노클러스터의 강도는 DNA의 수에 따라 증가하는 것으로 밝혀져 DNA를 정량화하는 쉬운 방법을 제공합니다(그림 9). DNA 정량화를 위한 강력한 형광 프로브로서 AuNC의 능력은 HeLa와 A549를 포함하는 두 가지 다른 암 세포주에서 나타납니다[95]. AuNC의 형성은 전구체(HAuCl4 ) 합성에 사용됩니다. 발광 방출의 강도와 나노클러스터의 양자 결과는 다양한 양의 금에 형성된 클러스터 치수를 기반으로 볼 수 있습니다. AuNC는 A, T, G 및 C로 구성된 다른 염기쌍에 의해 준비되었으며, 다른 염기쌍 조성과 동일한 서열 길이에 대해 동일한 발광을 생성했습니다. 또한, DNA 양에 대한 나노클러스터의 방출 강도 의존성을 식별하는 것은 독특한 테스트 방법을 제공합니다. 유전자 증폭 및 상대 발현의 분석을 얻을 수 있습니다. 또한, AuNC의 생체 적합성은 염료의 전통적인 세포 독성 특성과 비교하여 프로브로서의 사용을 더욱 강조합니다. 다양한 암세포주에서 유전자 발현 수준의 정량적 분석은 복잡하고 강력하며 값비싼 PCR 에너지 기계의 대안으로 간단하고 휴대 가능하며 저렴한 장비를 입증하는 데 사용할 수 있습니다. 또한, 발광 AuNC를 신호 생성제로 사용함으로써 이 도구는 전환 가능한 홀더와 특별히 설계된 소프트웨어를 사용하여 역전사 효소 PCR 및 여러 유전자/단백질의 어레이 기반 분석을 동시에 가능하게 합니다. HeLa 암세포의 세포자살과 관련된 유전자 프로필을 평가하고 글루타티온-S의 발현을 측정하기 위한 장치와 접근 방식이 개발되었습니다. -트랜스퍼라제(GST) 단백질 및 GST 태그 인간 과립구 대식세포 집락 자극 인자(GSThGMCSF) 재조합 단백질 추출 형태 대장균 [96].
<그림>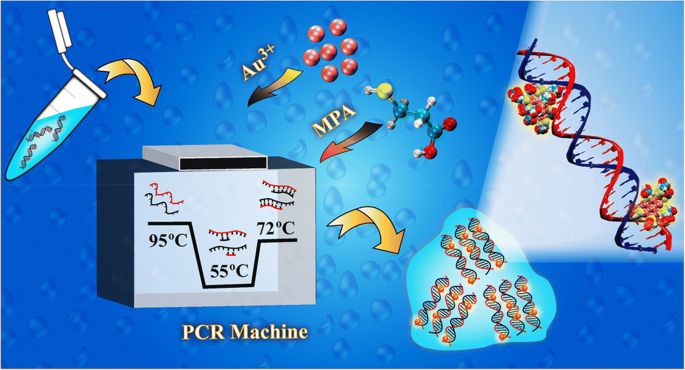
PCR 조건을 모방하여 발광 AuNC를 합성하는 방법 [95]
DNA 및 단백질에서 AuNC의 생체 적합성 신호 생성 물질을 고속으로 준비하면 정성적 검출이 가능합니다. 또한 단일 기기에서 DNA 및 단백질 연구(유체 및 멤브레인 샘플), PCR 앰플리콘 분석 및 멤브레인 기반 연구를 위한 공통 프로브로서 AuNC의 합성 방법을 제공합니다. 이 기기는 시중에서 구할 수 있는 기계에 비해 95% PCR 증폭 효율을 제공할 수 있습니다. 가장 중요한 것은 재료가 모두 환경 친화적이라는 것입니다. 장점, 통합된 도구 및 접근 방식을 사용하면 나노기술과 생물학을 통합하여 기존 기술에 새로운 응용 프로그램을 만들 수 있습니다.
Nguyen et al. AuNC를 안정화하는 이중 리간드를 개발하고 매트릭스 관련 매트릭스 메탈로프로테이나제-9 암을 검출하기 위한 "턴온" 형광 프로브로 AuNC/그래핀 나노복합체를 제작합니다[97]. 펩타이드와 mercapto undecanoic acid를 co-templating 리간드로 사용하여 AuNCs의 생의학적 적용을 위한 부드러운 1단계 방법을 조사했습니다. 메탈로프로테이나제-9 절단 부위가 있는 펩타이드는 안정화제 및 효소 감지를 위한 표적 리간드 역할을 합니다. 효소를 사용하면 산화 그래핀의 우수한 소광 특성과 무시할 수 있는 배경 때문에 AuNC/그래핀 나노물질은 효소 농도와 높은 상관관계가 있는 강력한 "켜짐" 형광 반응을 생성합니다. 나노물질의 검출 한계는 효소의 경우 0.15nM입니다. 형광 나노 물질은 높은 감도와 선택도로 MCF-7 암세포에서 분비되는 "켜진" 메탈로프로테이나제-9의 검출에 대해 성공적으로 입증되었습니다. 또한, 형광 AuNC는 이전 연구에 비해 시간, 비용 및 감각 복잡성을 크게 줄입니다. 이 플랫폼은 또한 환경 및 분석 연구를 포함한 다양한 분야에서 다양한 생물학적 분자를 감지할 수 있는 큰 잠재력을 보여주었습니다. 유사하게, Song et al. Zr 이온의 배위결합에 의해 유도된 인산화 금 나노클러스터 펩타이드(AuNCs-peptides)의 선택적 응집을 기반으로 단백질 키나아제를 검출하는 라벨이 없고 민감하며 간단한 방법을 개발했습니다[98]. AuNC는 펩타이드가 교란되는 것을 방지하는 강력한 환원제 없이 펩타이드로 제조되었습니다. AuNC-peptides를 사용하여 protein kinase CK2의 활성을 측정하는 label-free, green, sensitive, simple 형광에 대한 연구가 개발되었습니다. 최근 확립된 kinase 형광 시험과 비교하여 AuNC-peptide의 사용은 label-free, green 및 간단한 실험 과정을 포함하여 몇 가지 중요한 이점이 있습니다.
Selvaprakash et al. 아데노신-50-삼인산(ATP) 및 피로인산(PPi)과 같은 인산염 함유 대사 산물을 감지하기 위한 스위치 온 감지 프로브로 저렴한 닭 달걀 흰자 단백질(AuNCs@ew)을 사용하여 AuNC를 개발합니다[99]. ATP 및 PPi와 같은 인산염 함유 분자에 대한 형광 AuNC 프로브를 생산하는 비용 효율적이고 직접적인 접근 방식이 얻어졌습니다. 값싼 계란 흰자에 사염화금을 첨가하면 마이크로파 가열로 AuNCs@ew를 쉽게 합성할 수 있습니다. 이 작업에서 AuNCs@ew는 신중한 특성화를 통해 AuNCs@ovalbumin이 주로 지배합니다. 오브알부민은 당단백질이고 풍부한 글리신 리간드를 함유하고 있기 때문에 AuNCs@ew를 글리칸 결합 부위를 포함하는 ConA에 대한 형광 프로브로 사용할 가능성은 Selvaprakash의 연구에서 성공적으로 입증되었습니다.
Wu et al. 소 혈청 알부민(BSA) 및 GSH를 사용하여 각각 330 nm 및 650 nm에서 여기 및 방출로 금 나노클러스터(BSA/GSH-AuNC)를 합성합니다[100]. 이 접근법에서 BSA와 GSH는 주로 각각 제한제와 환원제로 작용합니다. GSH의 도움으로 광안정성 BSA/GSH-AuNC를 합성하는 데 30μM BSA만 필요합니다. GSH를 사용하면 형광 단백질/GSH-AuNC의 개발에 더 이상 BSA 및 트랜스페린과 같은 고가의 단백질을 대량으로 사용할 필요가 없습니다. 이 전략은 단백질 AuNC의 합성을 위한 저비용 접근 방식을 제공하고 또한 확립된 AuNC의 정제를 단순화합니다. Wu et al. NO2 - pH 3.0에서 효율적이고 구체적이었습니다. 높은 내염성, 감도 및 선택성으로 BSA/GSH-AuNC는 복잡한 NO2 측정에 큰 잠재력을 가지고 있습니다. 시료. Caoet al. AuNCs@BSA의 pH 유도 형광 변화와 형광, 원형 이색성(CD) 및 IR 스펙트럼 측정에 의한 리간드 단백질의 적절한 구조적 변화를 조사합니다. 이 작업에서 AuNCs@BSA의 BSA는 2차 및 3차 구조 수준에서 식별 가능한 형태적 변화를 겪습니다. CD 및 IR 결과는 더 불규칙한 구조가 얻어지는 극도의 산성 및 알칼리성에서 두 번째 구조에서 상당한 변화를 해석합니다[101]. AuNCs@BSA와 원래 BSA 간의 2차 구조적 변화 경향의 차이가 표시되었습니다. 극도의 알칼리성 조건(pH 11.43)은 묻힌 나선에 대한 노출로부터 변화를 유도합니다. 더욱이, AuNCs@BSA와 원래의 BSA 사이의 큰 트립토판 형광 갭은 금 핵이 BSA의 트립토판 근처에 산다는 것을 의미합니다. 이 연구는 접합된 AuNC에서 리간드 단백질의 행동 형태를 이해하기 위한 토대를 마련합니다.
Ghosh et al. CD에 대한 AuNC의 영향 및 α-키모트립신(ChT)의 효소 활성(기질 가수분해에 대한 N -숙시닐-1-페닐알라닌 p-니트로아닐리드) [102]. CD 스펙트럼은 AuNC에 결합할 때 ChT가 완전히 노출되어 거의 제로 타원을 생성함을 보여줍니다. ChT 코팅된 AuNC는 사실상 효소 활성을 나타내지 않습니다. 추가 GSH 또는 산화된 GSH는 ChT의 효소 활성을 30-45%만큼 회복시킵니다. ChT의 활성은 AuNC의 결합 표면에서 비가역적으로 손실됩니다. 이 손실된 활성은 ChT가 GSH 또는 산화된 GSH로 처리된 AuNC를 닫을 때 복구될 수 있습니다. 세포에서 효소 활성은 이 연구에서 볼 수 있듯이 GSH에 의해 소생될 수 있습니다. 암세포는 높은 수준의 글루타티온이 특징이므로 암세포와 정상 세포 사이에 효소가 함유된 금기의 흡수에 차이가 있을 것입니다.
형광 유도 수술이라는 새로운 기술은 수술 중 조직을 절제해야 할지 아니면 보존해야 할지 결정하는 데 도움이 되는 수술 과정에 도입되었습니다[103]. 이러한 성과는 환자 결과의 큰 개선을 위한 암 수술의 패러다임 전환을 확립할 수 있습니다. 이 분야의 최근 연구 진행은 종양 조직 절제 동안 정확한 안내를 제공하기 위한 형광 유도 프로브로서 디아트리조산 및 표적 특이적 AS1411 앱타머와 접합된 형광 AuNC의 사용에 초점을 맞추었습니다. 생체 내 실험은 CL1-5 종양 보유 마우스의 종양 위치가 분자 영상 조영제로 AuNC 접합체를 사용하여 선명한 CT 이미지에서 관찰되었음을 입증했습니다. 더 중요하게는, AuNC 접합체의 명확하게 보이는 주황색-적색 형광이 수술 중 형광 안내에 의해 CL1-5 종양의 절제를 돕는 데 활용되었습니다. 절제된 종양의 강력한 형광 향상은 형광 AuNC 접합체를 사용하여 성공적인 분자 표적화를 입증하는 생체 내 이미징 시스템 데이터를 기반으로 합니다. 이 작업은 생체 내에서 표적 특이적 형광 AuNC 접합체를 사용하여 장기간 형광 이미징 시간, 높은 광안정성, 이중 이미징 기능 및 대부분의 유기물과 비교하여 특정 표적 분자로 실현 가능한 표면 수정을 제공할 수 있는 큰 이점을 입증했습니다. 현재 사용되는 조영제. 또한, 이 작업은 기능화된 AuNC를 사용하여 생물의학 영상 및 치료 분야에서 고급 개념을 가져왔습니다.
전반적으로, 우리는 생체 영상, 검출 및 치료에 적용하기 위해 소분자, 중합체 및 생체 거대분자로 준비된 형광 AuNC의 최근 발전에 대한 간략한 검토를 제공했습니다(표 1). 이러한 연구는 형광 AuNC가 우수한 생체 적합성, 높은 광안정성 및 쉬운 표면 변형과 같은 독특한 특성으로 인해 유망한 형광 프로브가 될 수 있음을 보여주었습니다. AuNC는 다양한 생물 의학 응용 분야에서 입증되었지만 형광 양자 수율(QY)은 여전히 낮습니다(보통 20% 미만). AuNC의 적용을 확장하기 위한 첫 번째 과제는 높은 형광 QY를 가진 AuNC의 준비에 중점을 둡니다. With low fluorescence QY, the synthesis of AuNCs with uniform size will be an alternative way to improve their fluorescence QY. Furthermore, with the uniform size, fluorescent AuNCs with a narrow emission spectrum will increase their benefit in biomedical applications. The second challenge for AuNCs is the control of ligand on their surface because the chemical and physical properties of AuNCs can be significantly affected by their surface modification. Therefore, the theoretical and practical studies of AuNCs are still needed to have a better understanding of their structure, optical characteristic, and physicochemical property. Especially, for physicochemical property, recent studies have proven that AuNCs are potential fluorescent probes for biosensing, bioimaging, and cancer therapy. Accordingly, to realize the biomedical applications, we still have a lot of works to push the biomedical applications of AuNCs in imaging, detection, and therapy. Overall, with the great efforts, we believe that AuNCs will be served as a significant fluorescent probe in biomedical application in the near future.
Gold nanoclusters
Bovine serum albumin
Cord blood mononuclear cells
Circular dichroism
Chitosan
Chymotrypsin
Dihydrolipoic acid
D-penicillamine
디티오트레이톨
Folic acid
Fluorescence lifetime imaging
Förster 공명 에너지 전달
Glutathione
Glutathione-S -transferase
11-Mercaptoundecanoic acid
Ovalbumin
Polymerase chain reaction
Poly(DBAM-co-NASco-HEMA)
Polyethyleneimine
Pyrophosphate
Multidentate thioether-terminated poly(methacrylic acid)
Surface plasmon-enhanced energy transfer
Transferrin
Trypsin
Vancomycin
나노물질
이전 기사에서는 블록체인이 작동하는 방식과 안전한 이유를 설명하고 공급망 및 자산 추적과 같은 물류에 블록체인을 사용하는 방법을 소개했습니다. 이 기사에서는 산업 자동화에서 블록체인에 대한 예제와 잠재적인 응용 프로그램을 계속 제공할 것입니다. 블록체인 및 IoT 사물 인터넷(IoT)은 전 세계적으로 수백만 개의 애플리케이션을 보유하고 있지만 동시에 많은 보안 위험에 노출되어 있습니다. 악의적인 공격자가 무선 카메라, Amazon Alexa, 스마트 온도 조절기 등의 IoT 제품을 해킹하여 데이터를 훔쳤다는 소식을 종종 듣습니
3D 레진 프린팅은 모든 유형의 사용자가 사용할 수 있을 때까지 3D FDM 프린팅과 동일한 방식으로 발전했습니다. 3D 레진 프린터 사용을 통한 이러한 새로운 움직임은 광범위한 레진 개발로 이어졌습니다. 매우 다양한 특성과 용도를 가지고 있습니다. 이 기사에서는 기존 수지의 유형 및 용도를 설명하고 명확히 하려고 합니다. 3D 수지 프린터용(SLA, DLP, LED/LCD, LFS 등). 수지의 종류 대부분의 사용자는 FDM 기술 내의 재료 유형에 대해 잘 알고 있지만 3D 레진 프린팅을 시작할 때 일반적으로 레진 유형에 대한