나노물질








저분자 CO, H2의 기체 흡착 거동 오, H2 S, NH3 , SO2 , 및 순수 펜타 그래핀(PG)에 대한 NO는 고급 가스 감지 재료로 사용할 가능성을 조사하기 위해 첫 번째 원칙 계산을 사용하여 조사되었습니다. 결과는 CO를 제외하고 H2를 보여줍니다. 오, H2 S, NH3 및 SO2 상당한 흡착 에너지와 적당한 전하 이동으로 펜타 그래핀 표면에 물리적으로 흡착되는 반면, NO는 펜타 그래핀 표면에 화학적으로 흡착되는 경향이 있습니다. 또한, PG의 전자적 특성은 H2 이후에 효과적으로 수정될 수 있습니다. 오, H2 S, NH3 , SO2 , NO가 흡착되고 펜타-그래핀은 전하 이동 메커니즘을 통해 가스 센서에 사용할 가능성이 있습니다.
<섹션 데이터-제목="배경">가스 감지, 특히 오염 또는 독성 가스 감지는 항상 환경 오염 모니터링, 산업 제어, 농업 생산 및 의료 진단 분야의 응용과 관련된 연구의 초점이었습니다[1]. 최근에는 점점 더 많은 2차원 물질이 예측되고 합성되고 있다[2,3,4]. 2차원 물질은 넓은 표면적, 초고 캐리어 이동도, 낮은 전기적 잡음과 같은 매력적인 특성을 나타내기 때문에 가스 감지 요소로 광범위하게 조사되고 사용되었습니다[5]. 2차원 물질의 전자적 특성은 특정 기체 분자가 흡착된 후에 변할 수 있다고 보고되었습니다[6, 7].
2차원 물질 중에서 특히 그래핀과 그 유사체는 나노전자공학과 나노역학 모두에 응용할 수 있는 놀라운 물리적 특성과 잠재력으로 주목을 받고 있다[8,9,10,11,12]. 그래핀은 차세대 전자소자에 가장 적합한 호스트 재료 중 하나로 널리 알려져 있지만[13], 안정적인 sp 2 탄소 결합의 혼성화와 제로 갭 특성으로 인해 가스 흡착에 비효율적이며 이는 가스 센서 설계에 불리합니다. 또한 그래핀은 전기전도도가 우수한 전도체이다[8]. 반도체에 비해 기체 흡착 과정에서 저항 정보를 측정하기 어렵고 그래핀은 기체의 농도 변화에 둔감하다. 따라서 그래핀은 밴드갭을 열고 반도체로 작용할 수 있는 기능화가 필요하다[10]. 실험적 특성화의 한계로 인해 그래핀 표면에 대한 분자의 흡착 거동이 1원칙 계산에 의해 광범위하게 조사되었으며 이는 그래핀의 응용에 의미가 있다[14,15,16].
벌크 T12 탄소에서 박리될 수 있는 PG(Penta-graphene)는 가장 최근에 제안된 그래핀 동소체 중 하나로 탄소 오각형 구조가 반복되어 구성되어 있다[17]. 일부 조사에서는 PG가 고정 격자 상수로 안정적이라고 예측했습니다[17, 18]. 벌집 구조를 가지며 저온 CO 산화를 위한 유망한 금속이 없는 저비용 촉매입니다[19]. 질소 도핑된 PG는 매우 높은 촉매 활성을 나타내며 속도 제한 단계의 매우 작은 에너지 장벽으로 인해 저온 CO 산화를 위한 많은 금속 기반 및 탄소 기반 촉매와 더 경쟁력이 있습니다[20]. 또한 전이 금속이 도핑된 PG가 잠재적인 수소 저장 물질이라고 보고되었습니다[21]. 또한 그래핀과 달리 PG는 1.52–4.48 eV 범위의 밴드 갭을 갖는 진성 준직접 밴드 갭 반도체이며[8, 17, 22] 반도체 가스 센서에 적용할 수 있는 엄청난 잠재력을 의미합니다. 또한 PG는 sp 3 및 sp 2 탄소 결합. sp의 사면체 특성으로 인해 3 탄소 결합의 혼성화, PG는 이상적으로 평면이 아니라 주기적인 주름 방식으로 평면을 벗어나 진동하며[17], 감지 요소로서 가스 흡착을 위한 더 많은 가능한 위치를 나타냅니다.
작은 가스 분자와 깨끗한 PG 사이의 상호 작용에 대한 조사는 지금까지 거의 없었습니다. 실험 방법의 한계로 인해 본 연구에서는 작은 기체 분자(즉, CO, H2)의 흡착 거동을 조사하기 위해 밀도 기능 이론(DFT) 계산을 수행했습니다. 오, H2 S, NH3 , SO2 , 및 NO) 신규 탄소 재료 PG에 대한. 이 연구는 작업자가 가스 센서에 적용된 PG의 성능을 분석하고 예측하는 데 도움이 될 것입니다.
본 연구에서는 Dmol
3
에 구현된 DFT[23]를 기반으로 하는 제1원칙 계산에 의해 구조적 최적화 계산을 수행했습니다. 코드 [24]. LDA(local-density approximation)는 기체-분자-흡착 시스템을 연구하는 데 적합하며[25, 26], 이 조사에서 구조적 최적화를 위해 LDA-PWC가 선택되었습니다. 기체-분자 흡착 연구에서 van der Waals 상호작용을 무시하는 것을 피하기 위해 Ortmann, Bechstedt 및 Schmidt[27]의 방법이 사용되었습니다. 2 × 2 × 1 Monkhorst-Pack 메쉬[28]는 Brillouin-zone 통합에 사용되었으며, 여기에서 자체 일관된 필드 허용 오차는 1 × 10
− 5
으로 설정되었습니다. 하아. 최대 에너지 변화, 최대 힘, 최대 변위에 대한 에너지의 수렴 정밀도가 1 × 10
− 5
일 때 시스템은 바닥 상태에 도달합니다. Ha, 각각 0.002 Ha/Å, 0.005 Å입니다. 다중 코어 병렬 컴퓨팅이 수행되었고[29], NO 흡착 계산에 스핀 분극이 적용되었습니다. 30Å의 진공 공간을 갖는 3 × 3 슈퍼셀[21]은 두 개의 sp를 포함하는 단위 셀을 기반으로 모델링되었습니다.
3
-혼성화된 탄소(C1) 원자와 4개의 sp
2
-하이브리드화된 탄소(C2) 원자[17], 그림 1 참조, 여기서 C1 및 C2 원자는 각각 검은색 및 회색 구체로 구분됩니다. 기체 분자는 3.5Å의 초기 거리에서 기판에 수평으로 위치했습니다. 가스 분자의 가장 유리한 흡착 위치를 얻기 위해 4개의 가능한 위치, 즉 C1 원자의 상단(T1), C2 원자의 상단(T2), PG의 홈 중간(T
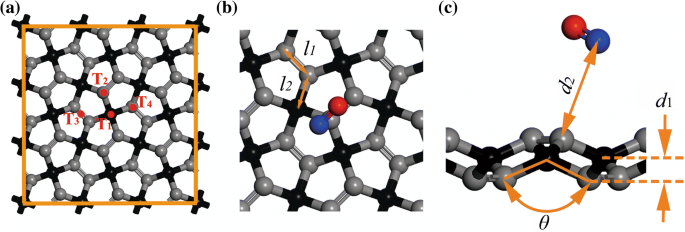
PG의 구조 및 기하학:a 3 × 3 슈퍼셀, b 단위 셀의 전면 보기 및 c 흡착물-PG 원자의 측면도. 두 C2 원자 사이의 거리, C1과 C2 원자 사이의 거리, PG의 두께 및 C2-C1-C2 천사를 l로 정의합니다. 1 , 나 2 , d 1 , 및 θ , 각각
시스템의 흡착능력을 정량적으로 평가하기 위해 LDA-PWC 외에 흡착에너지(E 아 ), 요금 이전(Q ) 및 흡착 거리(d 2 , 그림 1에 도시된 바와 같이 연구에서 Perdew-Wang 1991(PW91) 및 Perdew-Burke-Ernzerh(PBE)와 함께 GGA(generalized gradient approximation) 함수를 사용하여 계산되었습니다. d 2 평형 상태에서 PG와 기체 분자 사이의 가장 가까운 원자 거리로 정의됩니다. 질문 는 기체 분자의 Mulliken 전하를 나타내고 [30, 31] 음수 값은 PG에서 기체 분자로의 전하 이동을 의미합니다. 흡착 에너지는 다음과 같이 계산됩니다.
$$ {E}_a\kern0.5em =\kern0.5em {E}_{\left(\mathrm{PG}\kern0.5em +\kern0.5em \mathrm{분자}\right)}\kern0.5em -\kern0.5em {E}_{\mathrm{PG}}\kern0.5em -\kern0.5em {E}_{\mathrm{분자}}, $$ (1)여기서 E (PG + 분자) , E PG , 및 E 분자 는 각각 흡착질-PG 평형 시스템, 분리된 PG 및 분리된 기체 분자의 총 에너지입니다. 흡착 시스템의 전자 구조 계산에서 더 높은 정확도를 위해 GGA와 PBE 교환 상관 함수를 사용하는 DFT 계산이 사용되었습니다[2, 32].
구조 최적화 후, 이 백서에 보고된 원시 PG의 계산된 구조 매개변수(l 1 =1.342 Å, l 2 =1.551 Å, θ =133.9°, d 1 =0.612 Å)는 이전 연구[17]와 일치하는 것으로 나타났습니다. 가장 낮은 E를 선택하여 (PG + 분자) 또는 E 아 4개의 흡착 위치 T1에서 T4까지 (추가 파일 1의 표 S1 참조), 단층 PG의 가스에 대한 가장 유리한 흡착 구성이 그림 2에 표시되어 있고 가장 유리한 흡착 위치(즉, T1 , T2 , T3 , 또는 T4 )는 표 1에 나열되어 있습니다. 다음 텍스트에서 계산된 결과는 이러한 가장 유리한 흡착 구성을 기반으로 얻은 것입니다. 최근 연구에 따르면 단층 InSe, 그래핀 및 청색 인이 가스 센서에 사용하기에 큰 가능성이 있음이 밝혀졌습니다[14, 33, 34]. 본 연구에서 계산된 E 아 CO 값, H2 O, NH3 InSe [33]의 경우 각각 − 0.531, − 0.900 및 − 1.069eV인 반면(표 1 참조), 각각 − 0.120, − 0.173 및 − 0.185eV입니다. CO의 경우 H2 오, NH3 , 및 그래핀 표면의 NO, 계산된 E 아 값은 각각 − 0.014, − 0.047, − 0.031 및 − 0.029eV입니다[14]. 한편, E 아 H2 값 S 및 SO2 PG의 가스는 각각 - 1.345 및 - 1.212 eV이며, 이는 청인의 경우 각각 - 0.14 및 - 0.20 eV보다 훨씬 큽니다[34]. 분명히 계산된 E 아 PG에 있는 이러한 가스 분자의 값은 다른 물질에서 얻은 값보다 훨씬 커서 이러한 가스 분자가 PG의 표면에 쉽게 흡착된다는 것을 나타냅니다[35]. 계산된 E를 고려하면 아 CO의 값이 다른 가스의 값보다 훨씬 작기 때문에 CO의 흡착이 가장 약할 수 있습니다. 한편, 표 1에서 NO의 흡착 에너지는 H2와 같은 물리적 흡착(비공유) 흡착물의 일부보다 작습니다. S, NH3 및 SO2 . 이것은 물리적 흡착과 달리 NO의 화학적 흡착이 PG의 명백한 변형을 유도하여 추가 에너지를 소비하고 계산된 흡착 에너지 E를 줄이는 이유에 의해 설명될 수 있습니다. 아 , 추가 파일 1에 소개된 대로. 유사하게, NO2의 화학적 흡착에서도 명백한 변형이 관찰될 수 있습니다. 안티몬[5]의 표면에 존재하여 상대적으로 낮은 흡착 에너지를 유발할 수 있습니다. 또한 NO를 제외하고 d의 값은 2 표 1에 나열된 가스 분자의 해당 원자와 PG의 C 원자의 공유 반지름의 합보다 분명히 더 큽니다(즉, l C-O =1.38 Å, l C-H =1.07 Å, l C-N =1.46 Å, l CS =1.78 Å) [36], 이러한 기체 분자는 물리적으로 흡착되는 경향이 있음을 보여줍니다. NO와 관련하여 d의 값은 2 흡착 시스템에서 1.541Å은 공유 결합 범위에 있으며 이 경우 화학 결합이 존재할 수 있음을 나타냅니다.
<그림>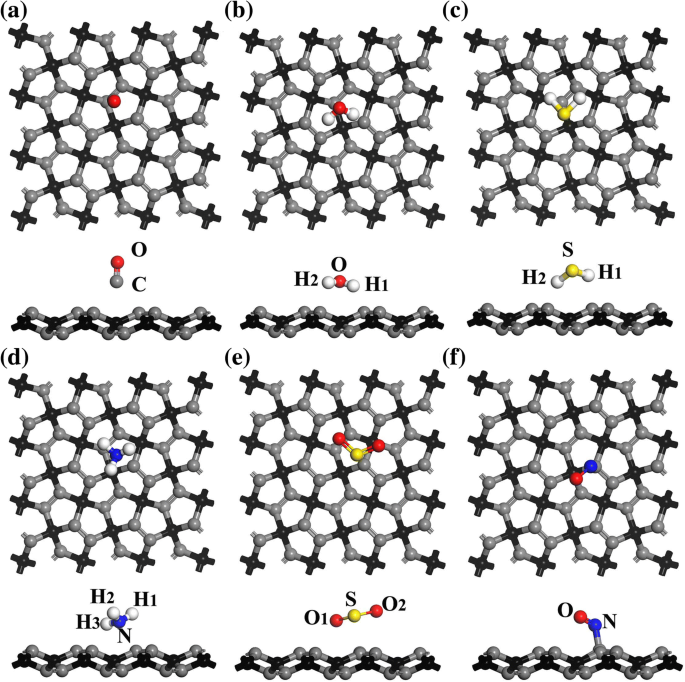
a에 대한 가장 유리한 흡착 구성의 평면도 및 측면도 CO, b H2 오, ㄷ H2 S, d NH3 , e SO2 , 및 f PG에 없습니다. 회색, 빨간색, 흰색, 노란색 및 파란색 구체는 각각 C, O, H, S 및 N 원자를 나타냅니다.
InSe 및 인화붕소에 대한 이전 연구에서는 흡착된 분자가 전하 수용체 또는 공여체로 작용하여 기판의 저항을 변화시키는 것으로 나타났습니다[33, 37]. 질문 CO, H2에 대한 값 오, H2 S, NH3 , SO2 , 및 PG 표면의 NO는 각각 0.023, 0.082, 0.133, 0.169, - 0.109 및 - 0.03e(표 1 참조)이며, 이는 CO, H2 오, H2 S 및 NH3 SO2 동안 전자를 PG에 기부 NO는 PG로부터 전자를 얻는다. Q CO 값, H2 오, NH3 , 및 InSe 표면의 NO는 각각 0.006, 0.014, − 0.025 및 0.018e이며[33], CO, H2의 경우 오, NH3 , 및 그래핀 표면의 NO는 각각 0.012, - 0.025, 0.027, 0.018 e로[14], 이는 PG 상의 기체 분자의 전자의 득실이 InSe 및 그래핀보다 더 명백함을 나타낸다. 또한, NO와 PG 사이에 화학적 흡착이 발생할 수 있지만 전하 이동은 - 0.030e에 불과합니다. 이것은 N 및 O 원자의 Mulliken 전하 분포가 화학적 흡착 전후에 상당히 다르다는 사실로 설명될 수 있습니다(추가 파일 1의 표 S2 참조). O 원자의 이득 전자는 N 원자의 손실 전자를 상쇄하여 NO의 총 전하 이동이 크지 않은 반면 NO와 PG 사이의 전자 상호 작용은 여전히 분명합니다. InSe 및 InN 표면의 작은 가스 분자의 전하 이동 감지 메커니즘에 따르면 [33, 38], PG는 전하 이동 메커니즘을 기반으로 하는 가스 센서에 사용할 수 있는 큰 잠재력을 가질 수 있다고 추측됩니다.
또한, PG에 대한 가스 흡착 계산은 두 개의 GGA 기능인 PW91 및 PBE를 사용하여 수행되었습니다. E의 계산된 값 아 , 질문 , 및 d PG의 가스 분자에 대한 목록은 표 2에 나와 있습니다. E 아 PW91과 PBE에 의해 계산된 값은 LDA에 의해 계산된 것보다 작은 반면, PW91과 PBE는 더 큰 d를 제공합니다. 2 LDA에 비해 LDA와 달리 GGA는 일반적으로 흡착 에너지를 과소 평가하고 결합 거리를 과대 평가하는 경향이 있어 이전 연구 결과와 일치합니다[26, 31]. 이 세 가지 기능의 결과 경향이 일관적이라는 점은 언급할 가치가 있습니다. 예를 들어, E의 계산된 값 아 CO가 가장 작고 계산된 값 E 아 H2의 S 및 SO2 다른 기체 분자보다 크다. 또한 d의 계산된 값은 2 LDA, PW91 및 PBE 기능에 대한 NO의 값은 각각 1.514, 1.592, 1.591Å이며 모두 공유 결합 범위에 있습니다[36].
PG의 전자적 특성에 대한 가스 분자의 영향에 대한 더 나은 이해를 얻기 위해 분자-PG 시스템의 상태 밀도(DOS)가 계산되었습니다(그림 3 참조). 분명히 페르미 준위(이 f , 예를 들어 − 2.5 ~ 2.5eV 범위에서) H2의 전자 수준의 명백한 기여가 있습니다. 오, H2 S, NH3 , SO2 , 및 NO는 흡착 시스템에 대한 것으로, 이러한 가스 분자의 존재가 PG의 전자 특성에 큰 영향을 미칠 수 있음을 나타냅니다[5, 37]. 예를 들어 H2의 경우 S, 전자 레벨의 명백한 기여는 0eV에 있습니다. 그림 3c를 참조하십시오. PG 표면의 CO와 관련하여 흡착 시스템에서 CO의 궤도 피크는 − 8.0, − 5.7, − 2.9 및 4.0eV에 위치하며 E 근처에서 명백한 궤도 기여가 없습니다. f . 또한 밴드 갭은 재료의 전자 특성을 결정하는 중요한 요소이기도 합니다[26, 34].
<그림>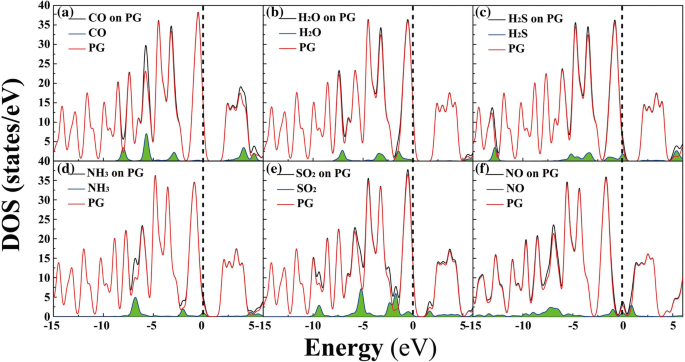
분자-PG 시스템(검정색)에 대한 총 전자 밀도(DOS) 및 흡착 시스템에서 소분자(녹색 그림자가 있는 파란색 선) 및 PG(빨간색)에 대한 예상 DOS:a CO, b H2 오, ㄷ H2 S, d NH3 , e SO2 , 및 f 아니요. 페르미 레벨은 0으로 설정됩니다(점선 참조)
흡착 시스템의 밴드 갭 및 해당 밴드 구조는 그림 4에 나와 있으며, 여기서 CO, H2의 밴드 갭 오, H2 S, NH3 , SO2 및 PG의 NO는 각각 2.15, 2.02, 1.86, 1.81, 1.61, 0eV입니다. 대조적으로 깨끗한 PG의 밴드 갭은 2.21eV입니다(추가 파일 1:그림 S2 참조). 분명히, CO를 제외하고 H2의 기체 흡착 오, H2 S, NH3 , SO2 , NO는 PG의 전자적 특성에 분명한 영향을 미치며 이는 DOS의 결과와 일치한다. 이러한 모든 결과는 CO를 제외하고 H2 이후에 PG의 전자적 특성이 효과적으로 수정될 수 있음을 나타낼 수 있습니다. 오, H2 S, NH3 , SO2 , 및 NO가 흡착되어 가스 감지에 중요합니다.
<그림>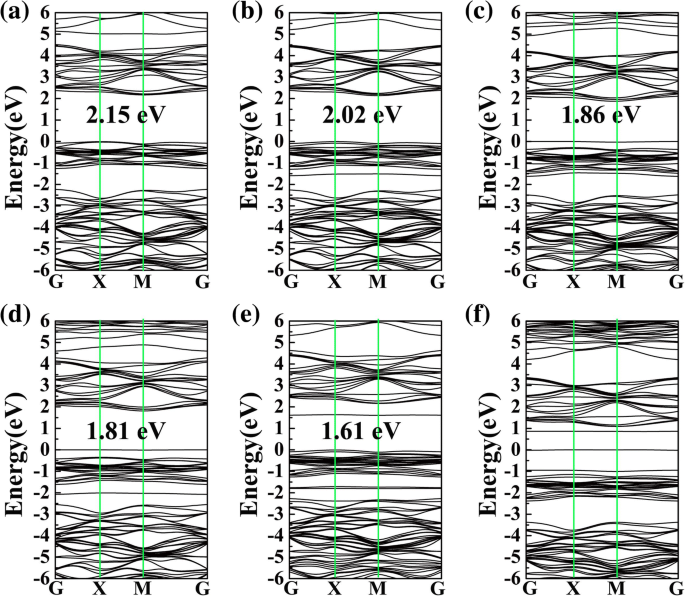
CO의 밴드 구조(a ), H2 오(b ), H2 S(c ), NH3 (d ), SO2 (이 ) 및 아니요(f ) PG 표면에
d 2 PG의 NO 값은 결합 범위에 있으며 시스템에서 NO의 전자 수준은 주로 E 주변에 국한됩니다. f , 화학적 흡착이 일어나는 것으로 추측된다. NO와 PG 사이의 흡착 메커니즘에 대한 깊은 이해를 위해 PG에 대한 NO의 예상 밀도 밀도(PDOS)와 전자 국부화 함수(ELF)가 그림 5에 표시됩니다. 분명히, N <나는>p 그리고 O p 원자는 주로 − 6.9, − 0.9, 0 및 0.8 eV에 위치합니다. 따라서 그림 5a에 표시된 것처럼 NO에는 분자 내 혼성화가 있습니다. 한편, 페르미 준위 근처에서 PG의 NO와 C 원자 사이의 궤도 혼합이 관찰될 수 있으며, 이는 주로 C s , C p , N s , N p , 및 O p 궤도. 궤도 혼합은 그림 5b에 표시된 것처럼 NO의 N과 PG의 C 사이에 화학 결합을 유도합니다. 따라서 PG는 NO 가스를 감지하거나 촉매하는 데 사용할 수 있습니다[5, 39]. 또한, 다른 가스 분자의 흡착 유형을 확인하기 위해 다른 흡착 시스템의 ELF도 계산됩니다(추가 파일 1:그림 S3 참조). 분명히, CO의 경우 H2 오, H2 S, NH3 그리고 SO2 , 기체 분자와 기질 사이에 화학 결합이 없으므로 시스템이 물리적 흡착 경향이 있음을 나타냅니다.
<그림>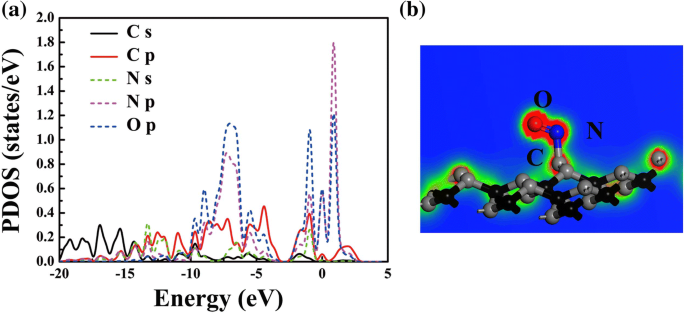
원자 투영 DOS(a ) 및 NO-PG(b)의 전자 국소화 함수(ELF) )
요약하자면 H2 오, H2 S, NH3 및 SO2 가스는 상당한 흡착 에너지와 적당한 전하 이동으로 단층 PG에 물리적으로 흡착됩니다. 약한 물리적 흡착, 작은 흡착 에너지 및 전하 이동을 위해 순수한 PG는 CO 검출에 적합하지 않습니다. PG, CO, H2 표면의 이러한 가스 분자에 대해 O 및 H2 S 및 NH3 PG에 전자를 기증하는 동안 SO2 NO는 PG로부터 전자를 얻는다. 더욱이, 페르미 준위 근처에서 H2의 전자 준위의 명백한 기여가 있습니다. 오, H2 S, NH3 , SO2 , 그리고 흡착 시스템의 DOS에 NO, PG의 전자 특성이 H2 후에 효과적으로 수정될 수 있음을 나타냅니다. 오, H2 S, NH3 , SO2 , NO가 흡착됩니다. 또한, PG에 대한 NO의 흡착은 화학적 흡착의 경향이 강하므로 PG는 NO 가스를 검출하거나 촉매화하는 데 사용할 수 있습니다. 따라서 Pristine PG는 가스 감지 응용 분야에서 큰 잠재력을 가지고 있습니다.
2차원
밀도 함수 이론
상태 밀도
전자 현지화 기능
일반화된 기울기 근사
국소 밀도 근사
퍼듀-버크-에른처
상태의 예상 밀도
펜타그래핀
퍼듀왕 1991
Perdew-Wang 상관 관계
나노물질
초록 SF6 , 우수한 절연 매체로 고압 절연 장치에 널리 사용되어 전원 시스템의 안전한 작동을 보장합니다. 그럼에도 불구하고 장기간 사용되는 장치에서 불가피한 부분방전은 SF6의 분해를 유발합니다. 절연 성능을 저하시킵니다. 이 작업에서 DFT 계산은 ZnO로 변형된 C3의 흡착 및 감지 특성을 연구하기 위해 수행되었습니다. N(ZnO-C3 N) SF6 쪽으로 나노시트 SF6의 운영 현황을 평가하기 위한 새로운 나노 후보를 제안하기 위해 분해된 제품 절연 장치. 우리는 먼저 ZnO-C3의 구조를 조사했습니다. N 단층 및 네 가
초록 우리는 1.5~21nm의 잘 제어된 폴리(메틸 메타크릴레이트)(PMMA) 간격 두께에서 금 나노 입자(NP) 근처의 하위 단층 로다민 6G 분자의 형광을 조사합니다. 금 NP의 플라즈몬 공명 피크는 두께가 다른 PMMA 스페이서에 의해 530~580nm로 조정됩니다. 그런 다음 플라즈몬 공명 여기 향상으로 인해 562nm에서 로다민 6G 분자의 방출 강도가 향상되고 PMMA 스페이서 두께가 증가함에 따라 감소하는 것으로 나타났습니다. 유한 차분 시간 영역 방법에 의해 시뮬레이션된 스펙트럼 강도의 변화는 실험 결과와 일치합니다