제조공정








<시간 />
인체의 가장 큰 기관인 피부는 질병과 신체적 손상으로부터 신체를 보호하고 체온 조절에 도움을 줍니다. 그것은 표피와 진피의 두 가지 주요 층으로 구성됩니다. 표피 또는 외부 층은 주로 각질 세포, 멜라닌 세포 및 랑게르한 세포로 구성됩니다. 콜라겐과 같은 결합 조직 섬유로 주로 구성된 진피는 표피에 영양을 공급합니다.
피부가 질병이나 화상으로 심각하게 손상되면 신체는 필요한 대체 세포를 생성할 만큼 충분히 빠르게 행동할 수 없습니다. 당뇨병 환자가 겪는 피부 궤양과 같은 상처는 치유되지 않을 수 있으며 사지를 절단해야 합니다. 화상 피해자는 감염 및 혈장 손실로 사망할 수 있습니다. 피부 이식은 이러한 결과를 예방하고 기형을 교정하기 위한 방법으로 개발되었습니다. 기원전 6세기 <작은> , 힌두교 외과 의사들은 환자의 코에서 피부 피판을 이식하는 코 재건에 참여했습니다. 이탈리아 의사인 Gaspare Tagliacozzo는 16세기에 이 기술을 서양 의학에 도입했습니다.
20세기 후반까지 피부 이식은 환자 자신의 피부(자가 이식) 또는 사체 피부(동종 이식)로 구성되었습니다. 감염 또는 사체 피부의 경우 거부 반응이 주요 관심사였습니다. 환자의 신체의 한 부분에서 다른 부분으로 이식된 피부는 거부 반응에 면역이 있는 반면 기증자로부터 수혜자에게 이식된 피부는 다른 조직 이식이나 이식보다 더 적극적으로 거부됩니다. 사체 피부는 화상 환자의 초기 치유 기간 동안 감염 및 체액 손실로부터 보호할 수 있지만 환자 자신의 피부를 이식해야 하는 경우가 많습니다. 의사는 환자가 사용할 수 있는 피부로 제한되어 있으며 심각한 화상 환자의 경우 결정적인 단점입니다.
1980년대 중반, 세포 생물학 및 플라스틱 제조 분야에서 일하는 의료 연구원과 화학 공학자들은 감염 및 거부 반응의 발생률을 줄이기 위한 조직 공학을 개발하기 위해 힘을 합쳤습니다. 조직 공학의 촉매제 중 하나는 이식에 사용할 수 있는 장기의 부족이 증가했다는 것입니다. 1984년, 하버드 의과대학 외과의사인 Joseph Vacanti는 사용 가능한 간 부족에 대한 불만을 Massachusetts Institute of Technology의 화학공학자인 Robert Langer와 공유했습니다. 그들은 함께 실험실에서 새로운 장기를 키울 수 있을지 고민했습니다. 첫 번째 단계는 신체의 조직 생산을 복제하는 것이었습니다. Langer는 포경수술 중에 제거된 기증된 신생아 포피에서 추출한 세포인 섬유아세포를 사용하여 피부 세포가 성장할 수 있는 생분해성 스캐폴딩을 구축하는 아이디어를 생각해 냈습니다.
다른 연구자들이 개발한 이 기술의 변형에서 추출된 섬유아세포는 결합 조직에서 발견되는 섬유질 단백질인 콜라겐에 추가됩니다. 화합물이 가열되면 콜라겐은 겔화되고 섬유아세포를 가두는데, 섬유아세포는 차례로 콜라겐 주위에 배열되어 조밀하고 밀도가 높으며 섬유질이 됩니다. 몇 주 후, 기증된 포피에서도 추출된 각질세포가 새로운 진피 조직에 주입되어 표피층을 만듭니다.
인공 피부 이식은 환자와 시체에서 파생된 것보다 몇 가지 장점이 있습니다. 그것은 조직의 필요성을 제거합니다 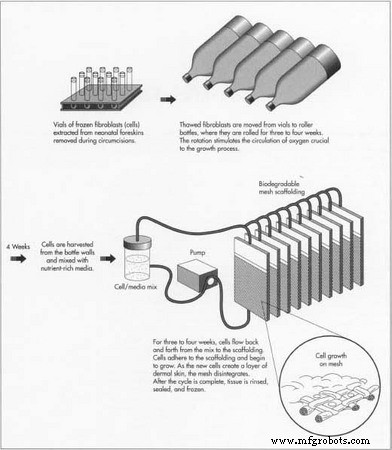 타이핑. 인공 피부는 대량으로 만들어 보관 및 운송을 위해 냉동하여 필요에 따라 사용할 수 있습니다. 각 배양물은 병원체에 대해 스크리닝되어 감염 가능성을 크게 줄입니다. 인공피부는 수지상세포, 모세혈관내피세포 등 면역원성 세포가 없기 때문에 체내에서 거부반응이 일어나지 않는다. 마지막으로 재활 시간이 크게 단축됩니다.
타이핑. 인공 피부는 대량으로 만들어 보관 및 운송을 위해 냉동하여 필요에 따라 사용할 수 있습니다. 각 배양물은 병원체에 대해 스크리닝되어 감염 가능성을 크게 줄입니다. 인공피부는 수지상세포, 모세혈관내피세포 등 면역원성 세포가 없기 때문에 체내에서 거부반응이 일어나지 않는다. 마지막으로 재활 시간이 크게 단축됩니다.
인공 피부 생산에 필요한 원료는 생물학적 성분과 필요한 실험실 장비의 두 가지 범주로 나뉩니다. 기증된 피부 조직의 대부분은 포경수술 중에 제거된 신생아 포피에서 나옵니다. 하나의 포피는 4에이커의 접목 재료를 만들기에 충분한 세포를 생산할 수 있습니다. 섬유아세포는 기증된 조직의 진피층에서 분리됩니다. 섬유아세포는 바이러스 및 IIV, B형 및 C형 간염, 마이코플라스마와 같은 기타 감염성 병원체에 대한 검사를 받는 동안 격리됩니다. 어머니의 병력이 기록됩니다. 섬유아세포는 유리병에 보관되고 -70°C(-94°F)의 액체 질소에서 동결됩니다. 유리병은 배양물을 성장시키는 데 섬유아세포가 필요할 때까지 동결된 상태로 유지됩니다. 콜라겐 방법에서는 포피에서 각질 세포도 추출하여 테스트하고 동결합니다.
섬유아세포가 메쉬 스캐폴딩에서 성장하려면 봉합사를 용해하는 데 사용되는 동일한 요소인 젖산과 글리콜산 분자를 결합하여 중합체를 만듭니다. 화합물은 화학 반응을 거쳐 반복되는 구조 단위로 구성된 더 큰 분자를 생성합니다.
콜라겐 방법은 어린 송아지의 신근 힘줄에서 소량의 소 콜라겐을 추출합니다. 콜라겐은 산성 영양소와 혼합되어 4°C(39.2°F)의 냉장고에 보관됩니다.
실험실 장비에는 유리병, 튜브, 롤러 병, 접목 카트리지, 금형 및 냉동기가 포함됩니다.
제조 과정은 믿을 수 없을 정도로 간단합니다. 주요 기능은 추출한 섬유아세포가 인체에 있다고 믿게 하여 자연스러운 방식으로 서로 소통하여 새로운 피부를 만드는 것입니다.
의료계는 인공 피부 기술을 사용하여 장기 재건을 개척하고 있습니다. 예를 들어, 이 소위 조작된 구조적 조직은 손상된 관절과 뼈를 대체하기 위해 현재 사용되는 플라스틱 및 금속 보철물을 언젠가 대체할 것으로 기대됩니다. 폴리머 메쉬에 연골 세포를 파종하여 귀와 코를 재구성합니다. 유방 및 요도 조직의 재생은 현재 실험실에서 연구 중입니다. 이 기술을 통해 언젠가는 간, 신장, 심지어 심장까지 인간의 조직에서 자라는 것이 가능합니다.
제조공정
인테그럴 스킨 폼이란 무엇입니까? 일반적으로 셀프 스킨 폼이라고도 하는 일체형 스킨 폼은 재료의 발포 과정을 통해 형성된 이중층 구조입니다. 이 구성은 빵 한 덩어리와 유사하며 단단한 외부 크러스트로 둘러싸인 폼 내부 코어가 특징입니다. 또는 피부. 여러 재료를 사용하여 일체형 스킨 폼을 생성할 수 있지만 열경화성 폴리우레탄은 밀도, 경도, 인장 강도, 내화학성 등을 포함하여 정확한 설계 요구사항을 충족하기 위해 사용자 정의 가능한 특성을 제공할 수 있습니다. 적응성으로 인해, 폴리우레탄 일체형 스킨 폼은 캐스트 또는 RIM(Re
21세기에 몰입한 3D 바이오프린팅. 적층 제조를 통해 인체 조직을 인쇄한다는 것은 놀라운 아이디어입니다. 조직 재생 및 조직 공학 의학의 탁월한 단계라고 할 수 있습니다. 지난 수십 년 동안 이 기술은 인간 조직을 모방한 기능적 조직 구조를 만드는 데 사용되었습니다. 따라서 3D 바이오프린팅은 약물의 동물 및 인간 임상 시험과 관련된 긴 과정을 종료할 수 있습니다. 또한 조직 거부로 인해 실패하기 쉬운 장기 이식 중 장기 부족에 대한 솔루션이 될 수 있습니다. 이 돌파구는 전 세계적으로 장기 기증의 절박한 상태를 종식시