나노물질








다양한 대기 가스 분자(예:N2 , O2 , CO2 , H2 O, CO, 아니요, 아니요2 , NH3 및 SO2 )는 밀도 기능 이론 계산을 통해 깨끗한 육각형 비소붕소(BA)에 흡수됩니다. 각 가스 분자에 대해 다양한 흡착 위치가 고려되었습니다. 가장 안정적인 흡착은 위치, 흡착 에너지, 전하 이동 및 일 함수에 따라 다릅니다. SO2 기체 분자는 가장 좋은 흡착 에너지, 대기 기체 분자에서 BA 표면에 대한 최단 거리 및 일정량의 전하 이동을 가졌다. 일함수 계산은 전자 및 광학 특성을 조정할 가능성을 탐색하는 데 중요했습니다. 우리의 결과는 BA 재료가 SO2의 잠재적인 가스 센서가 될 수 있음을 제시했습니다. 높은 감도와 선택성으로.
BA(육방정계 붕소 비소)는 III족 및 V족 원소로 구성됩니다. III-V족 원소 그룹은 우수한 광전 특성, 기계적 특성 및 큰 밴드 갭과 같은 우수한 특성을 가지고 있습니다[1]. 2D 재료의 유망한 잠재적 응용 [2,3,4,5]은 최근 연구 [6,7,8,9,10,11,12,13,14,15,16,17,18,19 ,20]; 이러한 물질은 다양한 생체 분자[21, 22], 오염 물질[23, 24] 및 가스 분자[25, 26]를 인식하여 적절한 감지 장치를 개발하는 데 사용되었습니다. 우리는 BN, AlN, GaN, GaAs 및 BP와 같은 III-V 원소 재료의 그룹을 점점 더 많이 발견했으며 이론 계산에 의한 가스 분자에 대한 연구가 점점 더 많아지고 있습니다. Strak et al. [27]은 AlN(0001)이 고압-고온 암모니아 합성의 강력한 촉매임을 발견했으며, AlN(0001) 표면에서 암모니아의 효율적인 합성 가능성도 확인했다. Diao et al. [28] H2의 흡착 제시 오, CO2 , CO, H2 , 및 N2 깨끗하고 Zn 도핑된 GaAs 나노와이어의 (10-10) 표면; CO2 흡착 효과 및 N2 흡수계수에서 가장 컸다. Cheng et al. [29]는 첫 번째 원리 연구에서 순수한 BP와 도핑된 BP에 대한 대부분의 가스 분자 흡착을 보여주고 N-BP가 SO2에 대한 가스 센서로 더 적합하다고 결론지었습니다. , 아니요, 아니요2 탈착 과정이 있기 때문입니다. Kamaraj와 Venkatesan[30]은 DFT와 LDA에 의해 BA의 구조와 전자적 특성을 연구했습니다. BA의 실험적 합성과 이론적 연구에서 상당한 진전이 있었지만, BA 나노시트의 결과는 시스템에 나노전자공학 및 광전지의 유망한 응용을 부여했습니다.
이 작업에서 우리는 먼저 밀도 기능 이론(DFT) 계산에 의해 가스 센서로서의 BA의 가능성을 완전히 활용하기 위해 가스 감지 특성을 조사했습니다. 우리는 대기 가스(예:CO2 , O2 , N2 , H2 오, 아니오, 아니오2 , NH3 , CO 및 SO2 ) 첫 번째 원칙 계산을 기반으로 한 BA. 우리의 작업은 SO2의 명백한 흡착 거동, 적당한 전하 이동 및 고유한 전송 특성을 보여주었습니다. BA에 대한 흡착. 결과는 단층 BA가 SO2에 대한 큰 잠재력을 가지고 있음을 시사했습니다. 감지 응용 프로그램입니다.
이 시스템은 4 × 4 슈퍼셀 BA와 그 위에 흡착된 대기 가스 분자로 모델링되었습니다. DMol 3 에서 [31] 계산 과정에서 교환 상관 계수는 Perdew-Burke-Ernzerhof(PBE)를 사용하여 일반 기울기 근사(GGA) 내에서 계산되었습니다[32]. Brillouin 구역은 5 × 5 × 1 Monkhorst-Pack k-point grid와 0.01 Ry의 Methfessel-Paxton smearing을 사용하여 샘플링되었습니다. 전체 에너지와 Hellmann-Feynman 힘이 1.0 × 10 −5 으로 수렴될 때까지 모든 원자 구조가 완화되었습니다. eV 및 0.06 eV/Å[33].
기체 분자와 흡착 시트 표면 사이의 상호 작용을 평가하기 위해 흡착 에너지(E 광고 ) 다음과 같이 정의된 흡착 시스템의:
$$ {E}_{\mathrm{ad}}={E}_{\mathrm{BAs}+\mathrm{기체}\mathrm{분자}}-\left({E}_{\mathrm{BAs} }+{E}_{\mathrm{기체}\ \mathrm{분자}}\right) $$여기서 E BAs + 기체 분자 BAs 흡착 시스템의 총 에너지, E BA BA의 에너지, 그리고 E 기체 분자 기체 분자의 에너지이다. 모든 에너지는 최적화된 원자 구조에 대해 계산되었습니다. 전하 이동은 Mulliken의 인구 분석에 의해 조사되었습니다.
이 작업에서 BA에 대해 3개의 흡착 사이트, 즉 붕소 원자의 상단(B), 비소 원자의 상단(As) 및 그림 1a에 표시된 것처럼 육각형 B-As의 중심(중앙)이 고려되었습니다. . 우리는 대기의 존재를 연구했고 최고의 가스 센서를 찾았습니다.
<그림>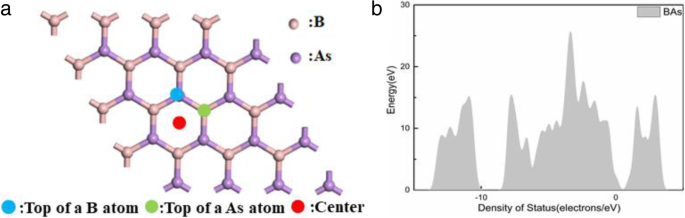
아 BA의 상위 사이트 및 센터 사이트의 개략도. ㄴ BA의 DOS
우선, 깨끗한 BAs 단층의 기하학적 구조가 최적화되었으며 그림 1b와 같이 BAs 결합 길이는 1.967 Å입니다. BAs sheet의 band 구조에서는 1.381 eV의 간접 band gap이 나타나 bulk 구조보다 작은 band 구조를 보였다. 이 값은 이전에 보고된 값과 잘 일치했습니다(그림 2)[34, 35].
<그림>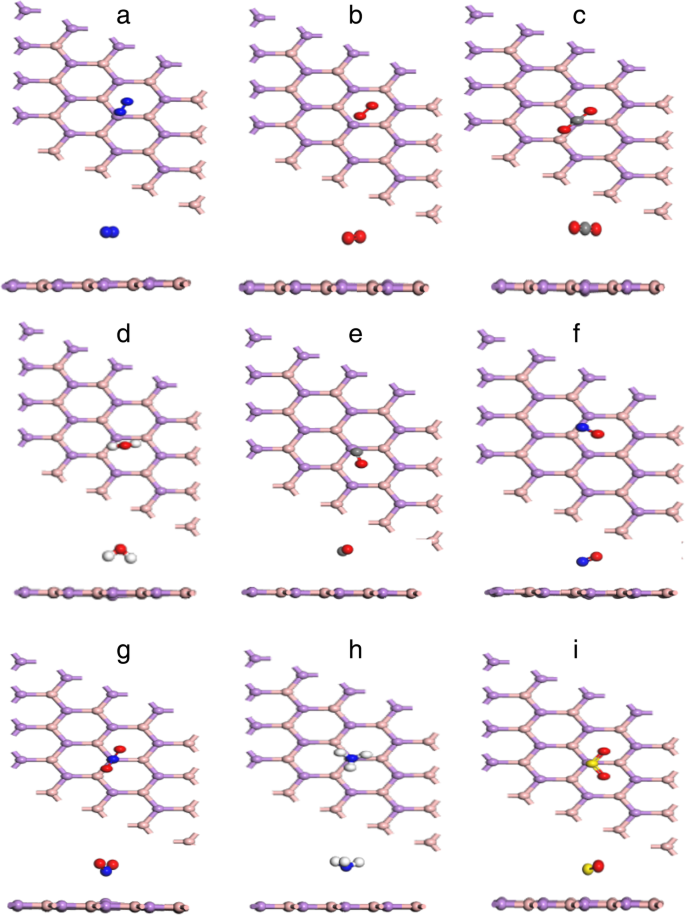
기체 분자의 가장 에너지적으로 유리한 흡착 구성:N2 (아 ), O2 (b ), CO2 (ㄷ ), H2 오(d ), CO(e ), 아니요(f ), 아니요2 (지 ), NH3 (h ) 및 SO2 (나 ) 단층 BA에
한편, 흡착 에너지, 전하 이동 및 분자와 BA 표면 사이의 거리를 분석했습니다. 최종 결과는 표 1과 같았습니다.
아니 2 흡착: N2의 흡착 BA의 가스 분자는 N2의 세 가지 구성에 대해 연구되었습니다. /BA, 즉. B 원자의 윗면, As 원자의 윗면, BAs 표면 위의 육각형 고리의 중심, 가장 가까운 거리는 3.764 Å, 3.549 Å, 3.65 Å이고 해당 흡착 에너지는 - 0.24 eV, - 0.27 eV 및 - 0.24 eV 각각. 센터는 가장 좋은 흡착 에너지와 가장 안정적인 구조를 가졌다. N2의 흡착 에너지 BA는 -0.24 eV, BA에서 N 2 으로의 전하 이동 기체 분자는 0.014e였고, N2-BA의 거리는 3.65Å였다. 그림 3a는 페르미 에너지 준위 아래에 많은 선이 있고 해당하는 상태 밀도가 페르미 에너지 준위 아래에서 여러 피크가 있음을 보여줍니다. 그림과 같이 N2 기체 분자는 4개의 피크를 가지며, 주로 - 5에서 0 eV까지 BA에 특정 영향을 미치고 DOS에 큰 기여를 했습니다. 전반적으로 N2의 효과 BA에 대한 가스 분자 흡착이 좋지 않았습니다.
<그림>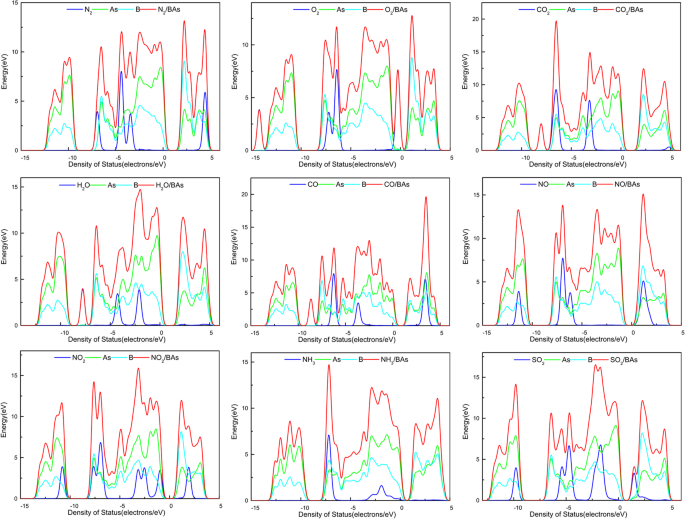
N2의 상태 밀도(DOS) /BA(a ), O2 /BA(b ), CO2 /BA(c ), H2 O/BA(d ), CO/BA(e ), NO/BA(f ), 아니요2 /BA(g ), NH3 /BA(h ) 및 SO2 /BA(i )
오 2 흡착: O2 기체 분자는 중심점에 흡착하는 경향이 있습니다. O2의 흡착 에너지 /BAs는 - 0.35 eV이고 O2의 거리는 -BA는 2.90 Å이었다. O2에 대한 전체 밴드 구조 및 DOS /BA는 그림 3에 표시되어 있습니다. 추가 선이 영점을 가로질러 밴드 갭을 줄인 것이 분명했습니다. O2 기체 분자는 - 1 ~ 0 eV에서 피크를 가지며 페르미 준위 이상의 상태 밀도에 영향을 미쳤습니다. Mulliken 전하 이동에 대한 모집단 분석은 - 0.172e가 BA 표면에서 O2로 이동되었음을 보여주었습니다. O2 기체 분자가 수용체로 작용했습니다. 일반적으로 O2 BA에 대한 가스 분자 흡착은 N2보다 우수했습니다. .
CO 2 흡착: CO2 기체 분자는 As 원자의 상단에 흡착되는 경향이 있습니다. CO 2 의 흡착 에너지 /BAs는 -0.28 eV, BA에서 CO로 전하 이동 2 기체 분자는 -0.018e이고 CO 2 의 거리는 -BA는 3.55Å였습니다. 그림 3에서 볼 수 있듯이, 순수한 BA와 비교하여 구조는 뚜렷한 변화가 없었고, DOS에서 - 9 eV의 에너지의 명백한 파동이 있었고, 이는 DOS에 큰 기여를 했습니다. 이 점은 또한 CO2의 흡착을 강조했습니다. BA에 의한 기체 분자. 결과는 CO2에 대한 BA의 흡착 효과 및 감도를 보여주었습니다. 기체 분자는 일반적이었습니다.
안 2 O 흡착: H2 O 가스 분자는 As 원자의 상단에 흡착되는 경향이 있습니다. H 2 의 흡착 에너지 O/BA는 − 0.38 eV, BA에서 H 2 로의 전하 이동 O 기체 분자는 -0.03e이고 H 2 의 거리는 O-BA는 3.63Å이었습니다. 그림 3에서 볼 수 있듯이 원시 BA에 비해 구조에는 큰 변화가 없었습니다. Al-G의 페르미 준위는 분명히 증가하여 가전자대로 이동했습니다. 일반적으로 H2 BA에 대한 O 가스 분자 흡착은 무시되었습니다.
CO 흡착: CO 가스 분자는 As 원자의 상단에 흡착되는 경향이 있습니다. CO/BA의 흡착 에너지는 -0.27 eV, BA에서 CO 기체 분자로의 전하 이동은 -0.024e, CO-BA의 거리는 3.50 Å이었다. BAs-CO의 총 상태 밀도(DOS)와 밴드 구조는 그림 3에 표시되어 있습니다. CO 가스 분자와 As 원자는 DOS에서 3~4 eV의 피크 효과에 큰 역할을 했습니다. 그러나 - 7 ~ 4 eV 범위에서 DOS에 편차가 없었으며, 이는 CO가 매주 BA에 흡착되었음을 시사합니다. - 3 ~ 1 eV 및 3 eV의 에너지의 명백한 파동 마루가 있었는데, 이는 DOS에 큰 기여를 했습니다. Mulliken 전하 이동에 대한 모집단 분석은 - 0.024e 전하가 BAs 표면에서 CO 가스 분자로 이동되었음을 보여주었으며, CO 가스 분자가 수용체로 작용함을 시사했습니다. 전반적으로 BA에 대한 CO 가스 분자 흡착 효과는 특별하지 않았습니다.
흡착 없음: NO 기체 분자는 B 원자의 상단에 흡착되는 경향이 있습니다. NO/BAs의 흡착 에너지는 - 0.18 eV, 전하 이동은 NO 가스 분자에서 BAs로 - 0.01e, NO-BAs의 거리는 2.86 Å이었다. 페르미 에너지 준위에는 많은 선이 있었습니다. 중간 밴드의 에너지 갭이 밴드 갭 값을 감소시키는 것을 발견했습니다. 상태 밀도 다이어그램에서 페르미 에너지 준위보다 높은 추가 파동 피크가 있었지만 페르미 에너지 준위 아래에서는 거의 변화가 없었으며 그림 3에서 비교적 안정적이었습니다. 오비탈의 혼합은 상호 작용에 대한 작은 전하 이동 및 재분배를 일으켰습니다. 지역. Mulliken 전하 이동에 대한 모집단 분석은 0.01 전하가 BA 표면에서 NO 분자로 이동되었음을 보여주었으며, 이는 NO가 공여체로 작용했음을 시사합니다. - 7 ~ 4 eV 범위에서 DOS에 편차가 없었으며, 이는 NO가 매주 BA에 흡착되었음을 시사합니다.
아니요 2 흡착: 아니요2 기체 분자는 As 원자의 상단에 흡착되는 경향이 있습니다. NO2의 흡착 에너지 /BAs는 - 0.43 eV이고 NO2의 거리는 -BA는 2.47 Å이었다. 흥미로운 점은 밴드의 영점이 NO2 흡착 직후 직선을 교차했다는 것입니다. 반도체인 BA가 금 속성으로 변환되었음을 의미하는 가스 분자; 밴드 갭은 0 eV였다. 전체적으로 큰 변화는 없었고 NO2로 인해 약 - 3 eV에서 피크가 발생하였다. 기체 분자 흡착. - 7 eV 및 2 eV의 에너지에 대한 일부 명백한 파동 마루가 있었는데, 이는 DOS에 큰 기여를 했습니다. 일반적으로 NO2의 흡착 BA에 의한 것은 위의 여러 분자의 것보다 우수했습니다.
NH 3 흡착: NH3 기체 분자는 As 원자의 상단에 흡착되는 경향이 있습니다. NH 3 의 흡착 에너지 / BA는 -0.34 eV, NH 3 에서 전하 이동 BA에 대한 기체 분자는 0.007e이고 NH 3 의 거리는 -BA는 3.27Å이었다. NH3 흡착 피크가 있는 것을 제외하고 에너지 밴드와 상태 밀도에는 뚜렷한 변화가 없었습니다. 페르미 준위 아래의 기체 분자. NH3 기체 분자는 - 8 ~ - 4 eV에서 BA에 약간의 영향을 주어 15 eV 피크를 형성했습니다. NH3에 대한 BA의 흡착 효과 및 감도 기체 분자는 일반적이었습니다.
SO 2 흡착: SO2 기체 분자는 SO2의 흡착 에너지인 중심점에 흡착하는 경향이 있습니다. /BAs는 - 0.92 eV이고 Mulliken 전하 이동에 대한 모집단 분석은 - 0.179e 전하가 BAs 표면에서 SO2로 이동되었음을 보여주었습니다. SO2 기체 분자는 수용체로 작용합니다. SO2의 거리 /BAs는 2.46 Å이었다. 다른 기체 분자에 비해 SO2 /BA는 가장 큰 흡착 에너지, 두 번째로 큰 전자 이동 및 SO2의 가장 짧은 거리를 가졌습니다. - 학사. 그림 3에서 보는 바와 같이 BA의 valence band는 뚜렷한 up과 band gap이 감소하였고 흡착된 SO2로 인해 기체 분자의 상태 밀도에서 - 7.5 eV에서 파동 피크가 하나 더 있고 페르미 준위에서 특정 전달이 있음을 알 수 있습니다. SO2의 흡착 BA에 의한 탁월한 효과가 있었습니다.
그림 4i는 SO2의 전자 밀도 다이어그램을 보여줍니다. /BA 및 BA와 SO 사이의 전자 로컬 겹침2 기체 분자. 이를 바탕으로 SO2의 흡착이 BA에 의한 물리적 흡착이었다. 그림 5에 표시된 WF의 계산은 작은 분자를 흡착하여 전자 및 광학 특성(예:흡수 스펙트럼 및 에너지 손실 함수)을 조절할 가능성을 탐색하는 데 큰 의미가 있습니다. 일 함수는 고체 물리학에서 전자를 고체 내부에서 물체 표면으로 이동시키는 데 필요한 최소 에너지로 정의되었습니다. 원시 BA의 일함수는 4.84 eV였습니다. 아니요 및 NH3 기체 분자는 전하 이동에서 공여체였으며 일 함수가 감소했습니다. 일함수는 각각 4.80 eV와 4.68 eV였다. N2의 일함수 /BA, CO2 /BA 및 CO/BA는 BA와 동일했습니다. O2의 일함수 /BA, NO2 /BA 및 SO2 /BAs는 BAs보다 높았습니다. 위의 흡착 에너지, 기체 분자와 BA 표면의 거리, 전하 이동 및 일함수와 결합하여 SO2 기체 분자는 BA 재료에 가장 적합했습니다.
<그림>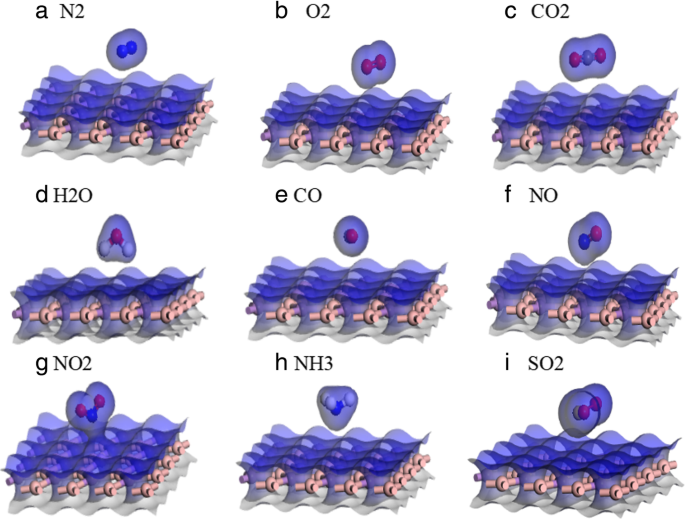
깨끗한 N2의 전자 밀도 /BA(a ), O2 /BA(b ), CO2 /BA(c ), H2 O/BA(d ), CO/BA(e ), NO/BA(f ), 아니요2 /BA(g ), NH3 /BA(h ) 및 SO2 /BA(i )
<그림>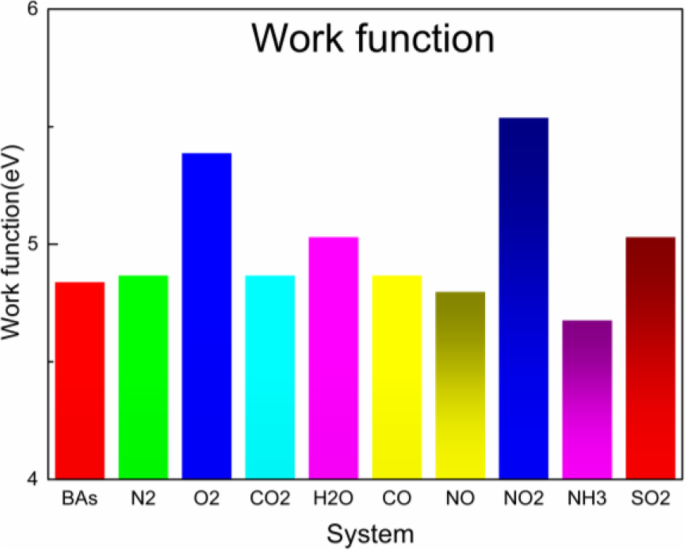
BA N2의 일함수 /BA, O2 /BA, CO2 /BA, H2 O/BA, CO/BA, NO/BA, NO2 /BA, NH3 /BA 및 SO2 /BA
우리는 N2 흡착제를 사용한 BA의 구조적 및 전자적 특성을 제시했습니다. , O2 , CO2 , H2 O, CO, 아니요, 아니요2 , NH3 및 SO2 밀도 함수 이론 방법을 사용하여 기체 분자. 흡착 에너지에서 SO2> 아니요2> H2 O> O2> NH3> CO2> CO> N2> NO 및 SO2 <아니요2
육각형 붕소 비소
상태 밀도
작업 기능
나노물질
MIG 용접은 용접 부위에 가스 흐름을 전달하는 가스 노즐과 함께 스풀 공급 와이어 전극이 포함된 휴대용 건을 사용합니다. 이 가스는 산소, 질소 및 기타 환경 가스가 용접 비드와 접촉하는 것을 방지하여 일관되고 강력한 결과를 보장합니다. 오염은 공작물의 용접 품질을 저하시킬 수 있으므로 최상의 결과를 얻으려면 올바른 가스를 선택하는 것이 절대적으로 중요합니다. 그러나 MIG 용접에 가장 적합한 가스는 무엇입니까? 불행히도 답은 그렇게 간단하지 않습니다. 대부분의 경우 75/25 아르곤과 CO2 혼합물을 사용하면 대부분의 금속에
사용 가능한 포지셔너 기능 및 옵션을 이해하면 의사 결정 프로세스를 용이하게 하여 품질을 추가로 개선하고 주기 시간을 단축하며 용접 라인에서 우수성을 제공할 수 있습니다. 여기서는 제조업체가 사용할 수 있는 모든 옵션과 기능을 더 잘 이해하는 데 도움이 되는 중요한 포지셔너 정보에 대해 논의합니다. 포지셔너란 무엇인가요? 포지셔너는 360도 회전이 가능하며 회전 및 회전 장치를 통해 부품에 접근할 수 있습니다. 포지셔너를 사용하면 생산을 가속화하고 용접 품질을 향상시킬 수 있습니다. 로봇 작업 셀을 설계할 때 로봇이 작업할