나노기술의 최근 기술 발전은 100nm보다 작은 입자인 공학 나노입자(ENP)의 개발을 가속화했습니다. ENP는 초소형 또는 대형 물질에 비해 조직 침투력 및 표면 반응이 좋아 화장품, 식품, 의약품 등 다양한 제품에 널리 사용되고 있다[1,2,3]. 예를 들어, ENP의 가장 일반적인 유형 중 하나인 은 나노 입자(nAgs)는 은 이온(Ag
+
)의 꾸준한 방출로 인한 항균 특성 때문에 화장품에 포함됩니다. ) [4, 5]. 그러나 nAgs의 작은 입자 크기와 관련된 독특한 물리화학적 특성은 위험할 수 있습니다. 이러한 입자는 혈뇌장벽과 같은 뚫을 수 없는 장벽을 파괴하고 염증을 유발할 수 있는 것으로 알려져 있습니다[6]. 또한 일부 연구에서는 ENP가 피부 장벽을 관통할 수 있다고 보고했습니다[7,8,9]. 따라서 이러한 입자의 지속적인 사용에 대한 안전성을 결정하려면 피부와 같은 조직 내에서 이러한 입자의 역학을 조사하여 nAgs를 함유한 ENP와 관련된 독성 영향을 이해하는 것이 중요합니다.
안전을 보장하기 위해 "위험"(잠재적 독성) 및 "노출 조건"의 통합 개념을 포함하는 ENP 사용과 관련된 가능한 위험을 이해하는 것이 필수적입니다. ENP의 위험성은 전 세계적으로 분석되어 왔지만 ENP 노출과 관련된 조건을 조사한 연구는 소수에 불과합니다[10]. 특히, nAgs 및 Ag
+
신체 내에서 물리적 특성을 변경할 수 있습니다. 예를 들어, nAgs의 이온화는 입자 크기가 더 작은 nAgs를 형성하고 Ag
+
를 방출합니다. [11]. 반대로 초산은을 경구 투여한 쥐의 장 상피에서는 입자 크기가 작은 nAg가 검출될 수 있다[12]. 또한, 우리는 최근에 더 작은 nAgs 및 Ag
+
에 비해 , 더 큰 nAgs는 nAgs에 노출된 수유 중인 마우스의 모유에서 더 쉽게 발견됩니다[13]. 따라서 nAgs는 신체의 물리적 특성을 변화시킬 수 있으며, 이는 결국 동역학의 변화로 이어집니다. 따라서 관련된 위험을 이해하려면 이러한 입자의 입자 크기와 같은 물리적 특성을 평가하고 이러한 입자와 체내 이온을 구별하는 것이 필요합니다.
이와 관련하여 우리는 체류 시간당 최대 하나의 입자를 분석기에 도입하는 단일 입자 유도 결합 플라즈마 질량 분석법(sp-ICP-MS)을 적용했습니다. 피크 속도를 통해 피크 강도와 입자 농도를 분석하여 입자 크기를 결정하는 데 사용할 수 있는 효과적인 방법입니다. 입자와 이온은 피크 신호와 배경 신호를 모두 분석하여 구별할 수 있습니다[14]. 우리는 이전에 생물학적 시료에서 sp-ICP-MS의 전처리 방법을 최적화하여 간, 심장, 폐, 신장 및 비장과 같은 다양한 기관에서 ENP의 물리적 특성을 반정량적으로 결정했습니다[15].
피부는 각질층(SC)을 포함한 표피와 혈관, 림프관 및 신경을 포함하는 진피로 구성됩니다[16]. 따라서 ENP가 각 피부층으로 유입되면 다양한 정도로 독성을 유발할 수 있습니다. 예를 들어, 표피의 인간 피부 각질형성세포에서 이산화티타늄 나노입자의 분포는 활성 산소 종의 생성을 자극할 수 있습니다[17]. 더욱이 털이 없는 생쥐에서 이산화티타늄 나노입자에 60일 동안 피부에 노출되면 국소 독성으로 인해 진피가 얇아지는 등의 병리학적 변화는 물론 전신 독성으로 인한 액화 괴사 등 간의 병리학적 변화도 나타났다. 진피의 혈관을 통해 퍼집니다[18]. 또한, 각 층의 생물학적 반응은 입자 크기와 같은 물리적 특성, 입자와 이온의 차이에 따라 달라질 수 있다[19]. nAgs 사용의 안전성을 이해하기 위해서는 nAgs가 피부에 노출된 후의 물리적 특성과 생체 분포에 대한 이해가 필요합니다.
이러한 특정 문제를 해결하기 위해서는 ENP의 물리적 특성 변화나 회복 중 손실이 발생하지 않으면서 피부를 전처리하고 피부층을 분리할 수 있는 접근 방식이 필요하다. 그러나 이러한 피부에 대한 최적의 접근 방식은 아직 고안되지 않았습니다.
본 연구에서는 sp-ICP-MS를 통해 피부의 각 층에서 모델 ENP인 nAgs의 물리적 특성을 반정량적으로 결정하는 전처리 접근 방식을 최적화하고 후속적으로 생체 내에서 그 효과를 평가했습니다.
방법
쥐
Slc:ICR 마우스(암컷, 8주령)는 Japan SLC(Shizuoka, Japan)에서 구입했습니다. 마우스는 다음과 같은 명암 주기로 방에 수용되었습니다:오전 8시에 조명을 켜고 오후 8시에 소등했습니다. 음식과 물은 음식 알약 형태로 제공되었으며 케이지 상단에 물 공급 시스템이 있습니다. 모든 실험 프로토콜은 일본 오사카 대학의 동물 연구 위원회에서 승인한 조건에서 수행되었습니다.
nAg 및 Ag
+
직경 100 nm(nAg100)의 시트레이트 리간드로 덮인 nAg 현탁액은 nanoComposix(San Diego, CA, USA)에서 스톡 분산액(1 mg/mL)의 형태로 구입했습니다. 질산은(AgNO3 )는 또한 스톡 분산액(1 mg/mL)의 형태로 Wako Pure Chemical Industries(Osaka, Japan)에서 구입했습니다. 운송 효율을 계산하기 위한 표준으로 사용되는 RM8013은 National Institute of Standards and Technology(Gaithersburg, MD, USA)에서 구입했습니다. 각 유형의 나노 입자는 사용하기 전에 10분 동안 초음파 처리되었습니다. 나노입자와 이온도 사용하기 전에 10초 동안 와동시켰습니다.
시약
수산화나트륨(NaOH, 0.1mol/L)은 Nacalai Tesque Company(일본 오사카)에서 구입했으며 질산(HNO3 , 70%)는 Kanto Kagaku Chemical Industries(일본 도쿄)에서 구입했습니다. 인산완충식염수(PBS), pH 7이 준비되었습니다.
전처리 방법 최적화
각 마우스의 표피와 진피를 분리하고 PBS(w/v 1:10의 비율), 균질화. 균질물을 100ng/mL nAg100 용액과 혼합했습니다. 그런 다음 혼합물을 v/v에서 다음 시약 중 하나로 처리했습니다. 1:1의 비율; 0.1 mol/L NaOH, 70% HNO3 , 또는 PBS. 샘플을 37°C에서 3시간 동안 배양하고 sp-ICP-MS에 적용했습니다.
마이크로파 조사를 통한 피부 분리
각 마우스를 isoflurane(Wako)으로 안락사시킨 후 2cm
2
(2 cm × 1 cm) 등 피부 샘플을 수술용 가위와 핀셋을 사용하여 절제했습니다. 절제 절차 중 조직 손상을 방지하기 위해 특별한 주의를 기울였습니다. 전자레인지(RE-SW-20-H, Sharp, Japan)를 사용하여 2450MHz의 주파수로 피부를 조사하였다. 피부 샘플을 접시에 놓고 전자 레인지 중앙에 넣었습니다. 테스트 요구 사항에 따라 피부 샘플에 각각 200, 600 및 900W에서 10초, 30초 및 60초 동안 조사했습니다. 조사 후 샘플을 신속하게 제거하고 외과용 핀셋으로 부드럽게 긁어 각 표피와 진피를 신속하게 분리했습니다. 100ng/mL nAg100 용액을 조사(200W, 30초) 후 nAg의 회수율 및 평균 직경의 분석에 사용했습니다.
nAg100 및 Ag의 경피 투여
+
9주된 암컷 Slc:ICR 마우스를 체중에 따라 그룹당 3마리씩 6개 그룹으로 나누었습니다. 이소플루란을 사용하여 마우스를 마취시켰다. 등의 털은 이발기(Panasonic®, Osaka, Japan)와 핸드 면도기(Gillette®, Germany)로 면도하였다. 다음으로 nAg100 및 Ag
+
(20μg/cm
2
) 2.25cm
2
의 표면적에 직접 도포되었습니다. (1.5 cm × 1.5 cm) 등쪽 피부를 비흡수성 플라스틱 필름으로 단단히 덮습니다. 플라스틱 필름 위에 같은 크기의 거즈 조각을 올려 놓았습니다. 자체 접착식 탄력 붕대로 피부를 감싸 거즈를 덮고 피부를 5일 동안 덮었습니다.
피부 샘플 및 혈액의 전처리
치료 5일 후, 안와후정맥총과 등쪽 피부에서 말초혈액을 채취하여 분석하였다. 다음 2.25cm
2
(1.5 cm × 1.5 cm) 등 피부 샘플을 수술용 가위와 핀셋을 사용하여 절제했습니다. 절제하는 동안 조직 손상을 방지하기 위해 특별한 주의를 기울였습니다. SC 층은 진피에서 표피를 분리하기 전에 접착 테이프(Scotch®, 3M)의 2cm 조각을 사용하여 순차적으로 제거되었습니다. 등쪽 피부의 치료 부위에 테이프 조각을 누른 후 10초 동안 일정한 압력을 가했습니다. 각 마우스의 전체 SC를 제거하려면 20개의 테이프 조각이 필요했습니다. 다음으로, 마이크로파 조사로 진피와 표피를 분리하고 PBS(w/v 1:10의 비율). 수집된 혈액과 진피 및 표피 균질물을 v/v에서 0.1 mol/L NaOH로 처리했습니다. 1:1의 비율로 37°C에서 3시간 동안 별도로 배양했습니다. 배양 후, 혈액, 표피 및 진피 혼합물의 총 은 질량을 유도 결합 플라즈마 질량 분석기(ICP-MS)로 분석했습니다. nAgs 및 Ag
+
의 물리적 특성의 정량화 및 평가 sp-ICP-MS를 사용하여 수행되었습니다.
은의 총 질량 측정
혈액, SC, 표피 및 진피 샘플의 총 은 농도를 측정하기 위해 Agilent 7700x ICP-MS 시스템(Agilent Technologies, Santa Clara, CA, USA)을 사용했습니다. 분석이 수행된 조건은 다음과 같습니다. RF 전력 1550W; 캐리어 가스 1.05L/min Ar; 및 체류 시간 100ms. 측정은 MS 모드에서 세 번 반복되었습니다. 로듐은 Ag의 내부 표준으로 사용되었습니다. ICP-MS 분석의 대상 요소는
103
이었습니다. Rh 및
107
Ag. Ag 및 로듐 표준 용액은 Wako에서 얻었습니다.
sp-ICP-MS 분석 및 계산
Agilent 7700x ICP-MS(Agilent Technologies)를 sp-ICP-MS 분석에 사용했습니다. 분석 조건은 다음과 같았다:RF 전력 1550W; 캐리어 가스 1.05L/min Ar; 체류 시간 10ms; 및 분석 시간 30초. Wagenen Food Safety Research(Wageningen University, Wageningen, Netherlands)에서 발행한 단일 입자 계산 도구인 RIKILT를 사용하여 입자 크기를 계산했습니다[20].
통계 분석
모든 통계 분석은 Macintosh용 GraphPad Prism 소프트웨어 버전 5.0(GraphPad Software, La Jolla, CA, USA)을 사용하여 수행되었습니다. 통계적 유의성은 P로 설정되었습니다. <0.05.
결과 및 토론
각 피부층에서 nAgs의 양과 물리적 특성을 결정하는 방법을 구성하기 위한 전략
각 피부층에서 nAg의 양과 물성을 결정하기 위해서는 피부 시료를 완전히 가용화하고 sp-ICP-MS 분석에 적합한 시료를 준비해야 합니다. 또한 경피적으로 흡수되지 않은 nAg는 테이프 스트리핑을 통해 SC를 제거하는 동안 제거될 수 있기 때문에 회복 중 손실이나 nAg의 물리적 특성 변화 없이 표피와 진피를 분리하는 것이 필수적입니다[21].
피부 시료의 가용화와 관련하여 우리는 이전에 NaOH 전처리가 간, 심장, 폐, 신장, 비장[16]. 따라서 본 연구에 사용된 피부 샘플에는 NaOH 전처리를 적용하였다.
콜라겐 섬유를 연화시키고 표피-진피 접합부(EDJ)에서 분리를 촉진하는 효소 소화를 강화하는 열수 치료는 피부를 표피층과 진피층으로 분리하는 데 널리 사용됩니다[22]. 이러한 치료는 피부층을 효율적으로 분리하지만, 층의 nAg는 수용액에서 이온화되어 물리적 특성에 변화를 일으킬 수 있습니다. 마이크로파 조사의 짧은 펄스는 EDJ를 방해하는 열 발생을 통해 피부가 표피층과 진피층으로 분리되도록 하는 것으로 보고된다[23, 24]. 따라서 단시간 동안 용액에 배양하지 않고 마이크로파 조사를 적용했습니다.
종합적으로, 우리는 각 피부층에서 nAg의 회복율과 물성 변화를 분석하여 검증된 전략(그림 1 참조)을 제안했습니다.
<그림><그림><소스 유형="이미지/webp" srcset="//media.springerature.com/lw685/springer-static/image/art%3A10.1186%2Fs11671-020-03421-x/MediaObjects/ 11671_2020_3421_Fig1_HTML.png?as=webp"> 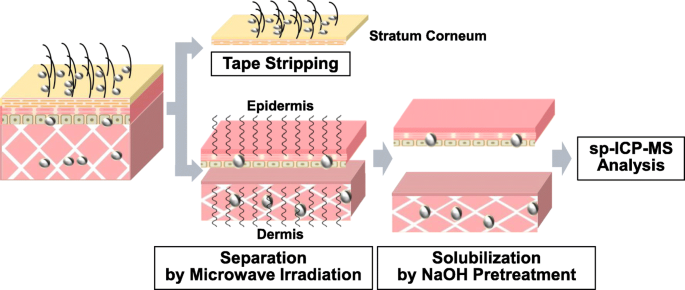
피부 조직의 각 층에서 nAg100의 양과 물리적 특성을 결정하기 위한 전략. 피부 조직의 각 층에서 nAg100의 양과 물리적 특성을 결정하기 위해서는 (1) 피부 조직을 완전히 가용화하고 (2) 회복 중 조직 손실 또는 변화 없이 피부를 표피 및 진피 조직으로 분리해야 합니다. nAg100의 물리적 특성. 이와 관련하여 (1) NaOH 전처리 및 (2) 마이크로파 조사
에 중점을 두었습니다. 표피 및 진피에서 nAg100 검출을 위한 전처리 방법 최적화
우리는 피부 샘플을 가용화하기 위한 전처리 방법을 최적화하기 위해 이전 연구를 참조했습니다. Ishizaka et al. [15]는 NaOH 및 HNO3와 같은 다양한 종류의 가용화 시약 중에서, NaOH 전처리가 최적이었습니다. 따라서 HNO3를 테스트했습니다. 산성 및 알칼리성 가용화 시약으로서 각각 NaOH. 마우스 피부 시료에서 분리한 표피와 진피 균질물을 nAg100과 혼합하여 최종 Ag 농도가 100ng/mL이 되도록 하고 각 가용화 시약으로 37℃에서 처리하였다. 먼저 이러한 시약으로 처리한 후 Ag의 회수율을 평가했습니다. ICP-MS 분석은 거의 100% 회수율이 NaOH 및 HNO3에 의해 달성되었음을 나타냅니다. 치료만(그림 2a). 다음으로 각 처리에 따른 물성의 변화를 평가하기 위해 각 입자와 이온의 회수 농도를 분석하였다. sp-ICP-MS 분석은 nAg100이 HNO3에 의해 거의 완전히 이온화되었음을 나타냅니다. . 이것은 HNO3, 산성 시약으로 입자를 용해시키고 이온으로 전환시키는 것으로 이전 연구에서도 보고된 바 있다[15]. 대조적으로, NaOH로 처리된 nAg100의 대부분은 이온이 아닌 입자로 남아 있었다(그림 2b). 따라서, NaOH는 대부분의 nAg100이 입자 형태로 남아 있도록 했습니다. 마지막으로 물리적 특성을 자세히 분석하기 위해 입경 분포를 평가하였다. HNO3 처리는 nAg100의 이온화에 해당하는 평균 입자 직경을 100nm에서 40nm로 변경했습니다. 반대로 NaOH 처리 후 평균 입경은 약 100 nm로 초기 입경에 해당하였다(Fig. 2c). 이것은 NaOH 전처리가 마우스 피부에서 nAg100을 검출하는 데 최적임을 시사했습니다.
<그림><그림><소스 유형="이미지/webp" srcset="//media.springerature.com/lw685/springer-static/image/art%3A10.1186%2Fs11671-020-03421-x/MediaObjects/ 11671_2020_3421_Fig2_HTML.png?as=webp"> 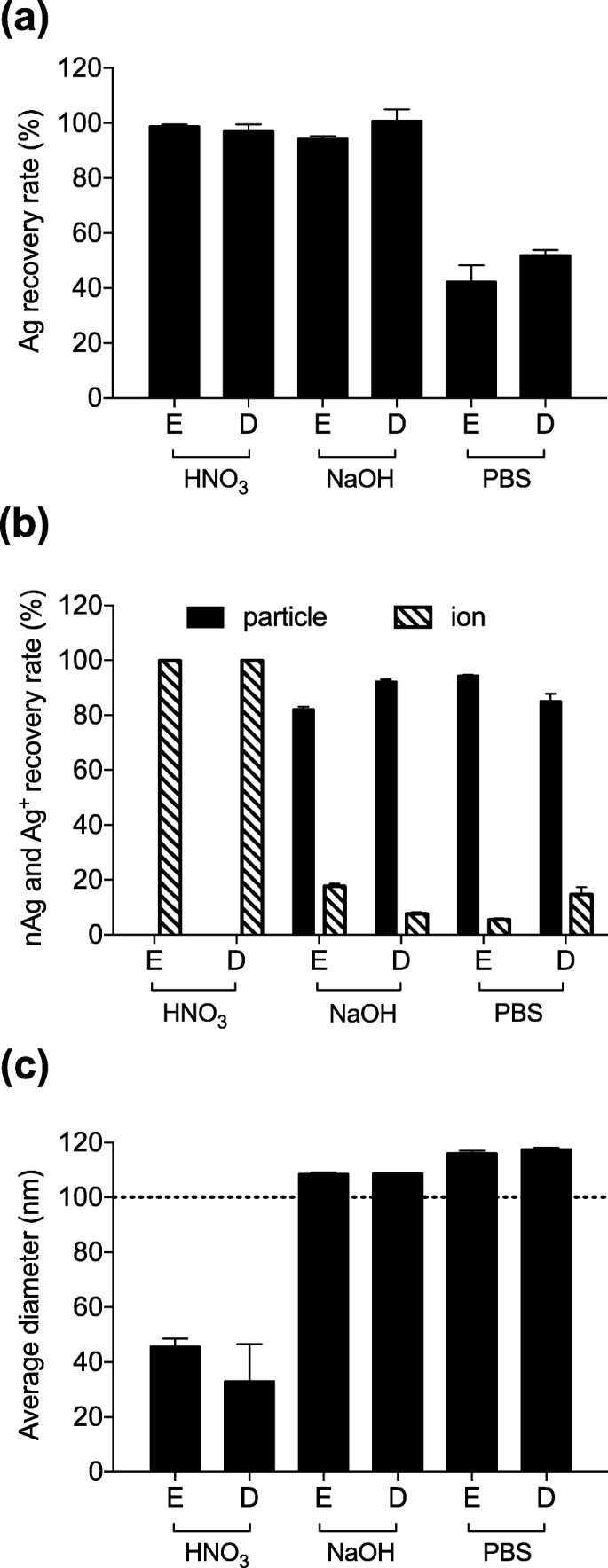
NaOH 전처리는 진피와 표피에서 nAg100을 검출하는 최적의 방법입니다. 2개의 가용화 시약(HNO3 및 NaOH)를 조직을 용해하기 위한 전처리 용매로 스크리닝하였다. 표피(E)와 진피(D) 균질물을 nAg100과 혼합하여 최종 Ag 농도가 100ng/mL이 되도록 하고 37°C에서 각 가용화 시약으로 처리했습니다. 3시간 후, 모든 샘플을 ICP-MS 및 sp-ICP-MS를 통해 분석했습니다. 아 Ag의 회수율, b nAg(검은색 막대) 및 Ag
+
(음영 처리된 막대) 복구율 및 c 평균 입자 직경이 표시됩니다. 점선은 초기 입자 크기를 나타냅니다. 데이터는 평균 ± SD로 표시되었습니다. (n =3)
마이크로파 조사를 통한 피부 시료의 표피와 진피 분리 및 nAgs의 회복률 및 물리적 특성 변화 평가
피부 샘플을 표피층과 진피층으로 분리하기 위해 우리 연구와 관련이 있고 이전에 성공적으로 보고된 다양한 조건의 마이크로파 조사를 적용하고 [24] 피부 분리성 및 피부의 변화에 대한 성능을 비교했습니다. 물리적 특성. 200W 10초, 600W 30초, 600W 60초, 950W 30초, 950W 60초 조건에서 피부가 표피층과 진피층으로 분리되지 않는 현상이 관찰되었다. 그림 3a). 또한 200W 60초, 600W 10초, 950W 10초 조건하에서 피부는 표피층과 진피층으로 부분적으로만 분리되었다. 대조적으로, 피부는 200W에서 30초 동안 조사한 후에야 표피층과 진피층으로 완전히 분리되었다. 이러한 결과는 200W에서 30초 동안 조사하는 것이 피부층 분리에 최적임을 나타냅니다.
<그림><그림><소스 유형="이미지/webp" srcset="//media.springerature.com/lw685/springer-static/image/art%3A10.1186%2Fs11671-020-03421-x/MediaObjects/ 11671_2020_3421_Fig3_HTML.png?as=webp"> 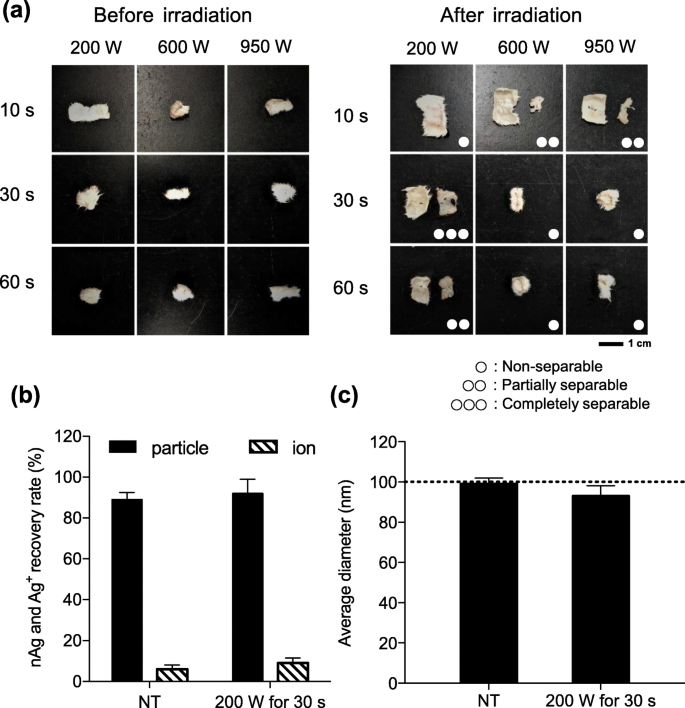
마이크로파 조사에 의해 피부가 표피와 진피로 분리되는 조건의 스크리닝 및 평가. 아 피부 조직에 9가지 조건에서 마이크로파를 조사하여 표피 조직과 진피 조직으로 분리하였다. 왼쪽과 오른쪽 패널은 각각 조사 전과 후의 피부 샘플을 보여줍니다. 오른쪽 패널에서 단일, 이중 및 삼중 흰색 원은 각각 분리 불가, 부분 분리 및 완전히 분리 가능한 조건을 나타냅니다. 눈금 막대:1cm. 피부 균질액을 nAg100과 혼합하여 최종 Ag 농도가 100ng/mL이 되도록 하고 200W에서 30초 동안 조사하고 sp-ICP-MS를 통해 분석했습니다. ㄴ nAg(검은색 막대) 및 Ag
+
(음영 처리된 막대) 복구율 및 c 평균 입자 직경이 표시됩니다. 점선은 초기 입자 크기를 나타냅니다. 데이터는 평균 ± SD로 표시되었습니다. (n =3)
200W에서 30초 동안 마이크로파 조사가 nAg100의 물리적 특성에 영향을 미치는지 확인하기 위해 표피 및 진피층에서 Ag의 물리적 특성을 결정했습니다. 표피 및 진피 균질물을 각각 100ng/mL의 nAg100과 혼합하여 NaOH를 사용하여 용해시키고 200W에서 30초 동안 조사하였다. Sp-ICP-MS 분석은 마이크로파 조사로 처리된 nAg100의 대부분이 입자로 남아 있었고, 처리하지 않은 그룹에서도 마찬가지임을 보여주었다(그림 3b). 물리적 특성을 자세히 분석하기 위해 입자 직경 분포도 평가했습니다. 평균 입자의 직경은 거의 100 nm였으며 이는 초기 입자 크기에 해당합니다(그림 3c). 이러한 발견은 200W에서 30초 동안 피부 샘플의 마이크로파 조사가 nAg100의 물리적 특성을 변경하지 않고 피부를 표피와 진피층으로 효율적으로 분리하는 유망한 접근법임을 시사합니다.
종합적으로, 이러한 결과는 각 피부층에서 nAg100의 물리적 특성을 반정량적으로 결정하는 시스템을 성공적으로 개발했음을 나타냅니다. 구체적으로, 이 방법은 다음을 수반한다:(i) 테이프 스트리핑 방법으로 SC를 제거하여 비경피적으로 흡수된 nAg100을 제거한다[21]. (ii) 마이크로파 조사를 통해 피부를 표피층과 진피층으로 분리; (iii) NaOH 처리에 의한 표피 및 진피의 가용화; 및 (iv) sp-ICP-MS를 사용하여 각 피부층에서 Ag의 물리적 특성의 반정량적 측정
nAg100 및 Ag의 수량 및 물리적 특성을 결정하여 실제 평가
+
In Vivo의 마우스 스킨 레이어
이 접근법의 실제 적용을 평가하기 위해 우리는 마우스 피부가 nAg100 및 Ag
+
에 노출된 후 표피와 진피 및 말초 혈액에서 Ag의 양과 물리적 특성을 분석했습니다. 생체 내. 노출 5일 후, 마이크로파 조사에 최적화된 조건에서 피부를 표피와 진피로 분리하고 이전 섹션에서 설명한 대로 NaOH를 사용하여 이들을 가용화했습니다. ICP-MS 분석은 Ag가 모든 그룹의 모든 조직(예:표피, 진피 및 혈액)에 존재함을 나타냅니다. 진피와 혈액에서 Ag
+
-노출군이 nAg100 노출군에 비해 증가하는 경향을 보였다(Fig. 4a). 데이터는 이온 형태와 입자 형태가 모두 이전에 보고된 바와 같이 경피적으로 흡수 및 분포되지만 [8, 9], 이온 형태가 입자 형태보다 깊은 조직 층으로 침투하는 것이 더 쉽다는 것을 시사했습니다.
<그림><그림><소스 유형="이미지/webp" srcset="//media.springerature.com/lw685/springer-static/image/art%3A10.1186%2Fs11671-020-03421-x/MediaObjects/ 11671_2020_3421_Fig4_HTML.png?as=webp"> 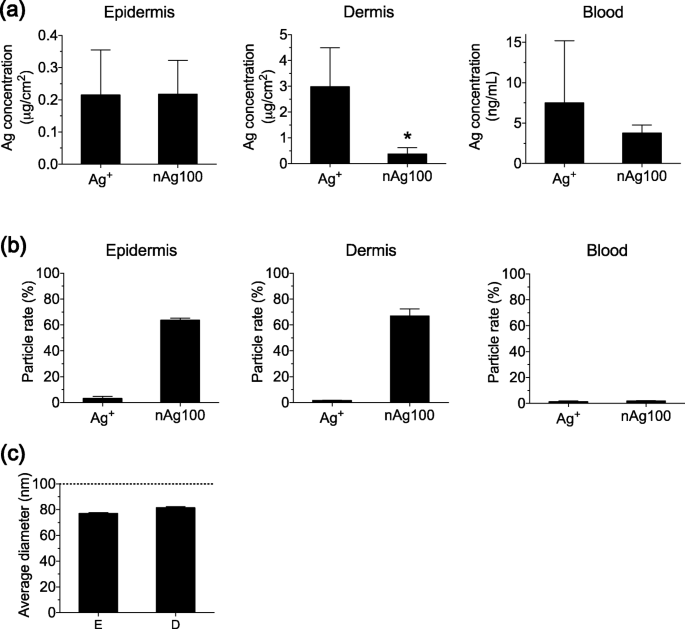
nAg100 및 Ag
+
의 반정량적 물성 분석 생체 내에서 마우스 피부에 적용했습니다. 첫째, 마우스 피부가 nAg100 및 Ag
+
에 노출되었습니다. (20μg Ag/cm
2
). 노출 5일 후 Ag의 표피, 진피 및 혈액에서 Ag의 물리적 특성에 대한 정량 및 평가를 각각 ICP-MS 및 sp-ICP-MS를 통해 수행하였다. 아 Ag 농도 및 b 표피, 진피 및 혈액에서 검출된 입자율. ㄷ 표피와 진피에서 검출된 입자의 평균 직경. 점선은 초기 입자 크기를 나타냅니다. 모든 데이터는 평균 ± S.E로 표현되었습니다. (n =3). *p <0.05 (학생의 t 테스트)
다음으로 nAg와 Ag
+
의 비율을 평가했습니다. 각 샘플에서. Ag
+
에서 -노출된 그룹, 거의 모든 Ag가 표피, 진피 및 혈액에서 이온 형태로 검출되어 Ag
+
물리적 성질의 변화 없이 경피적으로 흡수되고 분포되었다. 반대로, nAg100에 노출된 그룹에서는 표피와 진피에서 약 70%의 Ag가 입자 형태로 존재하는 반면, 나머지 Ag는 이온화되었다. 또한 말초혈액에서 검출된 Ag는 거의 완전히 이온화되었으며 입자형태는 거의 검출되지 않았다(Fig. 4b). 마지막으로 주로 입자형태가 검출되는 표피층과 진피층의 입자크기를 평가하였다. sp-ICP-MS 분석은 두 층 모두에서 검출된 입자 크기가 약 70-80 nm였으며, 이는 nAg100이 이온화되는 속도에 해당하는 것으로 나타났습니다(그림 4c). 이러한 데이터는 피부가 nAg100에 노출되었을 때 이온화되면서 흡수 및 분포될 수 있음을 시사합니다.
이전에 보고된 바와 같이 나노입자의 표면 리간드는 피부로의 흡수에 영향을 미쳤습니다[25, 26]. 예를 들어, 아미노기로 변형된 금 나노입자는 생체 외 실험에서 카르복실기로 변형된 금 나노입자보다 더 많이 마우스와 인간의 피부에 흡수되었다[25]. 또한 분자 역학 분석 결과 피부 투과 능력은 중성 소수성에서 양이온성, 음이온성 금 나노 입자 순으로 감소하는 것으로 나타났습니다[26]. 이와 관련하여 본 연구에서는 nAg100이 시트르산으로 변형되어 음전하를 띠기 때문에 초기 피부 장벽인 표피의 SC에 침투할 가능성이 적음을 추론하였다. 따라서 진피와 혈액에서 입자가 관찰되는 이유는 입자가 표피뿐만 아니라 모공을 통해 침투하기 때문일 수 있습니다.
또한 Tat 및 R7과 같은 세포 투과성 펩타이드로 변형하여 금 나노 입자의 투과성을 향상시킨 것으로 보고되었습니다[25]. 따라서 미래에는 nAgs를 피부 깊숙이 전달하기 위해 유사한 변형을 고려할 수 있습니다. 또한 비표면적이 클수록 표면 개질 효과가 더 크기 때문에 nAgs의 크기를 줄이는 것이 필요할 수 있습니다.
결론
이 연구에서 우리는 sp-ICP-MS를 사용하여 각 피부층에서 nAg100의 물리적 특성을 반정량적으로 결정하기 위한 전처리 접근법을 개발했습니다. 이 접근 방식을 사용하여 nAg100에 피부가 노출되면 nAg100이 이온화되고 흡수되어 더 깊은 층으로 분산될 수 있음을 보여주었습니다. 따라서 nAg100에 대한 피부 노출과 관련된 생물학적 반응이나 독성을 이해하기 위해서는 nAg100의 분포와 입자 크기뿐만 아니라 Ag
+
의 분포도 고려해야 할 수 있습니다. 피부 조직에 녹는 nAg100에서. 따라서 이 접근 방식은 위험 분석에 사용할 수 있는 기본 기술로서의 가능성을 보여줍니다.
데이터 및 자료의 가용성
현재 연구 중에 생성되거나 분석된 데이터 세트가 없으므로 데이터 공유는 이 문서에 적용되지 않습니다.
약어
- ENP:
-
가공된 나노입자
- nAg::
-
은 나노입자
- Ag
+
:
-
은 이온
- sp-ICP-MS:
-
단일 입자 유도 결합 플라즈마 질량 분석기
- SC:
-
각질층
- nAg100:
-
직경 100nm의 은 나노입자
- AgNO3 :
-
질산은
- NaOH:
-
수산화나트륨
- HNO3 :
-
질산
- PBS:
-
인산염 완충 식염수
- ICP-MS:
-
유도 결합 플라즈마 질량 분석기
- EDJ:
-
표피-진피 접합부







