나노물질








SF6 , 우수한 절연 매체로 고압 절연 장치에 널리 사용되어 전원 시스템의 안전한 작동을 보장합니다. 그럼에도 불구하고 장기간 사용되는 장치에서 불가피한 부분방전은 SF6의 분해를 유발합니다. 절연 성능을 저하시킵니다. 이 작업에서 DFT 계산은 ZnO로 변형된 C3의 흡착 및 감지 특성을 연구하기 위해 수행되었습니다. N(ZnO-C3 N) SF6 쪽으로 나노시트 SF6의 운영 현황을 평가하기 위한 새로운 나노 후보를 제안하기 위해 분해된 제품 절연 장치. 우리는 먼저 ZnO-C3의 구조를 조사했습니다. N 단층 및 네 가지 일반적인 SF6에 대한 흡착 거동 시뮬레이션 분해된 종, 즉 H2 S, SO2 , SOF2 및 SO2 F2 . ZnO-C3 N 단층은 SO2에서 바람직한 반응성과 감도를 나타낼 수 있습니다. , SOF2 및 SO2 F2 , 가스 분자와 큰 흡착 에너지의 강렬한 변형으로 이어집니다. 이러한 결과는 ZnO-C3 기반 가스 흡착제의 잠재적 적용을 가능하게 합니다. SF6에서 불순물 가스를 제거하기 위한 N 단층 절연 장비. 분석에 따르면 ZnO-C3 N 단층은 절연 강도를 유지하고 전력 시스템의 안전한 작동을 보장하는 데 사용할 수 있습니다.
최근 나노기술의 급속한 발전으로 새로운 나노물질을 기반으로 한 센서의 응용이 증가하고 있다. 나노 센서는 빠른 응답, 낮은 소비, 낮은 비용, 높은 감도 덕분에 의료, 군사, 가스 탐지 및 환경 모니터링 분야에서 독점적으로 연구되었습니다[1,2,3,4]. 저항형 센서는 가장 일반적으로 사용되는 센서 중 하나로 간단한 구조와 작동 메커니즘으로 인해 학자들에게 선호됩니다. 초기 단계에서 그래핀은 큰 비표면적, 높은 캐리어 이동도 및 유리한 열전도성과 같은 물리적 및 화학적 성능이 우수하기 때문에 가스 감지에서 매력적인 재료입니다[5,6,7,8]. 그러나 그래핀은 제로 밴드갭 특성[9, 10]으로 인해 가스 인식 적용에 제한이 있으며, CO, CO2와 같은 일반적인 가스를 식별하는 데 성능이 떨어집니다. , 채널4 , N2 , NO2 , NH3 , H2 , 및 H2 오 [11]. 그 후, 학자들의 공동 노력으로 그래핀과 동일한 특성을 갖지만 밴드갭이 없는 수많은 새로운 나노물질이 가스 감지 분야에서 나타났으며, 여기에는 전이 금속 디칼코게나이드(TMD)가 포함되지만 이에 국한되지 않습니다.[12,13,14 ], 금속 탄화물 및 질화물 [15], 층상 III-VI족 반도체 [16, 17], III-V족 질화물 [18,19,20].
새롭게 등장한 그래핀 유사 물질 중 C3 N은 헥사아미노벤젠 삼염산염 단결정의 직접 열분해 또는 2,3-디아미노페나진의 중합에 의해 합성되며[21, 22], 이는 가스 흡착제로 상당한 주목을 받고 있다[23,24,25]. C3 N은 본질적으로 0.39 eV의 밴드갭을 갖는 간접 반도체로, 직경이 다른 양자점을 제작하여 조정할 수 있습니다[22]. 미시적으로는 C3 N은 2개의 질소 원자로 치환된 2×2 그래핀 슈퍼셀로 간주할 수 있으며, 6개의 탄소 원자와 2개의 질소 원자가 있는 평면 벌집형 격자를 보유합니다. 추가된 N 원자의 결과로 고유 C3 N은 더 강한 화학적 활성과 더 높은 캐리어 이동도를 나타내지만 그래핀과 유사한 구조적 안정성을 유지하므로 C3 N 단층은 가스 검출을 위한 경쟁 후보입니다[26]. 흡착 능력 면에서 연구자들은 고유한 C3 N은 NO2를 검출하는데 탁월한 선택성과 감도를 가지고 있습니다[27]. 그리고 SO2 , 다른 가스의 경우 명백한 흡착 효과가 없습니다. 그럼에도 불구하고, 연구는 C3의 표면 반응성이 N은 불순물 입자의 개질에 의해 크게 촉진될 수 있다. 예를 들어, Pashangpour와 Peyghan[28]은 고유 및 도핑된 C3의 CO 흡착 능력에 대한 비교 실험을 수행했습니다. N 나노시트; 그들의 결과는 Al 도펀트가 깨끗한 C3보다 훨씬 더 강한 결합 상호작용을 일으킬 수 있음을 보여줍니다. N. 나중에 Zargham Bagheri[29]는 Si-doped C3를 이론적으로 연구했습니다. N은 아세톤의 흡착을 위한 것으로, C 원자를 Si 원자로 치환함으로써 발견되며, 흡착 에너지는 - 9.7에서 - 67.4 kcal/mol로 증가할 수 있으며, 더 많은 C 원자가 치환될수록 감도가 증가한다.
금속 산화물은 가스 상호 작용에 대한 화학 반응성을 향상시키기 위해 표면 개질에 일반적으로 사용되는 대안입니다. 금속 산화물 반도체 중 하나인 ZnO는 약 3.37 eV의 밴드갭을 가지며 약 60 meV의 여기 결합 에너지, 화학적 안정성, 우수한 광촉매 특성 및 일부 특정 가스에 대한 높은 활성을 갖는다[30]. Ref[31]에 따르면, ZnO는 0차원(0D), 1차원(1D), 2차원(2D) 나노구조 형태로 성장할 수 있으며, 각 클래스의 예로는 나노클러스터, 나노와이어/나노튜브 및 나노시트/ 각각 나노리본. 쉽게 제어되는 크기와 형태의 특성을 감안할 때[32, 33], ZnO 나노 입자는 나노 표면의 감지 성능을 향상시키는 도펀트로 작동하는 유망한 재료입니다[34,35,36]. 최근 몇몇 학자들이 단일분자 금속산화물 도펀트를 이용하여 나노물질의 표면활성을 향상시키는 이론적인 연구를 제안하고 있다. E. Mohammadi-Manesh et al. [37] H2에 대한 Cu 및 CuO로 장식된 그래핀의 흡착 능력을 조사했습니다. S는 이론적으로 H2 흡착 후 고유 그래핀과 비교하여 변형 그래핀의 전도도가 크게 변화함을 발견했습니다. S. Asadi와 Vaezzadeh[38]는 H2를 검출하기 위해 B와 CuO로 장식된 그래핀 시트를 설계했습니다. 밀도 기능 이론(DFT)에 기반한 S 및 CO. 이 작업의 시뮬레이션은 DFT에 의해 수행되었으며 계산 코드는 정의된 슈퍼셀을 기반으로 주기적으로 원자 또는 분자 구조를 확장한 다음 전체 시스템의 물리적 특성을 계산합니다. 이 방법을 기반으로 센서로 기판에 원자 또는 분자의 흡착을 사용하여 나노 구조를 연구합니다. 앞의 보고서는 단일 금속 산화물 분자 도핑에 대한 이 주제에 대한 관련 및 추가 연구를 수행하도록 자극합니다. 여기서는 C3을 도핑했습니다. 가스 감지에 대한 ZnO의 영향을 조사하기 위한 단순화로 ZnO 나노 입자 대신 ZnO 분자가 있는 N.
SF6 절연 및 소호 특성이 탁월한 가스 절연 개폐 장치(GIS)에서 널리 사용되는 매체입니다[39]. GIS의 부분방전(PD)과 같은 불가피한 사고 내부 결함은 SF6를 분해합니다. SF4와 같은 일부 저불소 황화물에 , SF3 , SF2 [40]. 이러한 부산물은 미량의 수분 및 산소와 추가로 반응하여 H2와 같은 안정적인 화학 물질을 생성합니다. S, SO2 , SOF2 및 SO2 F2 [41]. 이러한 부산물의 절연 신뢰성은 SF6보다 훨씬 낮습니다. 그리고 이들의 존재는 그대로 두면 PD 진화를 가속화할 것입니다. 따라서 GIS의 안전한 작동을 보장하기 위해서는 이러한 가스를 감지하거나 제거하는 것이 필수적입니다. 이 논문에서는 도펀트로 ZnO를 선택하고 ZnO로 수정된 C3 모델을 구축했습니다. N(ZnO-C3 N) 일반적인 SF6에 대한 흡착 성능을 연구하기 위한 단층 분해된 종(H2 S, SO2 , SOF2 및 SO2 F2 ) 이론적으로. 구조적 변화, 전자 전달 거동, 밴드 구조 및 상태 밀도(DOS)를 분석하여 C3 간의 상호 작용에 대한 ZnO 도펀트의 영향 N 표면 및 기체 분자를 종합적으로 연구했습니다. 우리 작업의 목적은 ZnO-C3의 상세한 흡착 및 감지 메커니즘을 제공하는 것입니다. SF6의 불순물 가스를 감지하거나 제거하기 위한 잠재적인 응용을 위한 N 단층 절연 장치.
DFT를 기반으로 한 모든 계산은 Dmol 3 에서 수행되었습니다. 패키지[42]. 실제 시스템의 불균일한 전자 밀도를 더 잘 설명하기 위해 Perdew-Burke-Ernzerhof(PBE) 함수 내에서 일반화된 기울기 근사(GGA [43])와 전자를 처리하기 위해 TS의 분산 보정을 사용했습니다. 교환 상관 항 [44, 45]. DFT semi-core pseudopots(DSSP)는 코어 처리를 위해 유도되었고 이중 수치 기반 양극화(DNP)는 원자 궤도 기반 세트로 선택되었습니다[46]. 몽크호르스트 팩 k - 6 × 6 × 1 메쉬의 포인트는 기하학적 최적화와 전자 구조 계산 모두에서 정의되었습니다[47]. 기하학적 최적화에서 에너지 수렴 허용오차, 최대 힘 및 최대 변위는 각각 1.0 × 10 −5 로 설정되었습니다. Ha, 0.002 Ha/Å 및 0.005 Å [48]. 또한, 단층과 인접 이미지는 상호 작용을 피하기 위해 15 Å의 진공 간격으로 분리되었습니다.
그림 1과 같이 C3의 2 × 2 × 1 슈퍼셀 N 단층과 가스 분자는 도핑 및 흡착 공정 전에 확립되고 최적화되었습니다. 최적화된 단층의 C-N 결합(1.422 Å)은 C-C 결합(1.418 Å)보다 약간 더 긴데, 이는 C 원자에 비해 N 원자의 반경이 더 크기 때문입니다. 이 작업에서 얻은 격자 상수는 4.92 Å이며 Ref. [25, 49]. 우리는 Hirshfeld 분석에 의해 분자와 단층 사이의 전하 이동을 계산하고 Q를 정의했습니다. T 기체 분자의 전하 변화를 나타냅니다. 긍정적인 Q T 기체 분자의 전자 방출 거동을 나타냅니다. 반대로 기체 분자의 전자 수용 행동을 암시합니다.
<그림>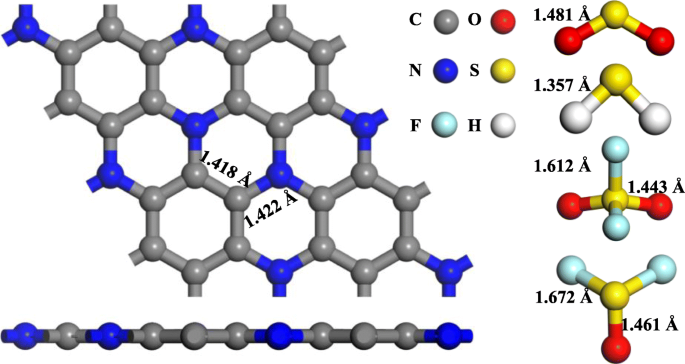
C3의 최적화된 구조 N 단층, H2 S, SO2 , SOF2 및 SO2 F2
기하학적 최적화 후, ZnO는 C3 표면에 배치되었습니다. ZnO-C3의 가장 합리적인 구성을 탐색하기 위한 다양한 방향과 위치의 N 단층 N. 그림 2a에 따르면 ZnO 입자가 C3에 접근하고 있음 수직을 통한 N 단층(O1 , O2 ) 및 병렬(O3 ) 육각형 구조의 중심 위치에서 평면에 대한 방향(PH1 , PH2 ), C-C 및 C-N 결합의 중간점(PB1 , PB2 ), C 원자 바로 위(PC ) 및 N 원자. 우리는 형성 에너지(E 양식 ) ZnO-C3의 안정성 평가 N 단층, 다음과 같이 계산됨:
$$ {E}_{\mathrm{form}}={E}_{\mathrm{ZnO}\hbox{-} {\mathrm{C}}_3\mathrm{N}}-{E}_{\ mathrm{ZnO}}-{E}_{{\mathrm{C}}_3\mathrm{N}} $$ (1) <그림>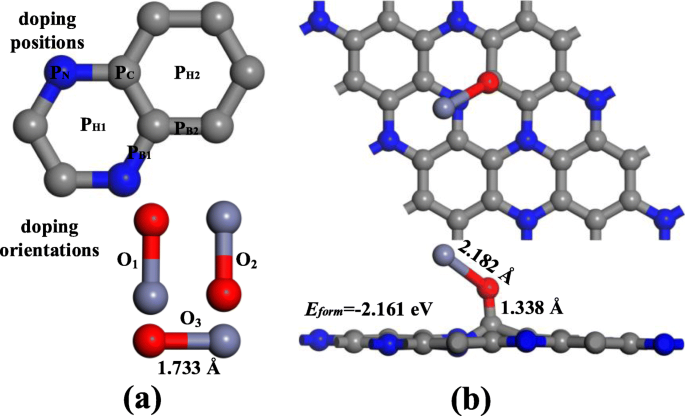
아 ZnO 분자의 접근 위치 및 방향. ㄴ ZnO-C3의 가장 안정적인 구성 N
여기서 E ZnO 및 \( {E}_{{\mathrm{C}}_3\mathrm{N}} \)는 ZnO 분자와 C3의 에너지입니다. 도핑 전의 N 단층, \( {E}_{\mathrm{ZnO}-{\mathrm{C}}_3\mathrm{N}} \)는 ZnO-C3의 에너지 N 구조. 원자 사이의 근거리 "결합"이 확장된 원자 구조에서 발생하면 총 에너지가 감소하여 음의 E가 됩니다. 양식 [50]; E가 가장 큰 구조 양식 흡착 및 추가 분석을 위해 선택됩니다.
ZnO-C3의 모든 구성 N 단층은 그림 S1, S2, S3에 표시됩니다. 이 결과는 대부분의 구조가 큰 E 양식 O2에 있습니다. 방향 및 ZnO 입자는 C3에 접근하는 것을 선호합니다. N 표면은 O 지향 위치에 있고 C 원자에 의해 포획됩니다. 또한, 이 연구의 각 수정 프로세스는 E 양식 음수이고 최대값 E 양식 ZnO 입자를 SC에 배치하여 얻습니다. O2에서 정위. 그림 2b에서 볼 수 있듯이 이원자 분자는 C3에 붙어 있습니다. N은 40°의 기울기를 가지고 있습니다. Zn-O 결합은 1.733 Å에서 2.182 Å로 늘어나며 C-O 결합은 1.338 Å으로 측정됩니다. ZnO의 영향으로 C3의 표면 N은 더 이상 평평하지 않지만 어느 정도의 왜곡이 발생하는 동시에 O 원자에 가장 가까운 C 원자가 표면에서 당겨집니다. ZnO-C3의 전자적 거동에 대한 추가 논의 N 단층, 변형 전하 밀도(DCD) 및 상태 밀도(DOS)가 그림 3에 나와 있습니다. 그림 3a에서 빨간색 영역은 전하 밀도의 증가에 해당하고 감소는 파란색으로 표시됩니다. ZnO 분자가 흡착되면 C3에서 0.255 를 추출합니다. N 단층과 뚜렷한 적색 영역은 O 원자 주위에서 인식될 수 있습니다. Zn 원자가 파란색 영역으로 둘러싸여 있는 동안 O 원자와 Zn 원자 사이의 전기 음성도 차이를 나타냅니다. 더욱이, O 원자와 C 원자 사이의 전하 밀도의 현저한 증가는 그림 3c와 같이 O 2p 궤도의 상태와 C 2p 궤도의 상태 사이의 강한 혼성화에 의해 지지될 수 있는 C-O 결합의 형성을 시사한다. 그림 3b의 DOS 곡선에서 ZnO의 도입이 전신 DOS의 증가와 몇 가지 새로운 피크의 출현으로 이어지는 것이 분명합니다. 새로 출현한 작은 피크는 약 - 2.5 eV에서 O 원자에 의해 기여하고 - 5.6 eV에 위치한 가장 큰 피크는 분명히 Zn 3d 오비탈에서 기인한 것임을 확인할 수 있습니다. DOS의 변화와 오비탈 간의 혼성화를 통해 ZnO 입자가 C3 표면에 단단히 흡착되었음을 확인 N 및 전체 시스템의 전자 구조에 큰 영향을 미쳤습니다.
<사진>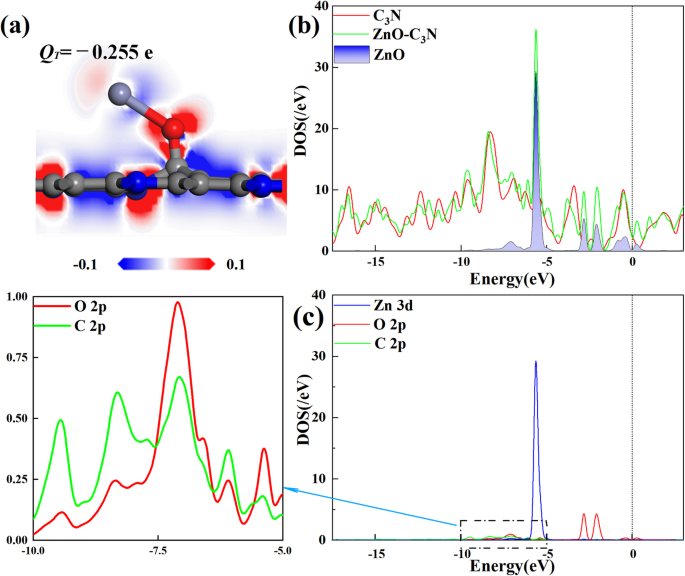
아 DCD 및 b , ㄷ ZnO-C3의 DOS 및 PDOS N 단층
가능한 흡착 매개변수를 완전히 비교하고 분석에 가장 바람직한 구성을 선택하기 위해 각 가스 분자를 ZnO-C3 표면 위에 놓습니다. 다양한 방향의 N 단층. 예를 들어, 삼원자 분자의 경우, 즉 H2 S 및 SO2 , 우리는 S 원자가 위 또는 아래로 표면에 평행하거나 수직인 세 개의 원자로 구성된 평면을 만들었습니다. 흡착 에너지(E 광고 )는 다른 흡착 구조의 에너지 변화를 설명하는 데 사용되며 다음과 같이 계산됩니다.
$$ {E}_{\mathrm{ads}}={E}_{\mathrm{ZnO}\hbox{-} {\mathrm{C}}_3\mathrm{N}/\mathrm{가스}}- {E}_{\mathrm{ZnO}\hbox{-} {\mathrm{C}}_3\mathrm{N}}-{E}_{\mathrm{가스}} $$ (2)여기서 E 가스 그리고 \( {E}_{\mathrm{ZnO}-{\mathrm{C}}_3\mathrm{N}} \) 은 분리된 기체 분자의 에너지이고 ZnO-C3 흡착 전 N 단층, \( {E}_{\mathrm{ZnO}-{\mathrm{C}}_3\mathrm{N}/\mathrm{gas}} \)는 기체가 흡착된 시스템의 에너지를 나타냅니다. 각 상황의 국부적 최소 총에너지를 구한 후 최대 E 광고 그림 4와 같이 추가 논의를 위해 선택되었으며 전하 전달 메커니즘에 대한 더 나은 이해를 위해 전자 밀도 차이(EDD)가 그림 5에 묘사되어 있습니다.
<그림>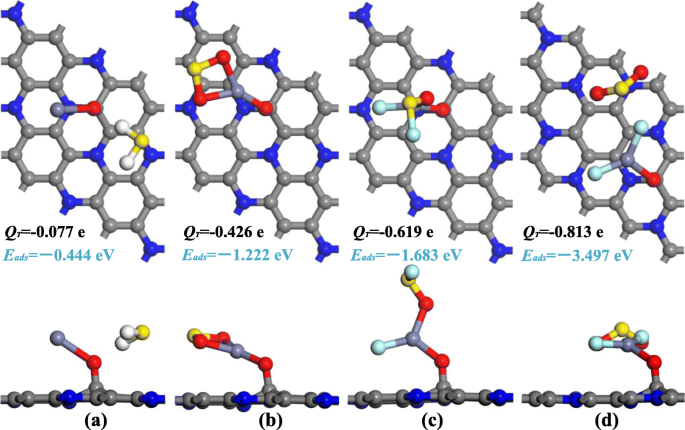
a의 흡착 구성 H2 S 시스템, b SO2 시스템, c SOF2 시스템 및 d SO2 F2 시스템
<사진>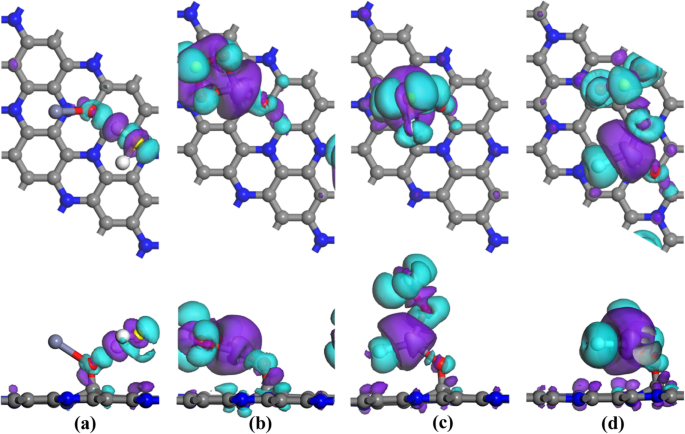
a의 EDD H2 S 시스템, b SO2 시스템, c SOF2 시스템 및 d SO2 F2 시스템
H2 S 흡착 시스템은 그림 4a에 나와 있으며, 여기서 H2 S 분자는 H2 사이의 가장 가까운 원자 거리와 평행한 위치에 흡착됩니다. 분자(H 원자) 및 ZnO 도펀트(O 원자)는 2.042 Å로 측정됩니다. 포획 H 원자의 H-S 결합은 분리된 상태의 1.357 Å과 비교하여 1.374 Å로 연장되는 반면, 다른 H-S는 흡착 과정 동안 변경되지 않은 상태로 유지됩니다. 지오메트리 구성의 약간의 변형은 H2 사이의 상호 작용을 나타냅니다. S 분자 및 ZnO-C3 N 단층은 약하다. E와 결합 광고 (− 0.444 eV) 및 Q T (− 0.077 e), H2 S 분자는 ZnO-C3에 안정적으로 부착할 수 없습니다. N 단층; 우리는 ZnO-C3 N 단층은 H2 검출에 적합하지 않습니다. S. SO2의 경우 도 4b에 도시된 분자, 2개의 O 원자는 각각 2.020 및 2.031 Å의 거리를 갖는 Zn 원자에 의해 포획된다. ZnO 입자는 표면에 더 가깝게 구부러지고 Zn-O-C에 의해 형성된 각도는 SO2의 존재로 인해 129°에서 118°로 감소합니다. . 동시에, Hirshfeld 분석에서 우리는 S 원자가 0.164 e의 손실을 가진 전자 공여체 역할을 하고 O 원자에 대한 흡착 효과가 약화되어 SO 결합이 1.481에서 1.619 Å까지 확장된다는 것을 발견했습니다. 51]. 반대로, 강화된 원자간 힘은 ZnO의 O 원자에서 전자 증가(0.292 e)로 인해 Zn-O 결합을 2.182에서 1.869 Å으로 단축했습니다. 기하학적 변화와 전자 이동 외에도 E 광고 최대 − 1.222 eV는 흡착 과정 중 강한 상호작용의 또 다른 증거이며, 이는 ZnO-C3의 잠재적 적용을 나타냅니다. SO2 검출 시 N 단층 . SOF2의 경우 그리고 SO2 F2 도 4c 및 d에 주어진 흡착 시스템에서, 표적 분자가 형태에서 극적인 변화를 겪었음을 알 수 있다. SOF2의 F 원자 S-F 결합의 구속을 제거하고 1.830 Å의 거리에서 Zn 원자에 흡착됩니다. SO2에서 훨씬 더 급격한 변화를 관찰할 수 있습니다. F2 여기서 S-F 결합은 모두 끊어지고 길이가 1.802 및 1.883 Å인 Zn-F 결합을 형성했습니다. Zn-F 결합의 형성 외에도 SOF2에 남아 있는 SOF 그룹 시스템은 또한 Zn-O 결합을 통해 Zn 원자에 의해 트랩됩니다. 그러나 SO2의 경우 F2 시스템에서 SO2 SO2 분해에 의해 생성된 그룹 F2 포착되지는 않지만 Zn 원자로부터 거리를 유지하고 S-O 결합은 분리된 SO2와 동일하게 계산됩니다. 길이. 가스 분자의 뚜렷한 변형은 큰 E와 관련이 있습니다. 광고 SOF2에서 최대 − 1.683 eV로 계산됨 시스템 및 − 3.497 eV in SO2 F2 체계. 이를 바탕으로 SOF2의 흡착 그리고 SO2 F2 ZnO-C3에 N은 이 과정에서 많은 양의 전하 이동을 수반하는 강한 화학 흡착으로 결정될 수 있으며, 이는 상당한 전자 궤도 혼성화가 존재할 수 있음을 나타냅니다. 큰 E 광고 및 Q T , ZnO-C3 N 단층은 SO2에 보다 안정적인 흡착을 제공할 수 있습니다. , SOF2 및 SO2 F2 ZnO-C3의 흡착 구성은 표 1과 같이 다른 나노 물질보다 N 단층은 나열된 나노 물질보다 0.358–3.281 eV 및 0.038–0.811 e 더 커서 가스 검출에 사용될 때 이 물질의 흡착 성능을 보장하지만 이러한 가스 분자(SO2 , SOF2 그리고 SO2 F2 ) 대형 E광고의 결과로 인한 강력한 상호작용력 제거 . 따라서 센서 중독으로 인한 성능 저하를 방지하기 위해 고온 어닐링 또는 자외선 조사와 같은 조치를 취하여 ZnO-C3의 탈착 성능을 향상시켜야 합니다. N 단층. 구체적인 탈착 성능 분석은 "가스 감지 성능 평가" 섹션에서 제공됩니다.
도 5에 도시된 EDD의 관점에서, 파란색 부분은 전자 축적 영역을 나타내고, 보라색 부분은 전자 공핍 영역을 나타낸다. H2용 S 시스템에서 H 원자와 O 원자 사이에 작은 축적 영역이 발견될 수 있지만 대부분의 축적 및 공핍 영역은 H2 주위에 있습니다. H2에서 작은 전하 이동과 분자 궤도의 재분배를 암시하는 S 분자 S 분자. SO2에서 흡착 시스템에서 S 원자와 Zn 원자를 둘러싸는 명백한 공핍 영역이 있는 반면 축적 영역은 주로 O 원자 주위와 S 원자 위에 분포됩니다. 이 현상은 SO2의 전자수신기 역할을 확인시켜줍니다. Q에 따른 분자 T (− 0.426 e) Hirshfeld 분석에서 구했습니다. SOF2에서 그리고 SO2 F2 축적 및 고갈 영역의 대규모로 판단하면 두 시스템 모두에서 현저한 전하 이동과 전자 혼성화가 있습니다. 축적 영역은 대상 가스의 원자 사이에 분포하는 반면, 공핍 영역은 주로 Zn 원자 주위에 국한되어 Zn 원자의 고유한 전자 공여 특성을 반영합니다. 결과적으로 이러한 전자적 거동은 ZnO-C3 N 단층은 더 설득력 있는 가스 분자에 강한 흡착이 있습니다.
그래핀-[56], SWCNT-[57] 및 MoSe2에서 보고된 바와 같이 - [58] 가스 센싱 연구를 기반으로 하는 DOS는 가스와 나노구조 사이의 전자적 거동을 조사하는 또 다른 중요한 매개변수입니다. 그림 6a에서 H2에서 분자 오비탈의 재분배가 S는 Fig. 5a의 EDD로부터 도출된 결론과 일치한다. H 1s 와 O 2p 궤도 사이의 혼성화는 − 4와 − 6 eV 근처에서 가능하지만 낮은 수준으로 약한 상호 작용과 새로운 H-O 결합을 형성할 가능성이 거의 없음을 보여줍니다. SO2에 관해서 그림 6c의 시스템에서 반결합 궤도는 페르미 준위 근처에서 약간 움직이고 궤도의 일부는 분리에서 연결로 변환되어 SO2에서 전자 구조의 명백한 재분배를 나타냅니다. 분자. 그림 6d의 원자 간의 상호 작용에 대해 O 2p, Zn 4s 및 Zn 3d 오비탈은 − 6, − 4 및 − 2 eV와 같은 여러 에너지 수준에서 혼성화되어 있습니다. 혼성화는 O 원자와 Zn 원자 사이의 강한 화학적 상호작용을 의미하며 최적화된 구조에서 계산된 Zn-O 결합의 형성을 효과적으로 지원합니다. SO2에서 F 및 SO2 F2 구조의 극적인 변형으로 인해 분자 궤도가 강력하게 활성화되고 새로 형성된 많은 궤도와 함께 재분배됩니다. SOF2의 F 2p 및 O 2p 궤도 − 8, − 7 및 + 3 eV에서 Zn 4s 및 3d 오비탈과 강하게 혼성화됩니다. F 원자와 Zn 원자 사이의 혼성화는 - 7, - 5 및 + 3.5 eV 근처에서 확인할 수 있습니다. Zn 원자와 갇힌 F, O 원자 사이의 명백한 혼성화는 안정적인 화학 결합, 즉 Zn-F와 Zn-O 결합이 형성되었다는 증거이며, 이는 ZnO-C 사이의 강한 흡착 효과에 대한 설명이 될 수 있습니다. 하위>3 N 단층과 두 가지 가스. H2를 제외한 4개의 흡착 시스템에서 얻은 결과와 결합 S 분자, 나머지 세 분자(SO2 , SO2 F 및 SO2 F2 ) ZnO-C3에 노출되면 단단히 흡착될 수 있습니다. N 단층. 이 결론은 물질이 고전압 장비에서 잠재적인 가스 제거 응용 프로그램을 가지고 있음을 증명합니다.
<그림>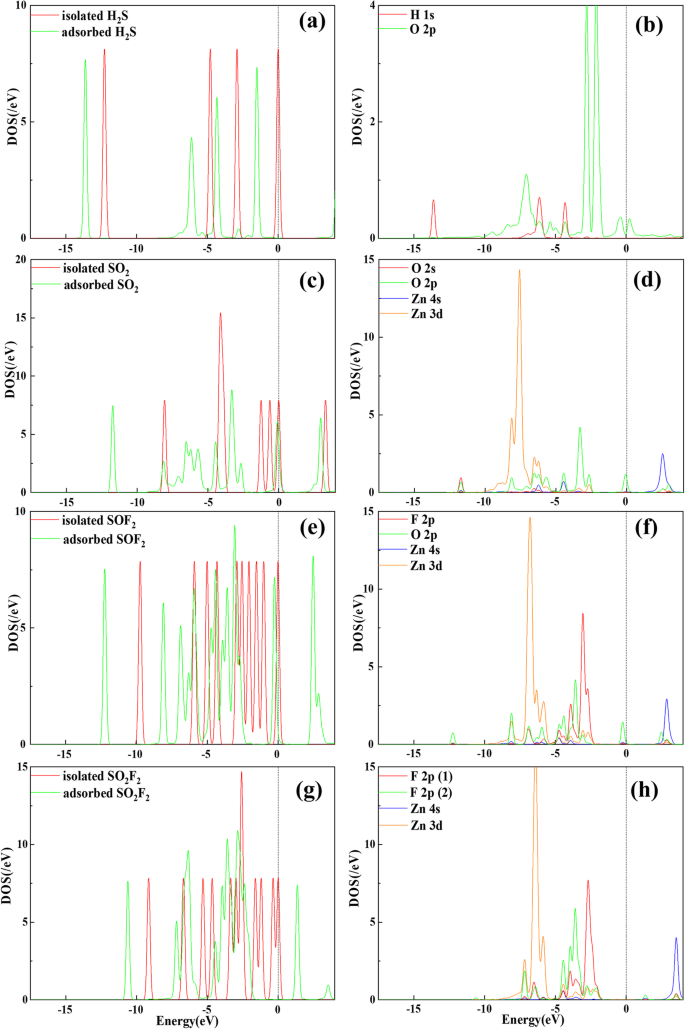
ZnO-C3에 흡착된 기체 분자의 DOS 및 PDOS N 단층. 아 , b H2 에스 시스템. ㄷ , d SO2 체계. 이 , f SOF2 체계. 지 , h SO2 F2 시스템
가스 검출을 달성하기 위해서는 후 흡착 저항 형 장치에 대한 적당한 전도도 변화가 필요합니다. 특정 시스템의 전도도는 다음 방정식에 따라 밴드갭과 관련이 있습니다[59].
$$ \sigma =A\times {e}^{-{E}_g/2{k}_BT} $$ (3)여기서 A 특정 상수, k 나 볼츠만 상수(8.62 × 10 −5 eV K −1 ) 및 T는 온도입니다. 전도도와 밴드갭 사이에는 반비례 관계가 있음을 알 수 있다. 밴드갭이 넓을수록 전자가 금지대를 넘는 것이 더 어렵다. 그림 7a는 ZnO-C3의 밴드갭이 N 단층은 0.168 eV로 매우 작으며 이는 깨끗한 C3 밴드갭의 절반 미만입니다. N(0.39 eV)인 반면, 반도체와 간접 밴드갭의 특성은 동일하게 유지되며 전도대 하단(M)과 가전자대 상단(Γ)의 위치가 다른 것으로 판단할 수 있다. 흡착 시스템의 밴드갭과 관련하여 그림 7b-d에서 다양한 변형을 찾을 수 있습니다. H2에서 S 시스템에서 밴드갭은 전도대 하단의 하향 이동으로 인해 0.125 eV로 감소합니다. 다른 시스템에서는 가전자대 상단에 나타나는 새로운 불순물 수준이 M 지점 근처에서 페르미 준위와 만나 이러한 시스템의 밴드갭이 0이 되는데, 이는 ZnO-C<하위>3 N 단층 [43, 60]. 흡착된 구조의 반도체 특성이 밴드갭이 없는 금속과 같은 특성으로 덮일 수 있지만[61], 밴드갭이 없으면 전도성이 눈에 띄게 향상될 수 있습니다. ZnO-C3 기반 장치의 응답 성능을 향상시키는 것은 매우 중요합니다. N 단층. 응답에 대한 추가 분석을 증폭하기 위해(R ) 성능, 여기에서는 다음 방정식[62]에 따라 계산합니다.
$$ R=\frac{\left|\frac{1}{\sigma_{\mathrm{gas}}}-\frac{1}{\sigma_{\mathrm{gas}}}\right|}{\frac {1}{\sigma_{\mathrm{순수}}}}=\left|\frac{\sigma_{\mathrm{순수}}-{\sigma}_{\mathrm{가스}}}{\sigma_{\ 수학{가스}}}\right| $$ (4) <사진><소스 유형="이미지/webp" srcset="//media.springerature.com/lw685/springer-static/image/art%3A10.1186%2Fs11671-020-03412-y/ MediaObjects/11671_2020_3412_Fig7_HTML.png?as=webp">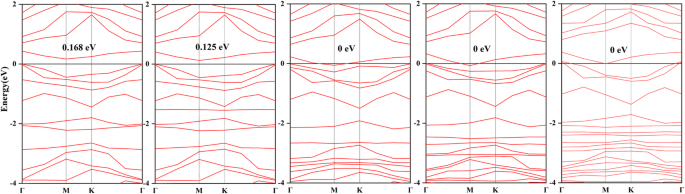
a의 밴드 구조 ZnO-C3 N 단층, b H2 S 시스템, c SO2 시스템, d SOF2 시스템 및 e SO2 F2 시스템
여기서 σ 순수 및 σ 가스 ZnO-C3의 전도도를 나타냅니다. N 시스템은 각각 흡착 전과 후입니다. 계산에 따르면 R H2용 S 시스템과 나머지 세 시스템은 0.567과 0.962, 즉 ZnO-C3 표면에 흡착이 일어날 때 전도도가 56.7%와 96.2% 증가합니다. N 단층; 이 경우 이러한 가스의 존재를 감지할 수 있습니다.
회복 시간(τ )는 흡착된 기체 분자를 제거하는데 소요된 시간을 나타내는 기체 검출에 사용되는 센서의 특성을 추정하는 또 다른 중요한 매개변수입니다. 문헌을 검토하여 τ van't Hoff Arrhenius 방정식[63]으로 계산할 수 있습니다.
$$ \tau ={F}^{-1}{e}^{-{E}_{\mathrm{a}}/{k}_{\mathrm{B}}T} $$ (5)여기서 F 시도 빈도이며 10 12 으로 정의됩니다. s −1 본 연구에서는. 이 아 는 E의 값과 동일하다고 가정되는 탈착을 위한 에너지 장벽입니다. 광고 여기, k 나 그리고 T 식과 동일하게 정의된다. (삼). 식에서. (5), 흡착된 가스에 대한 탈착은 E 광고 커지지만 작동 온도를 높여 제어할 수도 있습니다.
표 2는 4가지 가스가 ZnO-C3 표면에서 제거되는 데 필요한 회복 시간을 나열합니다. N 단층. H2의 경우 S 분자, 작은 E 광고 의심할 여지 없이 탈착을 위한 낮은 에너지 장벽을 반영하므로 마이크로초 단위의 매우 짧은 복구 시간이 발생합니다. 한편, E가 더 큰 시스템의 경우 광고 , 탈착에 며칠이 걸리기 때문에 작동 온도에서 표면에서 가스 분자를 분리하는 것은 불가능해 보입니다. 전기기기에서 드물게 발생하는 498 K와 598 K에 이르면 SO2의 분단위까지 탈착과정을 가속화할 수 있다. 및 SOF2 , 각각. 기체 분자 사이의 매우 강한 흡착(SO2 , SOF2 및 SO2 F2 ) 표면은 ZnO-C3의 잠재적인 적용을 나타냅니다. SF를 제거하기 위한 가스 스캐빈저로서의 N 단층6 분해종을 억제하고 전력계통 내부의 양호한 절연상태를 유지합니다. 또한 실제 구조에서는 C3에 ZnO 나노결정이 다량으로 존재하기 때문에 N, 그 효과가 실질적으로 향상될 것으로 기대된다. Besides, comparing to the original configuration, the activity of the gases releasing from the ZnO-C3 N monolayer is greatly impaired and can hardly exert impact on the system because of the severe deformation of the molecular structures (SOF2 그리고 SO2 F2 ). In terms of the H2 S, it is supposed that the unstable interaction and extremely short recovery time of ZnO-C3 N monolayer towards H2 S are unable to provide an effective detection as the adsorption density is supposed to be small.
In this paper, a model of ZnO-modified C3 N is established and the optimal structure is investigated by placing the ZnO particle on the surface of C3 N in various orientations and position. Thus, the adsorption parameters of the ZnO-C3 N monolayer on four SF6 decomposition species, namely H2 S, SO2 , SOF2 및 SO2 F2 , were obtained by analysing the E ads , DOS, Q T , and band structure before and after adsorption. It is found that the H2 S molecule can hardly adsorb stably on the nanostructure; at the same time, the other gases are strongly trapped in the ZnO particle. These results confirmed that the adsorption performance of ZnO-C3 N monolayer allows its potential application as gas scavenger to sweep SO2 , SOF2 및 SO2 F2 from the high-voltage equipment, which keeps the insulation strength and the safe operation of power system. Plus, the frontier molecular orbital theory implies that ZnO-C3 N monolayer possesses the possibility to estimate the dielectric state of SF6 insulation equipment as an indicator, given the obvious changes in conductivity caused by the adsorption of the abovementioned gases.
All the data and material are provided in the manuscript and supplementary file.
나노물질
초록 팁 기반 나노가공(TBN) 접근 방식은 미세구조 제작을 위한 강력하고 실현 가능한 기술임이 입증되었습니다. 분자 역학(MD) 시뮬레이션은 실험으로 완전히 밝혀지지 않은 메커니즘을 탐색하기 위해 TBN 접근 방식에 널리 적용되었습니다. 이 논문은 TBN 접근법의 MD 시뮬레이션의 최근 과학적 진보를 검토합니다. 먼저 다양한 재료에 대한 시뮬레이션 모델의 구축 방법을 제시한다. 그런 다음 절삭력 분석, 재료 제거 분석 및 표면 아래의 결함 분석을 포함하여 TBN 접근을 위한 가공 메커니즘의 분석이 논의됩니다. 마지막으로 MD 시
초록 2차원(2D) 위상 절연체(TI)의 발견은 지난 10년 동안 열전 분야에서 엄청난 잠재력을 보여줍니다. 여기에서 2D TI, Sb2를 합성했습니다. 테3 기계적 박리를 사용하여 65~400nm 범위의 다양한 두께를 갖고 마이크로 라만 분광기를 사용하여 100~300K 범위의 온도 계수를 연구했습니다. 포논 모드의 피크 위치와 선폭의 온도 의존성을 분석하여 온도 계수를 결정했으며, 이는 10–2 정도인 것으로 나타났습니다. cm−1 /K, Sb2가 감소함에 따라 감소합니다. 테3 두께. 이러한 저온 계수는 높은 성능 지수(ZT