나노물질








두경부암은 후두(목소리 상자), 입, 인두(인후), 비강 및 침샘을 둘러싸고 있는 편평 세포에서 발생하는 이질적인 질병입니다. 두경부암의 후기 진단은 환자의 생존율에 큰 영향을 미칩니다. 적절한 바이오마커로 개발 초기 단계에서 이 암을 식별하는 것이 필수 상황입니다. 편평 세포 암종 항원(SCC-Ag)은 순환하는 혈청 종양 바이오마커이며, 두경부암 환자에서 상승된 수준이 발견되었으며 종양 부피와 높은 상관관계가 있습니다. 본 연구는 산화티타늄(TiO2 )-SCC-Ag 항체에 의해 변형된 맞물린 전극 센서(IDE). SCC-Ag의 검출은 100fM 수준에서 발견되었지만 항체가 gold nanostar와 결합된 경우 10fM으로 개선되어 10배 개선되었습니다. 흥미롭게도 이러한 감도 향상은 다른 기판보다 1000배 더 높습니다. 또한, 2개의 다른 대조군 단백질을 사용하여 특이성 분석을 수행한 결과 항체가 SCC-Ag만 인식하는 것으로 나타났으며, 이는 IDE-TiO2에서 특이적으로 검출되었음을 나타냅니다. 감지 표면.
두경부암은 두경부 부위에 비정상적인 세포 성장을 보이며 널리 보고되고 있다. 그것은 인후, 입, 점막, 구강 상피, 타액선 및 비강에서 기원합니다[1]. 전 세계적으로 여섯 번째로 많이 보고되는 암입니다. 매년 644,000명 이상의 사람들에게 영향을 미칩니다[2]. 영향을받는 환자의 대부분은 진행된 단계에서 진단되며 생존에 큰 영향을 미칩니다. 두경부암의 조기 진단은 생존과 생활 방식을 개선하는 데 필수적입니다. 혈청학적 종양 표지자는 두경부암의 후속 치료를 진단하고 관리하는 데 사용되었습니다. 편평 세포는 우세한 편평 세포 암종 항원(SCC-Ag)을 방출하며, 암 환자에서 그 존재가 증가하고 SCC-Ag는 부인과, 폐암, 식도 및 항문암과 같은 편평 세포 관련 암의 유망한 종양 마커인 것으로 나타났습니다. [3, 4]. 두경부암을 고려할 때 SCC-Ag 수치가 높을수록 암 환자를 대상으로 한 여러 연구에서 입증된 바와 같이 질병 전이, 재발 및 사망률과 관련이 있습니다[5,6,7]. 연구원들은 혈청 SCC-Ag가 하인두, 구강 및 후두의 암에 대해 상당한 위험 수준에 있다는 것을 발견했습니다[8, 9]. 또한 두경부암 환자에서 SCC-Ag 수치와 종양 부피 사이에는 상관관계가 있었다[10]. 조기 치료를 제공하기 위해 두경부암의 상태를 식별하기 위해 SCC-Ag의 수준을 정량화하는 것이 현명합니다. 현재 연구는 SCC-Ag 항체에 의한 IDE(Interdigitated Electrode) 센서의 나노입자를 사용하여 낮은 수준에서 SCC-Ag를 검출하는 데 중점을 두고 있습니다.
IDE는 저비용, 휴대형 및 민감성과 같은 유망한 기능을 가진 전기화학적 바이오센서로, 특히 환경 모니터링 및 의료 진단과 함께 광범위한 응용 분야를 만듭니다[11, 12]. 감지 표면의 전기적 특성을 향상시키면 생체 분자의 감지가 향상됩니다. 나노 물질 응용은 감지 표면에서 생체 분자 검출을 향상시키기 위해 바이오 센서에 널리 사용되었습니다. 나노 물질은 크기가 더 작고 표면적이 크며 열 및 전기 전도성이 좋으며 생체 분자와 상용성이 있어 바이오 센서 분야에 적용할 수 있는 엄청난 능력을 보여줍니다[13, 14]. 나노 물질은 목적을 위해 두 가지 다른 방식으로 적용되었습니다. 하나는 표면 기능화이고 다른 하나는 검출을 개선하기 위해 분석물 또는 표적을 접합하는 것입니다[15]. 금은 잘 정립된 나노물질 중 하나로 표면 플라즈몬 공명, 도파관 모드 센서, 전기화학 센서 및 비색계를 비롯한 다양한 센서에 적용됩니다[16,17,18]. 그 외에도 은, 그래핀, 구리 및 티타늄 나노물질도 다양한 생물의학 응용 분야에 적용되었습니다. 친환경 반도체로 저비용, 티타늄 산화물(TiO2 ) SCC-Ag를 감지하기 위해 IDE에서 표면 수정에 사용되는 넓은 밴드갭을 가지고 있습니다. TiO2의 높은 전기적 및 광학적 특성으로 인해 , 그것은 대용량 목적, 광촉매 및 광전 변환에 널리 사용됩니다 [19,20,21,22,23]. 또한 친수성과 더 큰 표면적의 특성은 표면 개질에 적합하며 낮은 수준에서 생체 분자를 감지하는 데 도움이 됩니다. 이 연구에서 TiO2 생체 분자의 상호 작용이 발생할 때 전기 흐름을 향상시키기 위해 IDE 감지 표면에 코팅되었습니다. SCC-Ag의 검출을 향상시키기 위해 항체를 gold nanostar(GNS 항체)와 결합하고 TiO2에 고정화했습니다. -코팅된 표면. 금 나노물질이 결합된 생체분자는 더 높은 안정성을 보이며 적절한 배향성 표면 고정화 생체분자를 제공한다는 것이 입증되었기 때문에 검출한계를 개선하는 능력이 있다[24, 25]. 또한 단일 금 입자에 더 많은 생체 분자를 고정할 수 있어 목표 분자의 수준을 높일 수 있습니다. 이 작업에서 두 가지 다른 나노물질, 즉 TiO2 (표면 수정용) 및 GNS(항체 접합용)는 IDE 감지 표면에서 SCC-Ag의 검출을 개선하는 데 사용되었습니다. GNS의 적용은 더 많은 수의 항체를 포착하기 위해 더 큰 표면에 의해 전류 센서의 성능을 향상시킬 것으로 기대됩니다.
SCC 항원(45~55kDa 범위의 동형을 갖는 당단백질)은 Randox Life Sciences(Malaysia)에서 구입했습니다. Anti-SCC 항체는 Next Gene(Malaysia)에서 조달했습니다. (3-아미노프로필)트리에톡시실란(APTES), 에탄올아민, 알부민(45 mg/mL의 주요 혈액 단백질, 분자량 66.5kDa의 혈액 단백질의 50–70%), 인산완충식염수(PBS, pH 7.4) 티타늄 IV 이소프로폭사이드는 Sigma Aldrich(USA)에서 구입했습니다. Serpin(40~50 kDa의 분자량을 갖는 일반적으로 분포된 세린 프로테아제 억제)은 Sino Biological(중국)에서 구입했습니다. 금 나노별은 Shan et al. [26]. 획득한 모든 시약 및 화학물질은 제조업체가 권장하는 장소에 보관되었습니다.
IDE의 기본 설계 및 제작은 이전에 보고된 대로 따랐습니다[27]. 초기에 실리콘 웨이퍼는 표준 세척 용액으로 세척되었으며 알루미늄 IDE 전극은 실리콘 웨이퍼에 전통적인 습식 에칭 방법으로 증착되었습니다. 그런 다음 실리콘 웨이퍼 표면에 포지티브 포토레지스트를 증착한 후 열산화를 진행하였다. 알루미늄의 증착은 포토리소그래피 기술에 의해 수행되었습니다. 1단계는 1200rpm으로 10초, 2단계는 20초 동안 3500rpm, 10초 동안 500rpm을 사용하는 3단계가 포함되었습니다. 그런 다음 감지면에 자외선(UV)을 조사하여 IDE의 패턴을 시료 표면에 전사하였다. 이후 RD-6 현상액을 15초 동안 사용하여 현상과정을 진행하였다. 노출되지 않은 영역을 제거하기 위해 포토레지스트를 수행했습니다. 현상된 샘플은 불필요한 수분을 제거하고 SiO2 사이의 접착력을 향상시키기 위해 100°C에서 구워졌습니다. 층 및 알루미늄. 마지막으로 23 s의 알루미늄 식각액을 사용하여 노출되지 않은 부분을 제거하고 아세톤으로 세척하였다. TiO2에 의해 최종 표면이 수정되었습니다. SCC-Ag를 검출합니다. 제작된 IDE 표면은 고배율 현미경과 3D 나노프로파일러로 관찰되었다. 이미지는 관련 시스템을 사용하여 × 50 배율로 캡처되었습니다.
제작된 IDE 표면에 TiO2 용액을 코팅하고 티타늄 IV 이소프로폭사이드를 전구체로 사용하여 TiO2 용액을 제조했습니다. . 이를 위해 에탄올을 티타늄 IV 이소프로폭사이드와 혼합하고 5분 동안 격렬하게 교반하였다. 그 다음, 안정제(아세트산 100μL)를 교반 조건에서 떨어뜨리고 85 °C의 온도로 핫플레이트에서 가열하였다. 몰비 혼합물은 9:1:0.1(에탄올 대 TIP 대 아세트산)로 고정되었습니다. 3시간의 혼합 후 투명한 용액이 얻어졌습니다. 24 h의 숙성 과정에서, 용액은 이산화규소(SiO2 ) 2000rpm의 속도로 스핀 코터를 사용하여 기판. 코팅 후, 표면은 175°C의 온도에서 15분 동안 건조되었고 450°C에서 1시간 동안 어닐링되었습니다. TiO2 박막은 3중 코팅 후 충분한 두께가 됩니다.
SCC-Ag 항체는 링커 16-메르캅토운데칸산(16-MDA)을 사용하여 GNS에 고정화되었습니다. 처음에 5mM의 희석된 16-MDA를 100μL의 GNS와 혼합하고 실온(RT)에서 30분 동안 보관했습니다. GNS가 있는 결합된 16-MDA는 13,000xg에서 원심분리에 의해 제거되었습니다. , 5 분. 그런 다음 수집된 금 펠릿을 실온에서 15분 동안 배양하여 EDC(400mM)와 NHS(50mM)를 1:1의 비율로 활성화했습니다. 용액 혼합물로부터 결합되지 않은 EDC 및 NHS는 13,000×g에서 원심분리에 의해 제거되었습니다. , 5 분. 활성화된 GNS를 함유하는 펠릿을 수집하여 항체를 접합시켰다. 이어서 200nM의 SCC-Ag 항체를 EDC-NHS 활성화 GNS와 혼합하고 실온에서 1시간 동안 유지했습니다. 마지막으로, 결합되지 않은 항체는 13,000xg에서 원심분리에 의해 제거되었습니다. , 5 분. GNS와 결합된 항체는 추가 사용을 위해 4 °C에서 유지되었고 결합은 UV-Vis 분광기 스캐닝에 의해 확인되었습니다. 480~560nM 사이의 영역에서 스캔을 수행했으며 피크 최대값을 찾았습니다.
TiO2 -코팅된 IDE 표면은 APTES에 의해 아민으로 추가 변형되어 GNS 항체를 고정화했습니다. 3%(30% 에탄올로 희석)가 포함된 APTES를 TiO2에 떨어뜨렸습니다. RT에서 3 h 동안 유지합니다. 표면을 30% 에탄올로 3회 세척하여 결합되지 않은 APTES를 제거했습니다. 항체를 고정화하기 위해 위에서 언급한 활성화 단계를 따랐습니다. 항체 또는 GNS 항체를 표면에 떨어뜨리고 1 h 동안 기다렸다가 고정화 과정을 완료했습니다. 마지막으로 PBS 완충액으로 표면을 5회 세척하여 결합되지 않은 항체를 완전히 제거했습니다. 이들 항체 또는 GNS 항체-변형된 표면을 사용하여 SCC-Ag를 검출하고 비교하였다. GNS 항체 고정화 TiO2 표면은 앞에서 설명한 AFM(Atomic Force Microscopy), FETEM(field-Emission transmission electron microscopy) 및 EDX(energy dispersive X-ray) 분석기로 분석되었습니다[15]. AFM 관찰은 5 μm 규모인 반면 SEM은 15 kV로 작동되는 100 nM 규모였다. 요소의 존재는 EDX에 의해 발견되었습니다.
SCC-Ag, 항체 또는 gold nanostar 항체 변형 TiO2 검출 -IDE 표면은 항체가 없는 표면 영역을 가리기 위해 1 M 에탄올아민으로 차단되었고 실온에서 30분 동안 유지되었습니다. 에탄올아민 차단 표면에서 1 nM의 SCC-Ag가 상호작용했으며 SCC-Ag 첨가 전후에 전류 반응이 관찰되었습니다. 검출 한계를 평가하기 위해 SCC-Ag를 10fM에서 1 nM으로 적정하고 항체 또는 GNS 항체 변형 표면에 개별적으로 떨어뜨리고 전류에 대한 반응을 기록했습니다. 실험은 삼중으로 수행되었고 통계를 계산했습니다. 측정을 위해 0.01 V 단계 전압에서 0 ~ 2 V의 선형 스위프 전압을 따랐습니다. 검출 한계(LOD)는 배경 신호(S /아니 =3:1), 즉 LOD =기준선의 표준편차 + 3σ .
SCC-Ag와 그 항체의 선택적 상호작용을 확인하기 위해 세르핀과 알부민이라는 두 가지 다른 단백질을 사용하여 대조 실험을 수행했습니다. 이들 대조군 단백질의 1-nM 농도를 항체 또는 GNS 항체-변형된 표면에 떨어뜨리고, 상호작용 전후에 전류의 변화를 관찰하였다. 이러한 현재 수준은 항체 및 GNS 항체에 의한 SCC-Ag의 특이적 검출과 비교되었다. 다른 대조군 실험 설정에는 SCC-Ag와 GNS 단독 및 SCC-Ag와 TiO2의 상호 작용이 포함됩니다. - 비면역 항체 표지 GNS로 코팅된 IDE 표면. 실험은 삼중으로 수행되었고 통계를 계산했습니다. 측정을 위해 0.01 V 단계 전압에서 0 ~ 2 V의 선형 스위프 전압을 따랐습니다.
두경부암은 코, 입, 후두 및 부비동 내부 또는 주변에 다양한 종양이 발생하는 것으로 설명되었습니다[28]. 환자의 생존율을 높이기 위해서는 적절한 바이오마커를 통한 조기 진단과 치료가 필수적이다. SCC-Ag는 두경부암에 적합한 혈청 바이오마커로 발견되었습니다. 여기에서 실험은 TiO2에서 SCC-Ag의 수준을 감지하고 정량화하기 위해 수행되었습니다. - 항체에 의해 변형된 맞물린 전극(IDE) 센서. TiO2 생체 분자의 상호 작용 동안 전류 응답을 개선하기 위해 여기에서 사용됩니다. 다른 나노물질에 비해 TiO2 전극을 따라 표면에서 활성 거동과 전기 촉매 활성의 개선으로 인해 전기 화학 센서에서 매력적인 것으로 간주됩니다. 또한, 표면에 더 많은 안정성을 제공하여 전극에 의한 응답의 반복성과 피크 전류를 증가시켜 검출 한계를 향상시킵니다[29,30,31]. 이 긍정적인 특성을 활용하기 위해 본 연구에서는 TiO2를 코팅했습니다. IDE 표면(IDE-TiO2 ) 전류 흐름을 개선합니다. 또 다른 나노물질 GNS를 사용하여 IDE-TiO2에 항-SCC-Ag 항체를 고정했습니다. 표면 삭제의 한계를 강화합니다. gold-conjugated biomolecule-immobilized surface가 target의 검출을 향상시킨다는 것이 증명되었기 때문에[32, 33], 여기에서 SCC-Ag를 검출하여 항체와 GNS 항체 변형된 IDE-TiO2 표면. 다른 곳에서 일반화한 것처럼, 나노입자의 표면적이 증가함에 따라 생체분자 부착이 향상될 것입니다. 이러한 맥락에서 GNS는 구형 금 나노 입자에 비해 더 큰 표면을 갖는다. 이 아이디어를 구현하기 위해 현재 GNS를 사용하여 감도를 향상시키는 실험을 수행했습니다.
그림 1은 IDE-TiO2에서 SCC-Ag를 감지하는 개략도를 보여줍니다. 감지면. 그림 1a와 같이 초기에 IDE 감지 표면은 TiO2로 코팅되었습니다. 그리고 나서 항체는 GNS 접합의 유무에 관계없이 고정화되었습니다. 이러한 항체-변형된 표면을 사용하여 SCC-Ag 수준을 검출했습니다. 검출을 수행하기 전에, GNS와 항체의 접합을 UV-Vis 분광법으로 확인하였다. 항체와의 접합 전후에 원하는 파장 범위를 갖는 GNS 스캐닝 프로파일을 결정하였다. 고정화 후 이동이 535에서 545 nM으로 이동되었음을 분명히 알 수 있었습니다(그림 1b). 이 결과는 GNS 표면에 항체의 접합을 확인합니다. 한편, 제작된 감지면은 형태학적으로 관찰되었다. 그림 2a는 고배율 현미경 이미지를 표시하는 반면 그림 2b는 3D 나노프로파일러 이미징에서 캡처한 이미지를 설명합니다. 두 이미징 프로파일은 손가락을 형성하는 갭 및 전극 영역으로 명확하게 표시됩니다. 틈과 손가락의 배열이 균일하고 손상되지 않은 것처럼 보였습니다.
<그림>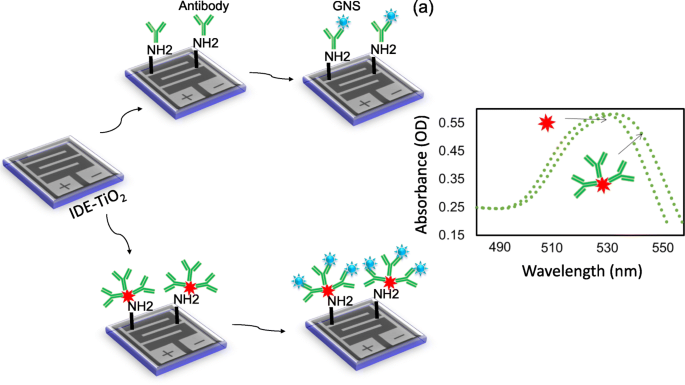
아 SCC-Ag 검출을 위한 개략도. IDE-TiO2 APTES에 의해 표면을 아민으로 변형시킨 후 항체 또는 GNS 항체를 고정화시켰다. APTES의 아민기는 항체의 카르복실기와 반응합니다. SCC-Ag는 항원 영역에서의 상호작용에 의해 검출되어 비교되었다. ㄴ GNS를 사용한 UV-Vis 분광기 측정. 스캐닝은 480과 560 nM 사이의 영역에 있었고 피크 최대값은 ~ 530 nM이었습니다. 항체가 있거나 없는 GNS는 화살표로 표시됩니다.
<그림>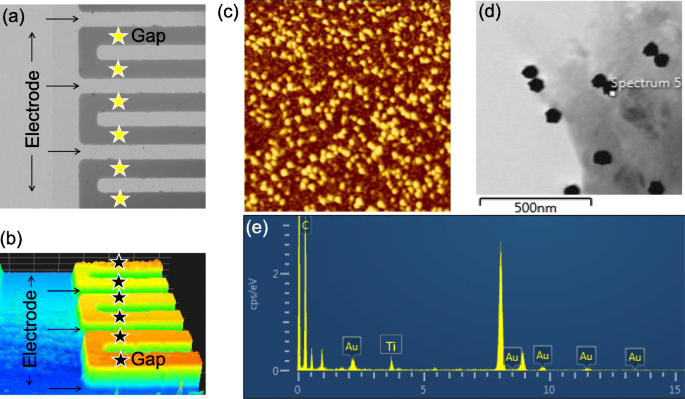
아 IDE 표면의 고배율 현미경 이미지. 이미지는 × 50에서 캡처되었습니다. b IDE 표면의 3D 나노 프로파일러 이미지. 이미지는 × 50에서 캡처되었습니다. 전극 및 갭 영역이 표시됩니다. 간격은 별표로 표시됩니다. 균일한 배열은 성공적인 제작을 나타냅니다. ㄷ 원자력 현미경 이미지. AFM은 TiO2 사이의 명확한 구별을 보여줍니다. 어두운 점과 밝은 점으로 각각 GNS. d 전계 방출 투과 전자 현미경 이미지. 이 에너지 분산 X선 분석. 표면에서 발견된 요소를 나타냄
TiO2에서 SCC-Ag가 감지되었습니다. - 항체 또는 GNS 항체 고정화 표면에 의한 IDE 표면. TiO2에 GNS 부착 표면은 AFM, SEM 관찰 및 EDX 분석으로 확인되었습니다(그림 2c). AFM 관찰에서 TiO2 사이에 명확한 구별이 나타났습니다. 어두운 점과 밝은 점으로 각각 GNS. 이것은 현저한 금과 적당한 티타늄 피크가 관찰된 SEM 및 EDX 분석에 의해 뒷받침되었습니다. 이 결과는 TiO2에서 GNS의 발생을 입증합니다. 표면. 그림 3은 amine-modified IDE-TiO2에 항체와 GNS 항체의 고정화 과정을 보여줍니다. 감지 표면. TiO2 -수정된 IDE 감지 표면은 현재 레벨을 4.65E-12로 표시합니다(그림 3a). APTES를 추가한 후 현재 수준이 5.37E-11로 증가했습니다. 이 전류 증가는 APTES에 의해 표면이 아민으로 변형되었음을 나타냅니다. 항체가 고정되면 전류 수준이 5.375E-11에서 1.05E-9로 변경되었습니다. 전류의 차이는 1.04E-9로 나타났습니다(그림 3a). 이러한 고정은 항체에서 APTES의 아민 그룹과 COOH 그룹의 화학적 상호작용으로 인해 발생했습니다[18]. 전류의 변화는 APTES 변형 표면에 대한 항체의 결합을 확인시켜주었다. 그 후, 나머지 표면은 1 M 에탄올아민으로 덮여 감지 표면에서 생체 분자의 비특이적 결합으로 인한 생물학적 오염 효과를 줄였습니다. 유사하게, GNS 항체는 TiO2에 고정화되었습니다. -IDE 표면 및 APTES 변형 표면에 GNS 항체를 고정화하면 전류 수준이 4.41E-12에서 1.23E-9로 증가했습니다(그림 3b). 항체가 GNS 표면에 고정되었을 때, 아민-변형된 표면에서 더 높은 반응을 나타내는 것을 분명히 발견하였다. 이것은 단일 GNS의 표면에 더 많은 수의 항체 결합과 아민-변형된 표면에 대한 이 복합체의 강한 결합 때문일 수 있습니다. 이 결합은 APTES의 아미노 말단기가 GNS의 시트레이트기를 대체하고 APTES로 변형된 IDE 표면에 화학적으로 고정되었기 때문에 발생했습니다[34]. 감지 표면에서 생체 분자의 감지는 주로 두 가지 요인, 즉 상호 작용하는 분자의 결합 친화도와 감지 표면에서 분자의 적절한 표면 고정에 의존한다는 것은 잘 알려져 있습니다. 감지 표면의 높은 생체 분자 고정화는 낮은 수준에서 표적의 탐지를 크게 향상시켰습니다. 이 연구에서 GNS는 IDE-TiO2에 항-SCC-Ag 항체를 고정하는 데 사용되었습니다. 효율적인 SCC-Ag 검출을 이끄는 더 높은 항체 결합의 기회를 향상시키기 위해 표면.
<그림>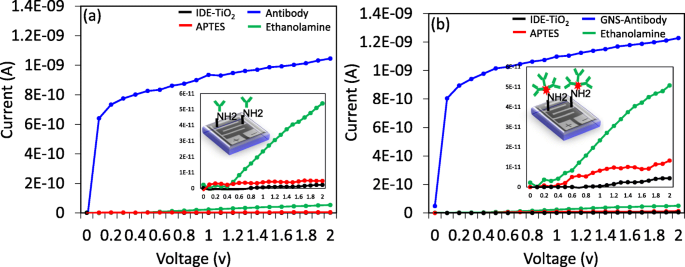
IDE-TiO2의 고정 프로세스 표면. 아 항체로. ㄴ GNS 항체로. 표면 변형은 3% APTES에 의해 시작되었고, 이어서 EDC 및 NHS 활성화로 항체를 고정시켰습니다. 1 M 에탄올아민을 사용하여 미부착 항체 영역을 차단했습니다. 측정을 위해 0.01 V 단계 전압에서 0 ~ 2 V의 선형 스위프 전압을 따랐습니다. 각 고정 후 전류의 적절한 변화는 감지 표면에 항체와 GNS 항체의 결합을 확인했습니다
항체 GNS는 IDE-TiO2에 효율적인 고정을 보여주기 때문에 표면에서 유사한 1 nM 농도의 SCC-Ag가 항체 표면과 GNS 항체 표면 모두에서 검출되었으며 현재 수준의 변화를 비교했습니다. 그림 4a는 항체 변형 표면에서 1 nM의 SCC-Ag 검출을 보여줍니다. 검출을 수행하기 전에 항체 변형 표면을 차단제 에탄올아민으로 덮어 생체 분자의 비특이적 결합을 방지했습니다. 에탄올아민은 4.65E-12로 전류 변화를 보여줍니다. 1 nM의 SCC-Ag를 첨가한 후, 전류 수준을 1.33E-09로 증가시켰다. 이러한 현재의 변화는 SCC-Ag의 항체에 대한 결합을 분명히 나타냅니다. GNS 항체 표면의 경우 에탄올아민은 현재 수준을 1.33E-11로 나타냅니다. 1 nM의 SCC-Ag를 추가한 후 1.62E-09로 증가했습니다(그림 4b). GNS 항체의 현재 변화는 유사한 농도의 SCC-Ag에 대해 항체-변형된 표면만 있는 경우와 비교하여 더 높았습니다. 이것은 IDE-TiO2에 결합된 항체 수가 더 많기 때문일 수 있습니다. GNS를 통해 표면.
<그림>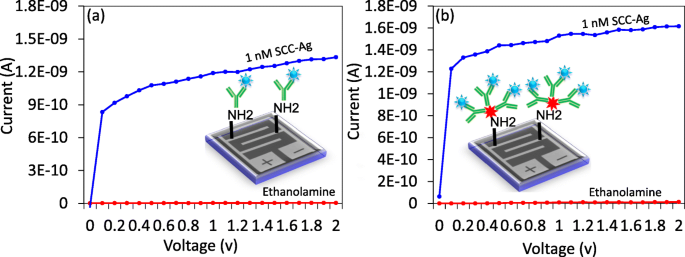
a를 사용한 SCC-Ag 감지 항체 및 b GNS 항체. IDE-TiO2에서 테스트됨 1 M의 에탄올아민이 차단될 때까지 위의 단계로 표면. 측정을 위해 0.01 V 단계 전압에서 0 ~ 2 V의 선형 스위프 전압을 따랐습니다. 1 nM의 SCC-Ag와 상호작용한 후 전류 수준은 두 경우 모두 증가했습니다. 동시에 GNS 항체로 더 높은 전류 변화를 보여줍니다.
항체 또는 GNS 항체 변형 표면은 SCC-Ag의 명확한 검출을 나타내며, 비교를 위해 양쪽 표면에서 검출 한계를 추정했습니다(그림 5a, b). 이를 위해 10fM에서 1 nM의 SCC-Ag 농도를 희석하여 이러한 표면에 개별적으로 떨어뜨리고 전류의 변화를 기록했습니다. 그림 5a는 항체 변형 표면에 대한 다양한 농도의 SCC-Ag 결합을 보여줍니다. 에탄올아민 후 10fM의 SCC-Ag가 상호작용했으며 전류 변화가 감지되지 않았습니다. 농도를 100fM으로 증가시키면 전류가 4.65E-12에서 6.54E-11로 약간 변경되었습니다. 또한, 농도를 1pM, 10pM, 100pM 및 1nM으로 증가시켰고, 전류 수준은 각각 4.69E-10, 7.91E-10, 8.78E-10 및 1.33E-09로 증가시켰다. 이러한 결과는 농도가 증가함에 따라 결합도 증가한다는 것을 분명히 나타냅니다. 검출 한계는 3σ을 기반으로 계산되었습니다. , 100fM에 있었습니다(그림 6a).
<사진>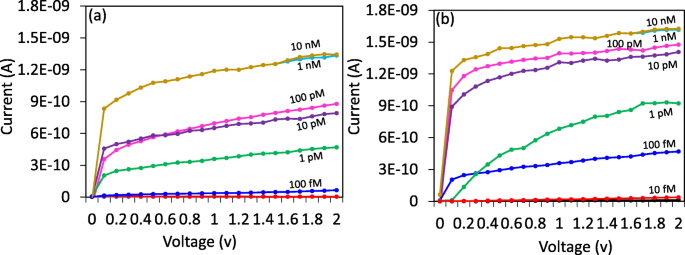
a와의 용량 의존적 상호작용 항체 및 b IDE-TiO2의 GNS 항체 표면. 표면은 1 M의 에탄올아민이 차단될 때까지 위의 단계를 따릅니다. 측정을 위해 0.01 V 단계 전압에서 0 ~ 2 V의 선형 스위프 전압을 따랐습니다. 10fM에서 10 nM까지의 SCC-Ag 농도는 양쪽 표면에서 상호작용했으며 현재의 변화가 감지되었습니다. 세척은 10 mM PBS(pH 7.4)를 사용하여 각 단계에서 5개의 반응 부피로 수행되었습니다. SCC-Ag 농도가 증가함에 따라 두 경우 모두 현재 수준이 점차 증가했습니다. GNS 항체는 10fM에서 현재의 변화를 보여주지만 100fM에서 변화는 항체에서만 나타났습니다. 두 경우 모두(항체 및 GNS 항체) 1 nM SCC-Ag는 포화 상태를 나타냅니다. 농도를 더 높이면 전류의 큰 변화가 관찰되지 않습니다.
<그림>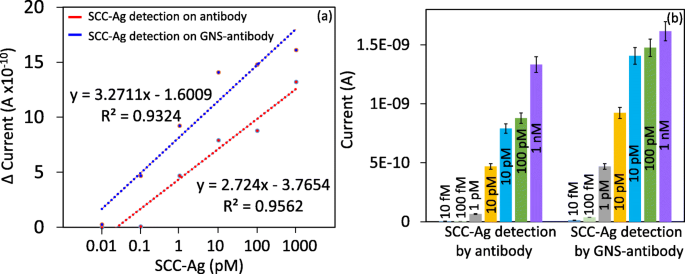
항체 및 GNS 항체 변형 표면에서 다양한 농도의 SCC-Ag에 따른 전류 변화 비교. 아 SCC-Ag 검출 한계에 대한 선형 회귀 그래프. 항체 포함(빨간색 선) 및 GNS 포함 항체(파란색 선)가 표시됩니다. 검출한계는 GNS 항체의 경우 10fM, 항체만 있는 경우 100fM으로 확인되었습니다. ㄴ SCC-Ag 및 항체 상호작용에 따른 현재 변화. 모든 농도에서 더 높은 수준의 전류 변화가 GNS 항체 표면에서 발견되었습니다. 측정을 위해 0.01 V 단계 전압에서 0 ~ 2 V의 선형 스위프 전압을 따랐습니다. 오차 막대는 삼중의 평균 값을 나타냅니다(n =3) 표준 편차는 ± 0.1 ~ 0.15 × 10 −9 범위입니다. A. 검출 한계(LOD)는 백그라운드 신호(S /아니 =3:1), 즉 LOD =기준선의 표준편차 + 3σ
동일한 농도의 SCC-Ag는 GNS 항체 변형 표면에서 독립적으로 상호작용했습니다. 10fM의 SCC-Ag를 표면에 떨어뜨리면 전류가 1.33E-11에서 3.74E-11로 명확하게 변경되었습니다. 이 결과는 10fM의 SCC-Ag라도 GNS 항체가 고정된 표면과 명확하게 상호작용할 수 있음을 보여주며, 이는 항체만으로는 감지할 수 없습니다. 또한 농도를 100fM, 1pM, 10pM, 100pM 및 1 nM으로 증가시키면 현재 수준이 4.69E-10, 9.23E-10, 1.41E-09, 1.48E-09 및 각각 1.62E-09(그림 5b). 표준 편차가 있는 통계 계산은 ± 0.1 ~ 0.15 × 10 −9 범위에 있습니다. A. 위의 두 표면의 센싱과 비교할 때 GNS 항체 변형 표면은 테스트한 모든 SCC-Ag 농도에서 더 높은 전류 변화를 나타냅니다(그림 6b). 3σ 기준 , 그것은 10 fM으로 검출 한계를 찾을 수 있습니다(그림 6a). 이것은 항체-변형된 표면만 비교했을 때 10배 더 나은(낮은) 검출입니다. 표준 편차를 사용한 통계 계산은 ± 0.1 ~ 0.15 × 10 −9 범위에 있습니다. A. 이전에 SCC-Ag는 스트론튬 나노입자 및 그래핀과 같은 다양한 나노물질에 대해 평가되었습니다. 그러나 이러한 표면은 현재 연구에 비해 ~ 1000배 낮은 감도를 나타냈습니다[35].
SCC-Ag의 선택적 검출은 혈류에 풍부한 세르핀 및 알부민의 두 가지 대조군 단백질과 비교되었습니다. Serpin은 다양한 인간 생리학적 기능과 생물학적 과정을 수행하는 프로테아제 억제제인 반면, 알부민은 45 mg mL −1 를 차지합니다. 혈청에 50~70% 기여합니다. 그림에서 볼 수 있듯이 이 두 대조군 단백질과 SCC-Ag의 1nM 농도는 표면 항체 또는 GNS 항체에 개별적으로 떨어뜨렸습니다(그림 7a). 현재의 변화는 두 경우 모두 SCC-Ag에서만 감지되었으며, 이는 항체가 SCC-Ag만 인식할 수 있음을 나타냅니다. 대조군 단백질의 상호작용과 함께 전류에서 유의미한 변화가 관찰되지 않았다. 이 실험은 현재 실험 설정이 SCC-Ag를 특이적으로 감지/진단할 수 있음을 확인합니다. 추가 지원은 SCC-Ag와 GNS 단독 및 SCC-Ag와 TiO2의 상호 작용에 의한 다른 대조군 실험에 의해 제공되었습니다. - 비면역 항체 표지된 GNS로 코팅된 IDE 표면. 특정 상호작용과 비교하여 인지된 전류에는 큰 변화가 없었습니다(그림 7b).
<그림>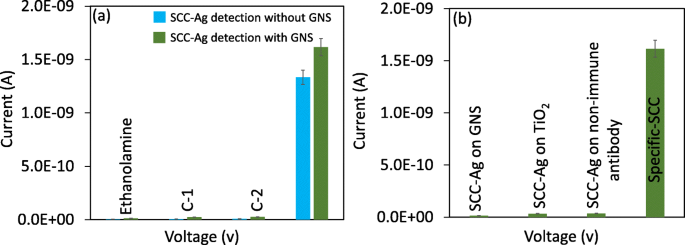
아 항체 및 GNS 항체 변형 표면에서 SCC-Ag의 선택적 검출. C1-세르핀 및 C-2-알부민과의 상호작용이 수행되었습니다. 표면은 1 M의 에탄올아민이 차단될 때까지 위의 단계를 따릅니다. 값은 삼중으로 평균을 냈습니다. 두 경우 모두 항체는 SCC-Ag만 인식하여 특이적 검출을 나타냅니다. ㄴ 측정을 제어합니다. 특이성 상호작용은 비특이적 상호작용과 비교됩니다. 분명한 차별이 눈에 띄었다. 측정을 위해 0.01 V 단계 전압에서 0 ~ 2 V의 선형 스위프 전압을 따랐습니다. 오차 막대는 삼중의 평균 값을 나타냅니다(n =3) ± 0.1 ~ 0.15 × 10
−9
범위의 표준 편차 답>
두경부암은 입, 인후 및 침샘 부위에 영향을 미치는 흔한 암입니다. Diagnosing head and neck cancer with a suitable biomarker is mandatory to give the necessary treatment to the patients and improve their lifestyle. SCC-Ag has been found to be one of the important biomarkers for cancers; herein, SCC-Ag was detected on the titanium oxide-coated interdigitated electrode sensing surface (IDE-TiO2 ). Antibody for SCC-Ag was immobilized on IDE-TiO2 surface and detected the SCC-Ag. The detection limit was found as 100 fM, and further increment in the limit of detection was attained by conjugating the antibody with gold nanostar (GNS antibody). The limit of detection was improved by 10-folds (to 10 fM), this might be due to the larger number of antibody bound on the amine-modified TiO2 surface through GNS. Moreover, control experiments were carried out with two different proteins and not able to recognize by the anti-SCC-Ag, indicating the selective detection of SCC-Ag. The demonstrated IDE-TiO2 sensing surface helps to diagnose the head and neck cancer, a strategy can be followed for the earlier detection.
All of the data are fully available without restriction.
16-Mercaptoundecanoic acid
(3-아미노프로필)트리에톡시실란
Gold nanostar
Interdigitated electrode
인산염 완충 식염수
실내 온도
Squamous cell carcinoma antigen
Silicon dioxide
Titanium oxide
자외선결론
데이터 및 자료의 가용성
약어
나노물질
화학적 흑화로도 알려진 흑색 산화물 코팅은 일종의 전환 코팅으로 기어, 유압 블록 및 도구 및 기계 부품과 같은 응용 분야에서 일반적으로 작고 복잡한 움직이는 부품에 사용됩니다. 이 코팅은 다른 마감재와 동일한 효과를 제공할 수 있지만 비용이 저렴하고 고유한 장점이 있기 때문에 독특합니다. 다음은 흑색 산화물 코팅의 정의, 공정 및 장점에 대한 자세한 소개입니다. 무엇을 인가 흑색 산화물 코팅 ? 흑색 산화철을 철 금속 및 기타 유형의 재료로 형성하는 과정을 일반적으로 흑색 산화물이라고 합니다. 흑색 산화물 공정은 철 금속
표면 연삭은 회전하는 숫돌을 사용하여 재료의 표면을 매끄럽게 하고 금속 또는 비금속 재료의 표면을 매끄럽게 하여 보다 세련되게 보이게 하는 마무리 공정입니다. 연삭 휠의 표면에 가장 일반적으로 사용되는 연마 재료는 알루미나, 탄화규소, 다이아몬드 및 입방정 질화붕소(CBN)입니다. 표면 연삭 유형 표면 그라인더 및 작업대의 구조적 특성 및 구성에 따라 표면 그라인더는 수평 스핀들 왕복 테이블 표면 연삭, 수평 스핀들 회전 테이블 표면 연삭, 수직 스핀들 왕복 테이블 표면 연삭, 수직 스핀들 왕복 테이블 표면 연삭의 4 가지