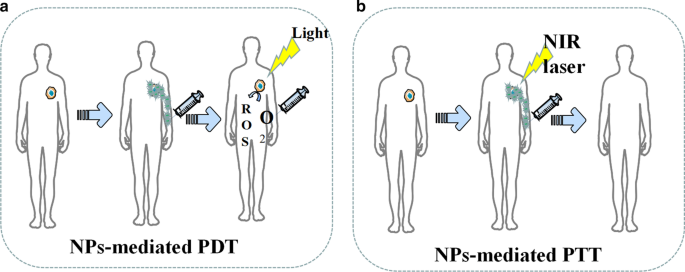
현재 나노입자(NPs)를 기반으로 한 광열치료(PTT)와 광역학 치료(PDT)는 종양 치료 중 강력한 효능, 작은 침윤 및 경미한 부작용의 장점을 보여주었다(그림 6)[80]. 종양 세포를 직접 죽이는 것 외에도 PDT 및 PTT 치료에 의해 생성된 죽은 종양 세포의 단편은 광열 및 광역학 면역 요법이라고 불리는 지속적인 면역 반응을 유발하는 잠재적 항원으로 사용될 수 있습니다[81]. PTT 치료 개념을 기반으로 설계된 나노 입자는 빛 에너지를 열 에너지로 변환하여 암세포를 죽일 수 있는 새로운 유형의 광열 변환 나노 물질입니다. 기존의 광열 변환 물질과 비교할 때 나노 입자는 많은 장점이 있습니다. 첫째, 나노입자는 입자 표면 변형을 통해 종양 표적 응집 효과를 얻을 수 있으며, 이는 표적 종양의 농축 능력을 높이는 데 기여한다[82, 83]. 둘째, 나노 입자는 CT, MRI 및 광음향 영상으로 정확하게 위치를 지정할 수 있는 기존의 광열 물질보다 더 나은 영상 기능을 가지고 있습니다[84, 85]. Pan et al.에 의해 합성된 표적 나노입자. 0.2W/cm
2
미만에서 PTT를 수행할 수 있습니다. NIR은 종양 세포 핵 DNA를 파괴하고 DNA 복구 과정을 억제하여 종양 세포 사멸을 유도합니다[86]. 표 5는 PDT 및 PTT에서 사용되는 NP에 대한 몇 가지 최근 예를 나열합니다.
<그림>
NP 매개 PDT 및 PTT의 도식적 설명. 아 NP는 활성 산소의 생성을 촉진합니다. ㄴ NP는 PTT 동안 종양 손상을 향상시킵니다.
또한 일부 연구에서는 나노입자 매개 PTT가 종양 다제 내성(MDR)을 역전시킬 수 있음을 발견했습니다. 약물 수송체, 다제 내성 관련 단백질 1(MRP1) 및 p-당단백질(p-gp)의 과발현은 일반적으로 다양한 종양에서 MDR을 유발하는 것으로 여겨집니다[95]. 예를 들어, Li et al. PTT에서 MRP1의 발현을 억제하여 결과적으로 A549R 세포의 약물 내성을 역전시킬 수 있습니다[96]. Wang et al. 금 나노 입자와 탄소 기반 나노 입자 모두 PTT에서 열 충격 인자 삼량체의 발현을 촉진하여 p-gp의 생성을 억제함으로써 DOX 내성을 극복할 수 있다고 보고했다[97, 98]. 게다가, 나노입자 매개 PTT는 종양 세포막의 완전성을 파괴함으로써 화학요법의 효과를 증가시킬 수도 있습니다[99].
PDT is a treatment that uses the selective retention of photosensitizing substances (PSs) in tumor tissue under the activation of specific wavelength excitation light and the presence of molecular oxygen to produce singlet oxygen and other reactive oxygen species, which leads to tumor cell apoptosis and necrosis [100]. However, traditional PS has poor tumor targeting, poor solubility, and instability, which is vulnerable to the internal environment [100]. Nanoparticle carriers modified by targeted molecules can not only improve the stability and biocompatibility of PS but also deliver PS to target cells, which improves the efficacy and reduces adverse effects [100]. Additionally, some common nanomaterials, like gold nanorods, have excellent PTT effects themselves. For example, Vankayala et al. found that the exposure of gold nanorods to near infra-red light (915 nm) were able to efficiently induce the generation of singlet oxygen [100].
In recent years, the role of up-conversion (UC) nanoparticles in PDT has attracted much attention. The NPs can convert long-wavelength light excitation into multiple short wavelengths, which enables the UC to replace the traditional ps-dependent short-wavelength excitation light with the near-infrared light with strong tissue penetration ability [101]. For example, Li et al. developed dual-band luminescent lanthanide nanoparticles as a PS carrier. This UC nanoparticles rely on the excitation light wavelength of 808 nm to achieve image-guided PDT without affecting imaging signals [102].
Since most photosensitive materials utilized in the phototherapy are metals, the biocompatibility of NPs designed for inorganic nanomaterials like metal ions still needs to be improved.
NPs-mediated phototherapy is now credited for not only the effectiveness against tumor but also the potential for spare internal space of nanoparticles since the therapy only utilizes the physical properties of NPs skeleton. Therefore, NPs are often multifunctioned by PDT and PTT. In the future, such NPs may be designed as dedicated NPs for tumor stem cells that are not sensitive to chemotherapy. Tumor stem cells are dormant for a long time and have a variety of drug-resistant molecules, so it is difficult to kill them by conventional treatments like chemotherapy, whereas the light therapy is more effective by killing the tumor stem cells physically. In the future, nanophysical therapy may be used with many other techniques, such as the multifunctional NPs for photothermal therapy after cryosurgery. Multifunctional NPs mediated therapy can give full play to its characteristics of low side effects, strong local lethality, and tumor stem cell killing. In addition, because nano-physiotherapy has a local killing effect and can effectively kill tumor stem cells, it may become a treatment method for small metastases.
Nanoparticles for Radiotherapy
Radiotherapy (RT) is a tumor treatment technique that kills local cells by ionizing radiation generated by rays and is currently an effective treatment for many primary and metastatic solid tumors [103]. Experiments prove that radiotherapy can effectively kill tumor stem cells [104].However, how to further improve the efficacy of radiotherapy is still a serious challenge. In recent years, nanoparticles in the field of radiotherapy have demonstrated strong radiosensitization capabilities, tumor-targeted delivery capabilities of radiosensitizing drugs, and imaging guidance enhancement capabilities [105]. At present, the most popular nanoparticles are made by high Z (atomic number) metal materials, which are featured by chemical inertness and strong radiation absorption capacity. They produce various reactions such as photoelectric effect and Compton effect after absorbing radiation, thereby releasing a variety of particles such as optoelectronics, Compton electrons, and Auger electrons. These electrons react with organic molecules or water in tumor cells to generate a large number of free radicals, leading to synergistic chemotherapy [106]. Common chemotherapy-sensitized NPs are currentlycategorized as precious metals, iron oxides, and semiconductors in terms of materials.
Precious metals NPs are made of high atomic number metal materials such as gold, silver, gadolinium, hafnium, platinum, bismuth, etc. [107]. Among them, gold nanoparticles have become the most popular NPs due to their good biocompatibility, chemical stability, and relatively strong photoelectric absorption coefficient [108]. In 2000, Herold et al. discovered the chemosensitizing ability of gold nanoparticles in kilovoltage X-rays. Nowadays, the specific mechanism of chemosensitization of gold nanoparticles is not yet clear, and the mainstream view believes that it depends on the photoelectric absorption capacity of high atomic number [109]. In addition to this, there are studies suggesting that the presence of gold nanoparticles improve the chemical sensitization of DNA to radiation, which increases the DNA damage induced by ionizing radiation (IR). At the same time, gold NPs can catalyze the mechanism of radiotherapy sensitization such as free radical production [105]. For instance, Liu found that AuNPs could significantly increase the production of hydroxyl radicals as well as the killing effect of x-rays and fast carbon ions on cells [110]. The hypothesis of the chemotherapy sensitization mechanism of other precious metals is similar to that of gold nanoparticles. Particularly, platinum NPs have an anti-tumor effect due to the inherent nature. Consequently, platinum NPs are expected to play the role of chemotherapy and radiotherapy simultaneously. However, the number of relevant research reports is insufficient, and the sensitizing effect of platinum NPs is also questionable. For example, Charest et al. reported that liposomal formulation of cisplatin was able to increase the uptake of platinum by tumor cells, and could enhance the killing of F98 glioma cells by γ-rays at the same time [111]. On the contrary, Jawaid et al. reported that platinum NPs would reduce the generation of reactive oxygen species (ROS) and the efficacy of radiotherapy during chemotherapy [112].
Iron oxide nanoparticles (IONs), especially the superparamagnetic magnet Fe3 O4 , have shown great potential in image-guided tumor radiotherapy because they are capable of enhancing the dose of radiotherapy and MRI imaging, whereas its sensitization mechanism is not clear yet. Its sensitization mechanism is not yet clear. Some studies believe that iron oxide NPs mainly catalyze the generation of ROS through Fenton's reaction and Haber–Weiss reaction. Then the highly reactive ROS will kill tumors [112,113,115]. Other studies propose that the mechanism depends on the radiation sensitization and synergistic effects of magnetic nanoparticles. As Khoei reported, iron oxide NPs can improve the radiosensitization of prostate cancer cells in vitro [116]. Huang et al. pointed out that cross-linked dextran-coated IONs (CLIONs) could be internalized by HeLa cells and EMT-6 mouse breast cancer cells, which enhances radiation therapy [117]. Although the synergistic effect of iron oxide NPs is obvious, its biological safety still needs to be improved. Many studies have proved that the biocompatibility and chemical stability of iron oxide NPs are questionable, and it has certain toxicity [118].
Semiconductor NPs like silica NPs have also been found to have a synergistic effect on radiotherapy. For instance, Zhang et al. used flow cytometry analysis and MTT experiments to find that mesoporous silica NPs can effectively enhance the radiotherapy of glioblastoma [119]. He et al. reported the mechanism of radioactive enhancement of silica NPs. He found that under X-ray irradiation, silica nanoparticles could produce fine hydroxyl radicals, which can effectively kill tumor cells [120].
At present, although many experiments have confirmed that NPs were able to sensitize radiotherapy, the specific mechanism of sensitization is still unclear, which hinders the development of new sensitized NPs. There are some doctrines like sensitizing chemotherapy that promotes free radical production. Nevertheless, there is a lack of a quantitative relationship among the amount of free radical production, radiation intensity, and physical data of nanoparticles. In addition, most sensitized NPs are made of high atomic number metals. These metals have many disadvantages in human body such as difficulty in self-metabolism and biodegrading. Meanwhile, long-term accumulation of the metals will produce toxicity, which limits the safe use of radiosensitized NPs. Moreover, compared with the radiotherapy sensitization NPs, fewer studies focused on NPs which can prevent the adverse reactions of radiotherapy and protect healthy tissues. The research on radiotherapy protective NPs is short in quantities.
In the future, searching for NPs material that can be metabolized by the kidney, biometabolized, biocompatible, stable in physicochemical properties, and inherently less toxic, or looking for surface modification that can help the body metabolize NPs may become a research direction for sensitized NPs. Moreover, although there have been many NPs studies on multi-function, namely simultaneous sensitization of radiotherapy and chemotherapy, there are still many potentials in this field, which are worthy of focus in the future. The development of protective NPs that can protect normal tissues around radiotherapy and alleviate poor defense against radiotherapy may also become a research direction.
결론
The poor curative effect, inefficient targeting ability, various side effects, and potential biological risk are some of the unfavorable attributes of conventional cancer therapy and diagnosis. In recent years, advanced nanotechnology and molecular cell biology have promoted the applications of NPs in cancer field. Not only metal NPs, but also many lipid, nucleic acid and silicon NPs showed evident outperformance in cancer diagnosis and treatment.. Moreover, new generation of NPs is no longer limited to solo but multiple functions. For example, gold-coated poly(lactic-co-glycolic acid) (PLGA) NPs equipped with PD-1 blockers which were designed by Luo et al. can not only target drug delivery but also mediate PTT therapy [121]. (Pd @ Au) / Fe3O4 Spirulina NPs with doxorubicin created by Wang et al. demonstrated the functions of photothermal therapy, delivery of chemotherapy drugs, and magnetic field control in cell experiments [122]. Multifunctional nanoparticles will become the trend of future research.
At present, we find that most of the nanoparticles only stay in vivo and in vitro stage. According to this review, we think the following reasons hinder the clinical application of NPs.
- (i)
Lack of injection routes and methods
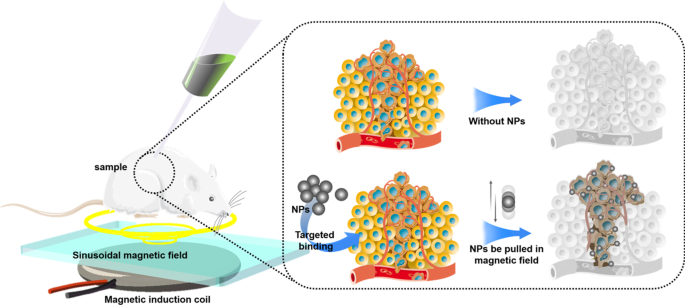
Most NPs are injected into body via puncture or intravenous injection. Therefore, the blood flow will take away NPs, making NPs difficult to stay in the target area for a long time, which leads to just few NPs that can be uptaked by tumor cells. Low-concentration drugs cannot produce the expected therapeutic effect, and low-concentration NPs also affect the physical killing effects of PDT, PTT, cryosurgery, and radiotherapy. In our opinion, magnetic NPs platform may be a solution. There have been many in vitro and in vivo experiments that have proved the feasibility of using the three-dimensional magnetic field to control the movement of NPs against blood flow [122,123,125]. However, how to solve the interference of the human body to the magnetic field, how to solve the impact of blood cells colliding with NPs, and how to control a large number of NPs in a group are still in discovery.
- (ii)
Difficulty in localization of NPs in vivo
Compared with the human body, the size of NPs is too tiny. Even if NPs are loaded with fluorescent proteins, it is still difficult for conventional imaging equipment (CT, X-ray, MRI) to locate the NPs in the human body in real time. To deal with this challenge, photoacoustic computed tomography (PACT) may be a solution. Photoacoustic computed tomography (PACT) has attained high spatiotemporal resolution (125-μm in-plane resolution and 50-μs frame
−1
data acquisition), deep penetration (48-mm tissue penetration in vivo), and anatomical and molecular contrasts [126]. Because of excellent performance, PACT has great potential in NPs localization imaging in vivo. The PACT-guided microrobotic system designed by Wu et al. has achieved controlled propulsion and prolonged cargo retention in vivo of NPs with a diameter of 50 μm [127]. Although the current resolution and deep penetration of PACT are still insufficient, it is superior to conventional imaging equipment (CT, X-ray, MRI) in terms of NPs imaging positioning.
- (iii)
Difficulty of degrading in the human body
Although NPs are made of high biosafety materials, there is still a risk of damages to liver, kidney, and other organs if they stay in the body for a long time and cannot be degraded or excreted The use of materials that will be disintegrated after near-infrared light irradiation to fabricate NPs may be a solution to this problem. Recently, more and more NPs have been produced by these materials. Such NPs mediate PTT while loading drugs, meanwhile, the substances produced by the disintegration of NPs can be rapidly metabolized by the human body. In addition, the use of more biocompatible and degradable materials for nanoparticle preparation is also a solution. For example, the surface of chitosan is positively charged and can be broken down by the colonic flora, which facilitates interaction with specific tissues and can be metabolized by the body. The biocompatibility and degradability of chitosan has been proven to be non-toxic at appropriate drug concentrations [128].
- (iv)
Difficulty in avoiding mononuclear phagocytic system (MPS)
In biofluids, NPs will adsorb proteins to form a corona layer referred to as “protein corona” in a broader sense giving biological identity to NPs and alters their biological characters, which will attract MPS especially macrophages to uptake NPs [129]. In order to avoid being uptaken by MPS, various polymer coatings such as forpolyether, polybetaine (PB) and polyolhave were investigated to cover NPs. For example, polyglycerol-grafting NPs are able to evade macrophage uptake by reducing protein adsorption [130]. In addition, there are two types of tumor-associated macrophages (TAM), M1 and M2. M1 macrophages inhibit tumor growth while M2 macrophages promote tumor growth. Therefore, no longer avoiding macrophages, but designing NPs targeted by macrophages, by regulating the function of macrophages, and even using macrophages as new drug carriers to exert anti-tumor effects may become a novel solution. At present, common design strategies for such NPs include inhibiting macrophage recruitment, depleting TAM, reprogramming TAMs, and blocking CD47-SIRPα pathway [131]. Among them, following the design concept of reprogramming or blocking CD47-SIRPα pathway, NPs that repolarize M2 macrophages to M1 type have made a breakthrough in vivo experiments [132].
Considering the above difficulties and referencing to advanced researches, we come up with a new possible design of NPs. The NPs skeleton is made of pyrolytic material (spirulina, exosomes, et al.). Then, photothermal materials (Au, Pd, etc.) are deposited on the NPs skeleton through electroless plating. After that the superparamagnetic iron oxide will be loaded on the surface of NPs through the sol–gel method. Then, suitable polymers (polybetaine, polyglycerol, etc.) will coat the NPs. Finally, drug (like doxorubicin) will be loaded on the NPs. Afterwards, under the guidance of PACT, NPs will be injected into the upstream of tumor supplying blood vessel, and the tumor will be irradiated with NIR. At the same time, three-dimensional magnetic field control is given to maximize the accumulation of NPs at the tumor site. Through this design, a large number of NPs will accumulate at the tumor site to ensure the drug concentration and PTT effect. At the same time, most NPs will be decomposed at the tumor site, and only a small number of NPs will circulate in the body.
Nowadays, anti-tumor therapy with NPs as the main body is still in the exploratory stage, and related technologies and equipments need to be invented, so it is unlikely to be clinically used in the short term. However, NPs can change part of the function or structure of many actual technologies. The upgrade of actual technologies is expected to be applied in clinic quickly, which contributes to upgrading the diagnosis and treatment of tumors in consequence. For example, NPs can help to develop electrochemical devices based on the interaction between ions and conductive polymers, such as organic electrochemical transistors (OFETs), electrolyte gated field-effect transistors (FETs), fin field-effect transistor (FinFETs), tunneling field-effect transistors (TFETs), electrochemical lab-on-chips (LOCs) [133]. These electrochemical devices are widely used in various tumor testing and diagnostic equipment. The use of NPs can help improve the accuracy of the equipment and reduce the detecting time. Many studies indicate that medical equipment using electronic components upgraded by NPs have been applied clinically [133,134,136].
Based on the evidence cited above, future research of NPs may not only focus on NPs themselves but also consider a feasible administration and efficacy assessing platform. In addition, the platform needs to be able to monitor immunotoxicity, the long-term toxicity, and neurotoxicity of NPs. As nanotechnology develops, if these problems were solved, NPs would be an ideal approach to upgrade cancer therapy and diagnosis.
데이터 및 자료의 가용성
All data generated or analysed during this study are included in this published article.
약어
- NPs:
-
나노입자
- PDT:
-
Photodynamics therapy
- PTT:
-
Photothermal therapy
- SPR:
-
Plasmon resonance effect
- Au NRs:
-
금 나노막대
- SI-ATRP:
-
Surface-initiated atom transfer radical polymerization
- NIPAAM:
-
N-isopropylacrylamide
- US:
-
초음파
- MSNs:
-
Mesoporous silica nanoparticles
- USMO:
-
Ultrasmall manganese oxide
- GEM:
-
Gemcitabine
- OINPs:
-
Oxygen/indocyanine green-loaded lipid nanoparticles
- PA:
-
Photoacoustic
- MPI:
-
Magnetic particle imaging
- MRI:
-
자기공명영상
- SPIO:
-
Superparamagnetic iron oxide
- USPIO:
-
Ultra-small SPIO
- OCT:
-
Optical coherence tomography
- MMOCT:
-
Magnetomotive optical coherence tomography
- mAb:
-
Monoclonal antibody
- DOX:
-
독소루비신
- 5-FU:
-
5-Fluorouracil
- FA:
-
엽산
- PTX:
-
파클리탁셀
- ROS:
-
활성 산소 종
- EPR:
-
Enhanced permeability and retention effect
- EGFR:
-
Epidermal growth factor receptor
- BHC:
-
Berberine hydrochloride
- AFP-1:
-
Antifreeze protein
- PCMs:
-
Phase change materials
- 3DPCT:
-
3D printed coplanar template
- RCDs:
-
Amino-rich red emissive carbon dots
- COF:
-
Covalent organic framework
- ICG:
-
Indocyanine green
- HSA:
-
Serum albumin
- MDR:
-
Multidrug resistance
- MRP1:
-
Multidrug resistance-associated protein 1
- p-gp:
-
P-glycoprotein
- 추신:
-
Photosensitizing substances
- UC:
-
Up-conversion
- RT:
-
Radiotherapy
- PLGA:
-
Poly(lactic-co-glycolic acid)
- PACT:
-
Photoacoustic computed tomography
- MPS:
-
단핵 식세포 시스템
- PB:
-
Polybetaine
- TAM:
-
Tumor-associated macrophages
- OFETs:
-
Organic electrochemical transistors
- FETs:
-
Electrolyte gated field-effect transistors
- FinFETs:
-
Fin field-effect transistor
- TFETs:
-
Tunnelling field-effect transistors
- LOCs:
-
Electrochemical lab-on-chips