나노물질








나노 기술의 급속한 발전으로 새로운 유형의 형광 나노 물질(FNM)이 지난 20년 동안 등장했습니다. 나노미터 규모는 FNM에 바이오이미징 및 형광 의존적 검출의 응용 분야에서 중요한 역할을 하는 고유한 광학 특성을 부여합니다. 그러나 형광 나노 물질의 낮은 선택성과 낮은 광발광 효율은 이미징 및 검출에서의 응용을 어느 정도 방해하기 때문에 과학자들은 여전히 더 나은 특성을 가진 새로운 FNM을 합성하는 방법을 찾고 있습니다. 이 리뷰에서는 반도체 양자점, 탄소점, 탄소 나노 입자, 탄소 나노 튜브, 그래 핀 기반 나노 물질, 귀금속 나노 입자, 실리카 나노 입자, 형광체 및 유기 프레임 워크를 포함한 다양한 형광 나노 입자를 요약합니다. 우리는 최근 몇 년 동안 FNM의 합성 및 생물 의학 분야에서의 응용 분야의 최신 개발의 최근 발전을 강조합니다. 또한, FNM의 합성 및 응용의 주요 이론, 방법 및 한계를 검토하고 논의했습니다. 또한 합성 및 생물 의학 응용 분야의 과제도 체계적으로 요약되어 있습니다. 임상 응용 분야에서 FNM의 미래 방향과 전망도 제시됩니다.
기존의 유기 염료는 세포 독성 및 낮은 생체 적합성과 같은 고유한 결함으로 인해 생물 의학에 적용하는 데 몇 가지 어려움에 직면해 있습니다[1]. 그러나 형광 나노 물질의 출현은 기존의 유기 염료를 대체할 수 있는 큰 잠재력을 보여줍니다. 과학자들은 형광 나노 물질 연구에 많은 시간과 노력을 쏟아 부었고 합성 및 응용 분야의 관련 성과는 고무적입니다.
형광 나노 물질의 모양, 크기 및 구조는 물리적 및 화학적 특성을 결정하며 성능에 큰 영향을 미칩니다. 따라서 형광 나노 물질의 제어 가능한 합성은 뜨거운 연구 주제가되었습니다. 최적의 합성 실험 조건은 형광 나노 물질의 가장 적합한 크기, 형태 및 안정성에 기여합니다. 최근에는 합성법을 개선하여 형광성 나노물질의 생체적합성을 향상시키기 위한 많은 노력이 이루어지고 있다[2]. 과거 금속 이온은 일반적으로 탄소점(CD) 또는 양자점(QD)으로 도핑되어 형광 나노 물질의 표면을 기능화했습니다. 그러나, 비효율적인 형광과 근본적인 독성은 바이오이미징 및 바이오라벨링에서의 적용에 위협이 되었습니다[3]. 이러한 문제를 고려하여 Zuo et al. 고효율 CD 유전자 전달 시스템을 보고했습니다. 불소가 도핑된 CD는 용매열 공정에 의해 합성되었으며 유전자 전달을 위한 양전하 부위는 분지형 폴리에틸렌이민(b-PEI)에 의해 제공될 수 있다[4]. 향후 새로운 표면 개질 방법이 핫스팟 연구 영역이 될 것으로 예상할 수 있습니다.
그림 1과 같이 생체 영상, 생체 검출 및 일부 치료 방법을 포함하는 생물 의학 응용 분야에서 형광 나노 물질의 잠재력을 탐구하기 위해 많은 노력이 있었습니다. 응용에 대한 신뢰할 수 있는 형광은 물리적 및 화학적 특성에 따라 다릅니다[5]. 따라서, 독성, 친수성, 생체적합성 등의 특성을 개선하기 위한 연구는 의생명 분야에서 형광 나노물질의 광범위한 활용을 실현하는데 중요한 역할을 해왔다. 암과 같은 일부 질병의 발병률이 증가함에 따라 환자의 정확도와 순응도가 높은 새로운 진단 및 치료 전략에 대한 요구가 증가하고 있습니다[6]. 현재 금속 또는 비금속 이온 도핑과 형광성 나노물질의 표면 개질은 PL 효율과 생체적합성을 향상시키는 데 여전히 지배적인 기술이며[7], 해당 연구는 형광성 나노물질의 생물의학 응용에 대한 새로운 비전을 제시하고 있습니다.
<그림>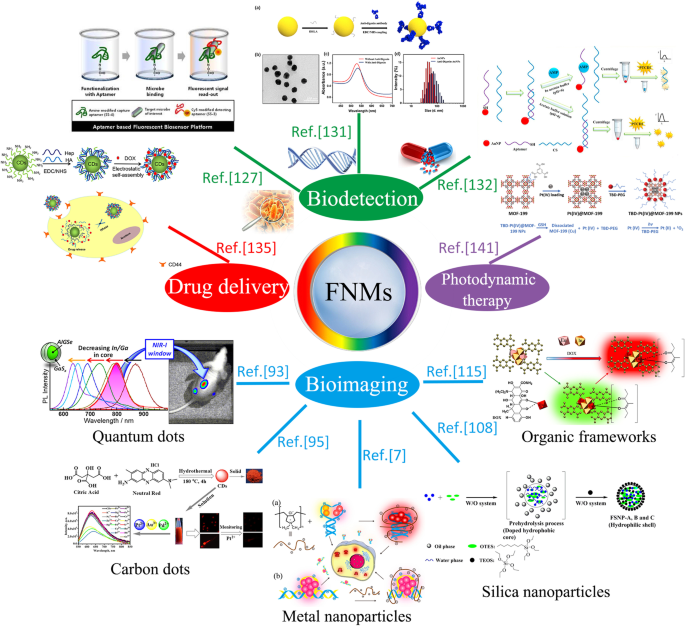
형광 나노 물질의 생물 의학 응용의 개요 다이어그램
형광 나노 물질이 생물 의학 분야에서 가지고 있는 큰 잠재력을 고려하여, 이 리뷰는 최신 발전과 개선에 중점을 둡니다. 과학자들은 형광 나노물질 표면의 기능화와 생물 의학 응용 분야에서의 성능에 전념해 왔습니다. 합리적으로 설계된 합성 전략을 통해서만 형광 물질은 생물 의학 분야에서의 응용에 필수적인 높은 PL 효율과 우수한 생체 적합성을 부여할 수 있습니다. 형광 물질의 합성과 응용에 대한 이 리뷰가 독자들이 현재 형광 나노 물질의 일반적인 개발 동향을 이해하는 데 약간의 도움이 되기를 바랍니다.
양자점(Quantum Dot, QD)은 광범위한 흡수 및 대칭 광발광 스펙트럼, 높은 양자 수율, 광표백에 대한 높은 내성, 높은 몰 흡광 계수 및 큰 유효 스톡 이동으로 인해 지난 수십 년 동안 연구 장소였습니다[8]. QD의 형성 메커니즘 측면에서 전하 캐리어(전자 및 정공)가 특정 영역에 대한 전위 장벽에 의해 제한될 때 반도체는 극적인 양자 크기 효과를 나타내어 흡수 스펙트럼과 형광 스펙트럼의 이동을 초래합니다. 작은 영역은 전하 캐리어의 드 브로이 파장보다 작거나 동등하게 나노결정 직경은 벌크 재료에서 여기자의 보어 반경의 두 배 미만입니다[9]. 전하 캐리어가 3차원 공간의 전위 장벽에 의해 제한될 때 QD가 형성되며 주로 II-VI족(CdSe, ZnS), III-V족(GaAs, InP) 또는 IV-VI족(PbS, PbSe).
QD의 합성은 1982년에 처음 보고되었습니다[10, 11]. 반도체의 나노 결정 및 미세 결정은 유리 매트릭스에서 성장되었습니다. 형광 물질의 개발과 함께 양자점은 직접 흡착법, 링커 보조 흡착법, situ법 및 이전 준비 방법의 조합과 같은 다양한 방법으로 준비되었습니다. 기존 방법의 조합에는 준비된 반도체와 QD 전구체의 조합 및 미리 준비된 QD와 반도체 전구체의 조합이 포함되며, 여기서 반도체 또는 QD를 별도로 준비합니다[12].
QD 합성에 대한 일련의 연구 끝에 많은 연구자들이 QD의 형광 특성 연구를 보고했습니다. Bawendi et al. QD의 크기 의존적 광학적 특성을 조사하기 위해 황화카드뮴(CdS), 셀렌화카드뮴(CdSe) 또는 텔루르화카드뮴(CdTe)과 같은 반도체 전구체를 도입하여 좁은 크기 분포의 양자점을 합성했습니다[13]. 그 이후로 CdSe는 QD의 가장 일반적인 화학 조성이 되었으며 다양한 표면 변형[14,15,16] 또는 보호 무기 쉘[13, 17]이 콜로이드 안정성을 제공하는 데 사용되었습니다.
탄소점(CD)은 2004년 전기영동에 의한 단일벽 탄소 나노튜브(SWCNT)의 정제에서 처음으로 얻은 10nm 미만의 크기를 가진 나노카본 계열의 새로운 나노물질입니다[18]. CD는 물에 대한 높은 용해도, 낮은 세포 독성, 높은 광안정성, 여기 의존적 다색 방출, 바람직한 표면 변형 유연성, 우수한 세포 투과성 및 더 나은 생체 적합성을 근거로 점차적으로 반도체 양자점을 대체한다는 점에 주목해야 합니다[19, 20]. 일반적으로 CD는 주로 탄소 양자점(CQD)과 그래핀 양자점(GQD)으로 구성됩니다. 조정 가능한 크기의 CD에 대한 합성 방법의 덩어리는 화학적 방법과 물리적 방법의 두 가지 주요 그룹으로 크게 나눌 수 있습니다[21].
화학적 합성 방법은 생성된 CD가 우수한 수용해도, 화학적 불활성, 낮은 독성, 기능화 용이성 및 광표백 저항성과 같은 우수한 특성을 갖기 때문에 탄소 도트 제조에 가장 일반적으로 사용됩니다. 일반적으로 화학적 합성 방법에는 전기화학적 합성[22, 23], 산성 산화[24, 25], 열수 탄화[26], 마이크로파 보조/초음파 처리[27,28,29], 용액 화학 방법[30], 지원되는 합성 [31] 등
수많은 합성 방법 중에서 전기화학적 합성은 지난 수십 년 동안 반복적으로 보고되었습니다. Zhao의 그룹은 전기산화 합성에 의해 세포독성이 낮은 CD를 제조하는 새로운 방법을 보고했습니다. 여기서 CD는 NaH2에서 Pt 와이어 상대 전극을 사용하여 포화 칼로멜 전극에 대해 흑연 컬럼 전극을 산화시켜 CD를 제조했습니다. PO4 수용액 [22]. 그런 다음 상층액을 원심 필터 장치를 통해 한외여과하여 각각 청색 및 황색 형광을 갖는 CD를 얻었다. Qu et al.은 인산염 완충 용액에서 그래핀 전극의 전기화학적 산화에 의해 3-5 nm의 균일한 크기를 갖는 GQD에 대한 또 다른 직접적인 전기화학적 접근을 최근 보고했습니다[23]. 이 입자의 광발광(PL) 색상은 녹색이었습니다.
Mao et al. 2007년에 양초 그을음과 산화제를 혼합한 후 환류, 원심분리 및 투석을 거쳐 CD를 정제하는 연소 산화 합성을 완료했습니다. 준비된 CD의 광발광 스펙트럼은 415(보라색)에서 615nm(주황-적색) 범위의 방출 피크 파장과 함께 넓은 색상 범위를 가지고 있습니다. 그 다음, 얻어진 CD를 폴리아크릴아미드 겔 전기영동에 더 적용하여 광학적 특성이 다른 CD를 분리하였다. 산성 산화는 또한 탄소 점과 같은 안정적인 나노 물질의 제조를 위해 광범위하게 사용되었습니다. 탄소 나노튜브/흑연의 산 처리 및 환류 후 생성된 3-4nm의 CD는 자외선 아래에서 밝은 노란색 형광을 방출하고 식염수에서 매우 안정한 황갈색 투명한 액체를 나타냈습니다. 이로 인해 장파(노란색/주황색/빨간색) 형광이 있는 CD가 더 나은 투과성을 갖게 되었습니다. CD 용액은 실온에서 장기간 보존할 수 있으며 형광성을 잃는 침전물이 형성되지 않습니다[25].
마이크로파/초음파 합성은 점차적으로 합성 과정에서 보조 합성 기술이 되었습니다[32]. 직경 3~5nm의 형광 CD는 경제적이고 신속하며 친환경적인 마이크로웨이브 지원 접근 방식을 통해 Xiao 그룹에 의해 합성되었습니다[33]. 이 1단계 접근법의 가장 두드러진 특징은 처음으로 이온성 액체에서 파생된 마이크로파 열분해를 통해 CD의 형성과 기능화가 동시에 완료되었다는 것입니다[34]. 반응 과정은 탄소원으로 값싼 이온성 액체를 사용하는 전자레인지에서 발생하였으며, 반응 시간이 경과함에 따라 용액은 무색에서 암갈색으로 변하였다[35]. Tanget al. 단분산된 수용성 CD를 합성하기 위해 탄소원으로 포도당 또는 활성탄을 기반으로 한 초음파 방법을 사용했습니다. 그들은 밝고 화려한 형광을 방출했습니다[28]. 유사하게, Vanesa Romero et al. 야채에서 탄수화물의 광화학적 산화 후 형광성이 높은 질소(N)와 황(S)이 함께 도핑된 탄소점(CD)을 얻습니다. N과 S의 공동 도핑은 CD 표면의 활성 사이트 수를 증가시켜 발광 성능을 향상시킵니다[36]. 형광 프로브인 질소 도핑된 탄소 양자점(NCQD)은 독시사이클린 측정에 성공적으로 적용되었습니다[37]. Pathaket al. 마이크로웨이브 열수법에 의해 티오우레아와 트리스-아세테이트-에틸렌디아민 완충액으로부터 합성된 질소 및 황으로 공동 도핑된 탄소점(NSCD)도 준비했습니다. NSCD는 다색 형광측정법으로 인해 다양한 병원성 박테리아와 인간 협측 상피 세포를 이미지화하는 데 사용되었습니다[38].
위에서 언급한 합성 방법의 대부분은 강산, 몇 가지 복잡한 실험 단계, 그리고 CD의 수용해도를 개선하고 광발광 특성을 향상시키기 위해 다른 화합물에 대한 추가 수정이 필요하다는 점을 고려하여 일부 연구팀은 다음과 같은 탄수화물 광발광의 열수 탄화를 이용했습니다. 복잡하고 시간 소모적인 정제 및 기능화 과정을 피하기 위해 키토산, 포도당, 구연산 등. Yang et al. 온화한 온도에서 키토산의 열수 탄화에 의해 7.8%의 양자 수율(QY)을 갖는 고도로 아미노 기능화된 형광 CD를 위한 1단계 합성 방법을 설명했습니다. 이 방법은 강산 용매나 표면 부동태화 시약이 필요하지 않았습니다. 게다가, CD 표면의 작용기는 수용성을 향상시키고 잠재적인 생물독성을 감소시켰다[26]. 밝고 색상 조정 가능한 발광을 갖는 다중 도핑된 탄소 점(MCD)은 추가 표면 패시베이션 없이 원 포트 방법으로 합성되었습니다. 합성된 MCD는 풍부한 생체 원소(O, N, P)로 도핑되어 강력한 형광 방출 및 여기 파장 의존 특성, 우수한 수용해도, 높은 광학 안정성 및 이온 안정성을 나타냅니다. MCD는 Fe 3+ 를 선택적으로 민감하게 감지할 수 있을 뿐만 아니라 15.9nm에서 청색광 검출, 세포 내 Fe 3+ 도 측정 다색 형광 이미징을 통해 [40].
용액 화학 방법의 경우 지난 수십 년 동안 아릴 그룹의 산화 축합이 GQD 준비에 성공적으로 적용되었습니다. Li의 그룹은 가용화 전략을 사용하여 원하는 크기와 구조의 안정적인 콜로이드성 GQD를 생성했습니다. 이 방법은 비실용적인 크기 분리 프로세스 없이 CD의 크기 조정 가능성과 좁은 크기 분포를 달성했습니다[30]. 지원되는 합성 절차와 관련하여 많은 연구팀이 이를 활용하여 나노 크기의 CD와 같은 단분산 나노 물질의 합성을 완료했습니다. Zhu의 그룹은 나노 반응기로 메조다공성 실리카(MS) 구를 채택하고 탄소 전구체로 시트르산을 채택하고 1.5-2.5nm 크기의 친수성 CD를 함침 방법으로 준비했습니다. 23%의 높은 광발광 효율을 갖는 CD는 강한 청색 발광을 방출할 수 있고 우수한 변환 발광 특성을 나타낼 수 있다[31]. 밝은 노란색 방출 탄소 점(Y-CD)은 Yan et al.에 의해 준비되었습니다. 용매열법을 통해 무수 구연산을 탄소원으로, 2,3-페나진디아민을 질소원으로 사용합니다. 카르복실기가 풍부한 Y-CD는 상당한 형광 양자 수율(24%), 188-nm Stokes' 이동, 높은 감도 및 우수한 안정성을 나타냅니다[41]. CD의 합성 방법 및 특성은 표 1에 나와 있습니다.
일반적으로 물리적 합성 방법에는 주로 아크 방전, 레이저 제거/패시베이션 및 플라즈마 처리가 있습니다. Xu와 동료들은 HNO3로 아크 방전 매연을 산화시켰습니다. 그런 다음 겔 전기 영동에 의해 현탁액을 SWCNT로 분리했습니다. 그들은 마침내 고형광성 탄소점 나노입자의 빠르게 움직이는 밴드를 분리했다[18]. 나노 탄소 재료를 전구체로 사용하고 친환경 용매를 액체 매질로 사용하는 CD는 Li et al. 가벼운 레이저 절제 접근을 통해 [44]. 또한 Gokus와 동료들은 산소 플라즈마를 사용하여 단일층 그래핀에 강한 형광을 유도할 수 있음을 입증했습니다[45].
감소된 세포독성, 광표백 저항성 및 증가된 생체적합성을 갖는 형광 탄소 나노입자는 생체영상 및 기타 생체의학 응용 분야에서 점점 더 많은 관심을 받고 있습니다. 1~6nm 이내의 일반적인 탄소점 크기에 비해 탄소나노입자의 크기는 20nm 이상으로 분리, 정제, 수집의 수고를 덜어준다[46]. 탄소 나노 입자의 합성 방법은 열수 탄화, 마이크로파 처리, 화학적 ablation 방법 및 laser ablation을 포함하여 탄소 점과 유사합니다. 이들 방법은 나름대로의 장점이 있지만 나노입자의 크기를 효과적으로 제어할 수는 없다. 전기화학적 탄화는 탄소 나노 입자의 크기와 발광 특성을 제어할 수 있는 단일 단계 방법입니다. 불행히도, 이 방법에 사용할 수 있는 기질은 극소수에 불과합니다. 현재 오산화인 연소 방법과 같은 몇 가지 흥미로운 새로운 방법이 보고되었습니다[47].
최근 몇 년 동안 생물 의학 응용에 적합한 탄소 나노 입자는 변형 된 방법으로 합성됩니다. Santu et al. Resorcinol의 탄화를 제어하여 고품질의 적색 형광 탄소 나노 입자의 합성을 해결했습니다[48]. 이 접근법은 탈수와 관련된 산화 페놀 커플링을 포함하여 적색 형광 탄소 나노 입자를 형성합니다. Anaraet al. 수정된 열수법을 사용하여 6.08%의 양자 수율로 형광 탄소 나노 입자를 합성했습니다. 이 방법은 몇 시간까지 긴 열처리가 필요한 기존의 방법에 비해 반응 시간을 30분 미만으로 단축하여 형광 탄소 나노 입자의 빠른 합성을 실현했습니다[46].
1차원(1D) 탄소나노튜브는 우수한 전자적, 광학적 특성으로 인해 생물의학 분야에서 큰 주목을 받고 있다. 탄소나노튜브는 원통형 그래핀 층의 수에 따라 단일벽 탄소나노튜브(SWCNT)와 다중벽 탄소나노튜브(MWCNT)로 나눌 수 있다. SWCNT가 실린더로 말려진 단일 층의 그래핀 시트로 구성되는 반면, MWCNT는 그래핀 시트의 여러 동심원 층으로 구성됩니다. 탄소나노튜브의 외경은 100nm 미만이지만 길이는 수 밀리미터에 이를 수 있어 종횡비가 매우 높고 표면적이 넓습니다[49]. 더욱이, 탄소 나노튜브의 탄소 원자의 독특한 배열은 나노튜브 외부의 풍부한 π-전자 접합을 형성합니다[50]. 또한 탄소나노튜브는 NIR 영역에서 강한 흡수와 형광을 나타낸다[51]. 이러한 모든 특성은 생체 분자와의 효과적인 상호 작용에 기여하여 탄소 나노튜브를 생물 의학 응용 분야에 이상적인 후보로 만듭니다.
합성 방법은 탄소나노튜브의 직경, 길이, 구조, 키랄성 및 품질에 큰 영향을 미치며, 한편 이 방법이 대규모 생산에 적합한지 여부를 고려해야 합니다. 일반적으로 사용되는 방법에는 아크 방전[52], 레이저 절제[53] 및 화학 기상 증착[54]이 있습니다. 또한 탄소 나노튜브는 용해도를 개선하고 용매 및 생물학적 매체에서 응집되는 것을 방지하기 위해 기능화되어야 합니다. 공유 기능화는 탄소 나노튜브의 구조에 결함을 도입하여 NIR 형광의 극적인 감소 또는 심지어 완전한 손실을 초래합니다. 폴리머와 같은 양친매성 분자를 사용한 비공유 기능화는 탄소 나노튜브의 구조와 형광 특성을 보존하지만 탄소 나노튜브의 QY를 낮춥니다. 이러한 장애물을 극복하기 위해 최근 탄소나노튜브를 합성하고 기능화하는 새로운 방법이 보고되고 있다. Lee et al. 환원제인 dithiothreitol을 첨가하면 처음으로 SWCNT의 형광 QY를 향상시켜 QD와 동등한 밝기를 갖는 형광단을 생성할 수 있다고 보고했다[55]. Hou et al. 다양한 계면활성제로 기능화된 SWCNT에 디티오트레이톨을 첨가하는 것을 조사했습니다. DNA 및 SDS로 감싼 SWCNT의 경우 형광 QY가 크게 증가한 반면, 다른 계면활성제에서는 다른 정도의 형광 소광이 관찰되었습니다[56]. 결과적으로 DNA 또는 SDS로 포장된 SWCNT에 디티오트레이톨을 추가하는 것은 생물 의학에서 탄소 나노튜브를 적용하기 위한 실현 가능한 솔루션입니다.
2차원 탄소 나노물질로서 그래핀과 그 유도체는 생체 영상 및 약물 전달과 같은 다양한 생물 의학 응용 분야에서 널리 연구되었습니다. 그래핀 나노물질은 그래핀 나노시트, 그래핀 옥사이드(GO) 및 환원그래핀 옥사이드(rGO) 나노시트를 포함한다. 그들은 염료 분자, 생체 분자 및 수불용성 약물과 비공유 상호 작용을 허용하는 높은 표면적과 독특한 표면 특성을 가지고 있습니다. 2004년 처음으로 성공적으로 제조된 이후 많은 연구자들이 다양한 그래핀 제조 방법을 보고했습니다. 그래핀 나노 물질의 합성 방법은 하향식과 상향식의 두 가지 범주로 분류할 수 있습니다.
하향식 방법은 기계적 박리[57], 용매 기반 박리[58] 및 전기화학적 박리[59]를 포함하여 적층된 흑연 층으로부터 그래핀 시트를 형성하기 위한 분리를 포함합니다. Gu et al. 초음파 보조 용매 기반 각질 제거를 체계적으로 연구한 결과 초음파가 좋은 각질 제거 효과가 있음을 발견했습니다. 그들은 또한 제어 가능한 합성을 가능하게 하는 그래핀 시트의 크기와 두께 분포에 영향을 줄 수 있습니다. 상향식 접근법은 대체 탄소원을 사용하여 탄소 원자를 재구성하는 것을 포함합니다. 에피택시 성장[60]과 화학 기상 증착(CVD)[61]은 가장 일반적으로 사용되는 상향식 합성 방법입니다. 많은 sp 2 로 구성된 GO 시트 산소 함유 그룹에 의해 분리된 도메인은 Hummer의 방법을 사용하여 합성할 수 있습니다. 이 sp 2 의 다양한 크기 도메인은 GO 시트의 PL을 500~800nm 범위로 광범위하게 만듭니다[62]. rGO는 하이드로퀴논 및 하이드라진과 같은 환원제를 사용하여 화학적 환원을 통해 GO에서 파생됩니다. GO와 비교하여 rGO의 형광은 UV 영역에서 형광 소광과 함께 청색 이동 방출을 나타냈으며, 이는 새로 형성된 결정질 sp 2 사이의 침투 경로에 기인합니다. 클러스터 [63]. Akbari et al. sp 3 의 비율이 /sp 2 GO 시트의 도메인은 형광 스펙트럼을 결정합니다. 따라서 GO는 다양한 환원 정도에서 광범위한 파장에 걸쳐 유망한 형광 나노물질이며, 이는 생물의학 응용 분야에 사용될 수 있습니다.
귀금속 원자는 동시에 양자점에 비해 세포 독성이 적습니다. 금, 은, 구리 나노입자에 대한 관심이 높아지고 있으며 많은 분야에 적용되고 있습니다. 생물의학 분야에서 광발광 방출 또는 플라즈몬 공명과 같은 금 나노입자의 양자역학적 효과는 금 나노입자(AuNP)를 세포독성이 낮은 또 다른 생체내 나노센서의 이상적인 후보로 만듭니다[64, 65].
AuNPs는 합성의 용이성과 독특한 특성으로 인해 광범위한 과학적 관심을 끌었으며 다양한 합성 방법이 보고되었습니다. 가장 중요한 방법 중 하나로서 화학적 방법은 일반적으로 안정제 존재하에서 클로로아우레이트 수용액을 환원제로 처리하여 수행된다. 시트르산은 안정제와 환원제로 작용할 수 있는 가장 널리 사용된다[66]. 그러나 시트르산으로 안정화된 AuNP는 티올레이트 리간드로 기능화 개발 중에 비가역적 축적을 겪을 수 있습니다. 이 문제는 더 높은 안정성을 제공하고 나노입자 응집을 방지하는 데 도움이 되는 수용성 고분자, 계면활성제 또는 캡핑제의 존재하에 반응이 일어나도록 함으로써 극복할 수 있습니다. AuNPs의 크기와 모양은 gold-citrate 비율, 표면 개질제 또는 반응 조건을 변경하여 제어할 수 있습니다. 원 포트 초음파 유화 방법으로 Zhang과 그의 동료들은 Bis(4-(N-(2-naphthyl) phenylamino) phenyl)-fumaronitrile과 AuNP를 마이셀에 공동 로딩하여 나노 프로브를 얻었다[67]. 무엇보다 얻은 나노프로브는 생체내 종양표적 영상화 및 진단에 활용 가능성이 매우 높아 금 나노입자가 존재함에도 불구하고 우수한 형광 영상화 능력을 처리했다. AuNPs는 특정 실험 조건에서 독성이 없지만 독성 및 부작용에 대해 철저히 조사해야 합니다[68].
형광 Ag 나노클러스터는 독특한 물리적 및 화학적 특성으로 인해 많은 관심을 받아왔습니다. 이러한 나노클러스터의 합성 과정은 안정화 스캐폴드에 따라 DNA 올리고뉴클레오티드, 펩타이드, 단백질, 덴드리머 및 폴리머로 분류됩니다. 게다가, 광범위한 문헌은 D의 수성 줄기 추출물의 적용과 같은 일부 녹색 합성을 입증했습니다. 삼엽충 및 S. 알바 준비 조건을 최적화하기 위해 [69].
Cu 나노클러스터(Cu NCs)는 귀금속 재료로 비교적 널리 사용되지만 산화에 대한 취약성으로 인해 합성이 여전히 부족합니다. 최근 Kawasaki et al. 마이크로파 보조 폴리올 방법으로 안정적인 Cu NC를 성공적으로 준비했습니다[70]. DNA는 형광 Cu NC의 합성을 위한 템플릿으로 사용될 수 있습니다. Mohir et al. 고 선택성으로 Cu NC를 얻기 위해 용액에서 이중 가닥 DNA를 기반으로 하는 방법을 제안했습니다[71]. Cu NC의 형광 특성을 사용하여 RDX의 선택적 결정을 위한 효과적인 형광 켜짐 신호 표시기로 성공적으로 활용되었습니다[72].
포함된 형광단의 투명도, 기계적 안정성, 견고성 및 안정화 특성을 고려하여 실리카 나노입자는 생물학적 영역에 광범위하게 적용됩니다. 예를 들어, Zn 2+ 의 세포내 검출을 위해 적용된 실리카 코어/쉘 NP 및 H2 PO4 - 살아있는 세포에서 "off/on" 형광 나노센서로 합성되었습니다. 최근에는 유기염료가 도핑된 실리카 나노입자가 합성되어 생체검출과 같은 많은 응용분야에 널리 사용되고 있다[73]. 실리카 나노입자 합성법 중 가장 널리 사용되는 방법은 Stöber법과 역마이크로에멀젼법이다. 1960년대에 처음 기술된 Stöber 방법[74]은 알킬 실리케이트의 가수분해와 암모니아 첨가에 의해 촉매되는 알코올 용액에서 규산의 후속 축합을 포함합니다. 두 번째 실리카 NP 형성 방법인 역 마이크로에멀젼 방법은 유중수 마이크로에멀젼의 물방울 내부에서 알킬 실리케이트, 일반적으로 TEOS의 반응을 포함합니다[75]. 그는 외. 3종 염료 도핑 실리카 나노입자를 Stöber 방법과 입자의 코어에 염료를 임베딩하여 역 마이크로에멀젼 방법으로 제조했습니다. Zn 2+ 에 기능적으로 반응하는 일부 분자 입자 표면에 증착됩니다[76]. 형광 실리카 나노 입자는 세포 내 Zn 2+ 형광 이미지에 사용되었습니다. (H2 PO4 - ) HeLa 세포에서. Zn 2+ 일 때 비례 Zn 2+ 에 추가되었습니다. 나노센서, 나노입자는 H2의 농도를 비례적으로 검출하는 능력을 보여주었습니다. PO4 - .
일반적으로 단분산성과 생체적합성이 좋은 실리카 나노복합체는 관능기로 쉽게 더 변형될 수 있다[77,78,79]. Lee et al. 자성 나노 입자 및 형광 염료를 실리카 나노 입자에 도핑. 이러한 실리카 나노복합체는 자기공명(MR) 및 형광 이미징을 위한 다중 모드 이미징 프로브뿐만 아니라 항암 약물 전달 운반체로도 사용될 수 있습니다[80]. 간단히 말해서, 실리카 입자는 이러한 경우에 크게 확장된 용도로 연구 장소가 될 수 있습니다.
형광체는 자가형광 및 조직의 광산란 간섭을 줄이는 독특한 이점으로 인해 생물 의학에서 널리 사용됩니다. 일반적으로 형광체는 호스트 물질과 도핑된 이온으로 구성됩니다[81]. 형광체의 호스트 재료 중 이트륨 산화물(Y2 O3 ) 낮은 광 내구성과 포논 에너지로 인해 유망한 것 이상입니다. 란탄족은 풍부한 전자 준위와 에너지 전달 채널을 고려하여 인광체에 주로 도핑됩니다. 열수[82], 화염 분무 열분해[83], 졸-겔[84] 및 공침 공정[85]을 포함하여 인광체의 제조를 위한 수많은 방법이 보고되었습니다.
열수 합성은 형광체 합성에 효율적이고 경제적인 것으로 입증된 이상적인 공정으로 떠오르고 있습니다. Yu et al. 합성 Y2 O3 :Eu 3+ 구연산나트륨이 있는 상태에서 열수법에 의한 형광체 [82]. 구연산나트륨의 농축액, 수열과정에서 첨가되는 NaOH 및 Eu의 양에 따라 얻어진 형광체의 특성이 결정되었다. 화염 분무 열분해는 산화물 기반 형광체의 신속하고 연속적인 합성을 위한 유망한 방법입니다. 이 방법은 기존의 방법에 비해 결정도가 높고 도펀트 분포가 균일한 형광체를 제공합니다. Khan et al. Tb 3+ 를 성공적으로 제작했습니다. -도핑된 Y2 O3 화염 분무 열분해를 사용하여 좁은 크기 분포를 가진 직경이 약 100nm인 형광체[83]. 그들의 방법에서 알칼리 염은 다른 금속 질산염 전구체와 혼합되어 좁은 범위에서 크기 분포를 효과적으로 제어했습니다. 졸-겔 합성 경로는 높은 균질성과 순도, 합성 시간 단축, 균일한 입자 형태 및 좁은 입자 크기 분포와 같은 여러 이점을 제공합니다[86]. Leonardo et al. Sm 3+ 획득 도핑된 SiO2 -Gd2 O3 졸-겔 공정에 의한 형광체 [84]. Co-precipitation is a common and simple method for synthesizing crystalline phosphors, which ensures high homogeneity and controlled morphology characteristics. Perhaita et al. reported that the phase composition of the phosphors strongly depends on the pH during the precipitation [85].
Covalent-organic frameworks (COFs) are new porous crystalline materials possessing outstanding stability, adsorption and low toxicity. The design of fluorescent small organic molecules with a combination of fluorescence determination methods can be used to construct more efficient nanoprobes [87]. For selective 2,4,6-trinitrophenol (TNP) determination, a novel Naphthalimide-Benzothiazole conjugate was prepared as colorimetric and fluorescent nanoprobe. The fluorescence emission peaks of receptor were selectively quenched by TNP with a limit of detection as low as 1.613 × 10 –10 M.
Metal organic frameworks (MOFs) are a kind of new generation multifunctional inorganic–organic materials with various holes and functionalized 3D crystalline structures formed by metal ions and linkers. MOFs show potential applications in separation, catalysis and other aspects due to unique attributes such as excellent chemical tenability, specific surface area and confinement of the pores. Some of the MOFs are luminescent and the quantum yield as well as light intensity will be influenced by temperature and excitation wavelength [88]. With the addition of doxycycline, Yu et al. synthesized a new functional metal–organic framework of pyromellitic acid and europium, which exhibited remarkable fluorescence enhancement at 526 nm and 617 nm. Results showed that both fluorescence intensities were positively correlated with the doxycycline concentration. The unique fluorescence response of the system could discriminate doxycycline from other tetracycline antibiotics with high selectivity.
Fluorescent nanomaterials have been widely used in bioimaging. Compared with conventional organic fluorescent molecules, fluorescent nanomaterials are equipped with many superior properties such as high photostability, tunable emission spectra and high quantum yields [89].
As early as 1998, QDs were first successfully applied in biological imaging [90]. Since then, applications of QDs in this field have been springing up gradually. Chen’s group applied it in bioimaging and nuclear targeting with great stability and biocompatibility in living cells [91]. In spite of the extremely high sensitivity and spatial resolution of QDs, poor performances on hydrophilicity and biocompatibility hindered their applications in bioimaging in vivo. To tackle this problem, it has been found that the water-solubility of QDs can be greatly improved by attaching thiol or other hydrophilic groups to the surface of quantum dots [92]. In the same way, with the intention of improving the effectiveness and specificity of in vivo targeted imaging, targeting molecules are attached to the surface of QDs. Furthermore, the wavelength region of the emission light can be controlled by altering the size of QDs.
The combination of QDs and inorganic metal ions can optimize the application of QDs in bioimaging because the QDs’ defect-site PL peaks will be utterly removed by controlling the proportion of doped inorganic metal ions. Kuwabata, S et al. modulated the degree of Ga 3+ doping in Ag–In–Se QDs. Thus, the QDs’ defect-site PL peaks were completely removed and a sharp band-edge emission peak come into appearance [93]. They found a blue shift of the band-edge PL peak ranging from 890 to 630 nm which could be credited to the fact that the energy gap of QDs was enlarged by Ga 3+ doping. After injecting a mouse with QDs, the potential of AIGSe@GaSx core–shell QDs for bioimaging turned out satisfying. The imaging effect of this kind of QDs in mice is demonstrated in Fig. 2. However, sensing of mid-IR wavelengths is challenging due to increased dark currents and noise. HgTe QDs synthesized by colloidal method is a promising candidate for IR bioimaging by virtue of lower dark currents, higher-temperature operation, and higher detectivity [94].
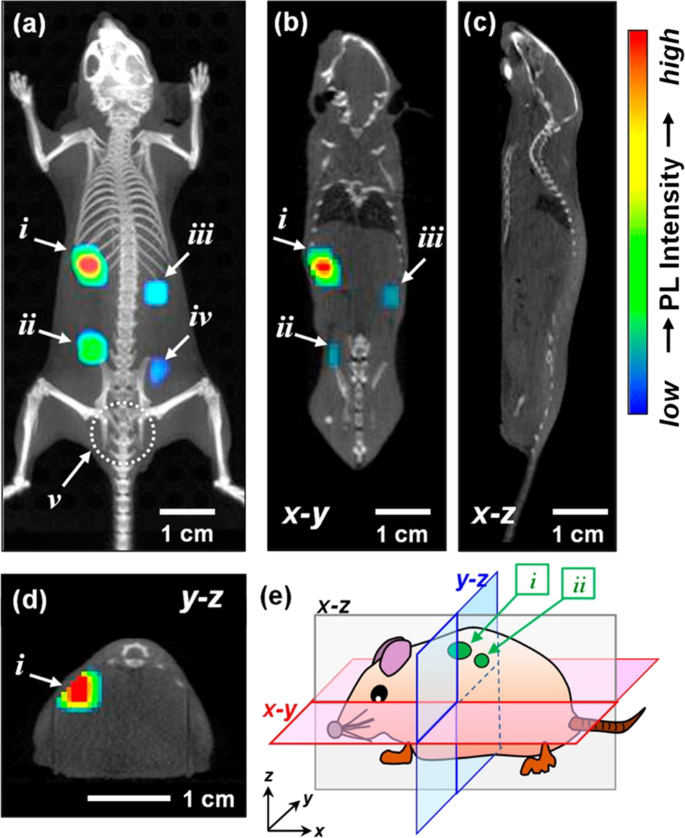
Three-dimensional PL image superimposed on an X-ray CT image of the mouse subcutaneously injected with DSPC-AIGSe@GaSx liposome dispersions (each 50 mm 3 ) in the back [78]
The poor photostability of current fluorescent nanomaterials hinders their long-term bioimaging to a large extent. To overcome this limitation, CDs have been studied for bioimaging and some positive results have been obtained due to the great performance on PL efficiency. Enormous efforts have been put to improve their water solubility and lower their toxicity in organisms. At present, most CDs are facing a barrier in bioimaging, that is, their short-wavelength excitation disables deep penetration in tissue. Aside from this, being exposed under the short-wavelength for a long time could do irreversible damages to living cells and tissues. As shown in Fig. 3, with the purpose of overcoming this deficiency, Gao et al. designed fluorescent CDs with red emission which were successfully used for bioimaging of noble metal ions (Pt 2+ , Au 3+ , Pd 2+ ) in cells and zebrafish [95]. Sun and co-workers first studied the near infrared (NIR) imaging of CDs in vivo using mice as a model. Recently, it was reported that molecules or polymers containing plentiful sulfoxide or carbonyl groups can enhance NIR fluorescence through the surface modification. As shown in Fig. 4, under NIR excitation, sulfoxide or carbonyl groups are bound to the outer layers and the edges of the CDs. Thus, electron transitions are promoted, influencing the optical bandgap [96].
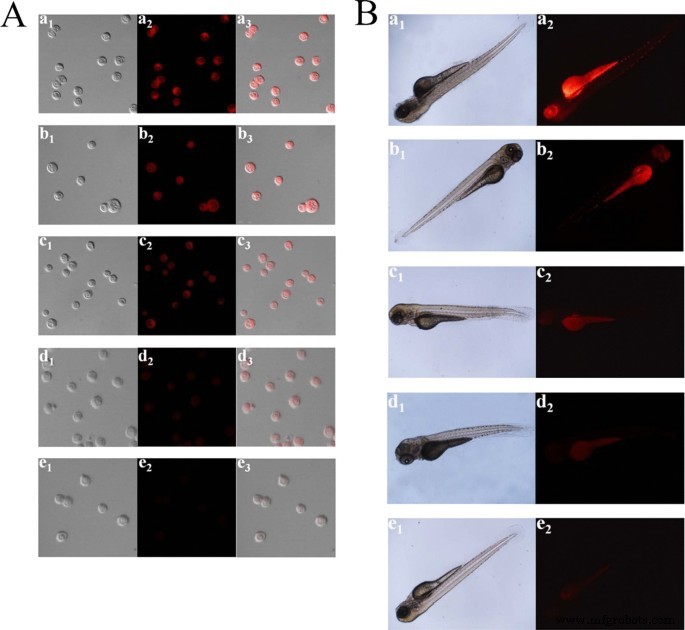
A Confocal imaging of Pt 2+ in PC12 cells. (a1–e1) Bright field images. (a2–e2) Black field images of the CDs in PC12 cells with the different concentrations of Pt 2+ (0, 25, 50, 150, and 300 μM). (a3–e3) Overlay images. B Fluorescence imaging of Pt 2+ in ZF. (a1–e1) Bright field images. (a2–e2) Fluorescence images of the CDs in ZF with the various concentrations of Pt 2+ (0, 30, 60, 100, and 150 μM) [80]
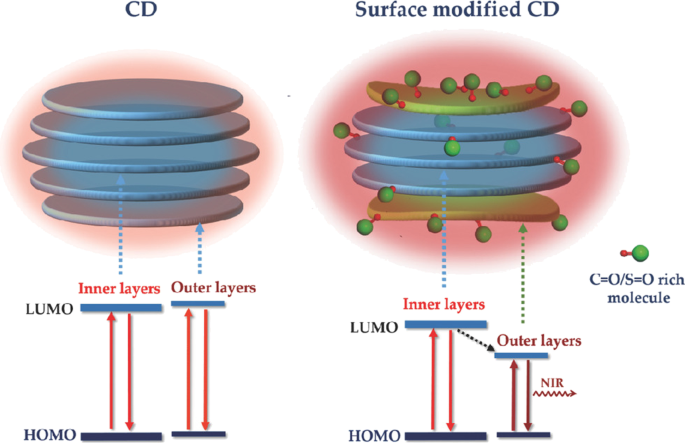
Schematic of structure and energy level alignments of nontreated CDs (left column) and CDs modified with S = O/C = O‐rich molecules (right column). The red (oxygen atom) and green double‐bonded balls represent the C = O/S = O‐rich molecule [81]
In the field of bioimaging, fluorescent carbon nanoparticles show unique chemical and optical properties over traditional fluorescence probes. Different size, shape and elemental composition make carbon nanoparticles with different features. The biomedical fields are always seeking the most promising fluorescent carbon nanoparticles. Gaurav et al. obtained both larger and smaller size carbon nanoparticles with laser ablation method [97]. Both green and blue fluorescence were observed in the cells incubated with the carbon nanoparticles, suggesting their different sizes. Cell viability results indicated that the prepared carbon nanoparticles were nontoxic and safe for bioimaging applications. Shazid et al. employed carbonization method to obtain fluorescenct carbon nanoparticles derived from biocompatible hyaluronic acid. Both the in vitro and in vivo bioimaging studies showed that the prepared carbon nanoparticles would be reliable and stable for opticle imaging. Moreover, based on the experimenal data, their cytotoxicity was proved to be tolerable for biomedical applications.
Fluorescence of carbon nanotubes in the NIR is attracting high attention for their good light penetration depth in biological tissues. However, their low quantum yield requires for considerable excitation doses, leading to a fair degree of blue-shift and failure of penetrating live tissue. Mandal et al. reported that bright and biocompatible p-nitroaryl functionalized SWCNTs, encapsulated in phospholipid-polyethylene glycol, are suitable for bioimaging applications. The prepared SWCNTs enabled high signal-to-noise ratio imaging in live brain tissues using ultra-low excitation intensities. Their 1160 nm emissions in the NIR guarantee that they will provide optimal fluorescence imaging results [98]. Ceppi et al. applied SWCNT-based fluorescence imaging to debulking surgery in an ovarian cancer mouse model. SWCNTs are coupled to an M13 bacteriophage carrying modified peptide binding to the SPARC protein, which is overexpressed in ovarian cancer, leading to real-time imaging to guide intraoperative tumor debulking. This imaging system enables detection in the NIR window with a pixel-limited resolution of 200 μm, demonstrating real potential in fluorescence imaging guided surguries for patients [99].
Furthermore, fluorescent moieties can be conjugated by a carbon nanotube backbone, which integrate strong fluorescent ability with robust mechanism strength, exhibiting ideal bioimgaing results. Katharina et al. functionalized SWCNTs with an amphiphilic C18 -alkylated polymer conjugated with bright perylene bisimide fluorophores. The polymers wrapping around the SWCNT backbones not only increase their water dispersibility but also promote their biocompatibility by providing a shield. In vitro studies on HeLa cells demonstrated that the biocompatibility of SWCNTs is dramatically improved. In microscopy studies, direct imaging of the SWCNTs' cellular uptake via perylene bisimide and SWCNT emission proved their potential for bioimging [100]. Park et al. combined carbon nanotubes with mussel adhesive proteins which can be specifically targeted at tumors in tissue. They then made carbon nanotubes conjugated with a ZW800 NIR fluorophore to obtain NIR fluorescence imaging [101]. The prepared carbon nanotube probes react with a specific tumor in one hour and can be easily eliminated via urine, demonstrating great value as tumor imaging and detecting agent.
Large surface area and feasible further functionalization make graphene-based nanomaterials a promising candidate for biomedical applications. However, as a result of their chemical sturctures, graphene nanosheets lack photoluminescence and rGO only display weak fluorescence, which makes it difficult to be utilized in bioimgaing applications. Many researchers attempted to resolve this problem by conjugation of fluorescent dyes and probes onto the large surface of graphene and its derivatives. Sun et al. reported an assembly strategy to prepare fluorescence probe RACD functionalized a single layer GO via π-π interaction and hydrogen bonding. The resluting nanomaterials exhibited that the fluorescent probes reduce the aggregation degree and acquire very well monodispersion, hydrophilicity and photostability, which is attributed to the strong synergy between RACD and GO [102]. Even so, fluorescence quenching remains a critical issue for these materials. In addition, the biocompatibility and toxicity of polymers applied to connect graphene-based materials and fluorescent moieties have not been adequately investigated. These facts appeal for alternative solutions to utilize graphene and its derivatives in bioimaging applications. Georgia et al. developed intrinsically photoluminescent graphene derivatives that show desirable biocompatibility and tunable fluorescence properties [103]. They can be organophilic or hydrophilic with different amine functionalization dodecylamine and hexamethylenediamine, respectively. The intrinsic fluorescent graphene-based nanomaterials possess great potential in a variety fileds of bioimgaing.
In recent years, fluorescent metal nanoparticles have shown great potential in bioimaging for improved disease diagnosis and treatment [104]. Gold is the most commonly used metal for bioimaging. The surface of AuNPs can be easily modified with various biomolecules such as peptides, proteins, antibodies, enzymes, and nucleic acids. These biomolecules can interact with specific cells or organelles in vivo, which makes it possible for AuNPs to be used for targeted optical imaging. Gao et al. reported a real-time in situ imaging of nucleus by AuNPs fabricated with bifunctional peptides constructed with both Au-binding affinity and nucleus-targeting ability. The bifunctional peptides showed strong binding affinity toward AuNPs and ensured good surface coverage of the nanoparticles, which made it stable and efficient for precise bioimaging of the nucleus in cells [105]. The Au-Se bond is considered as a better candidate than the Au–S bond to link the peptides and AuNPs due to the stronger ability against interference of intracellular thiol. Pan et al. prepared the Au-Se-peptide nanoprobes through a direct freezing process. The obtained nanoprobe was successfully applied to identify autophagy and apoptosis in chemotherapeutic drug treated cancer cells [106].
As a novel fluorescent imaging technology, DNA-templated silver nanoclusters (DNA-Ag NCs) have aroused the attention of many scientists due to their unique properties, especially the tunable fluorescence emission range relying on DNA sequences. However, the highly negatively charged DNA backbones have always been a great obstacle for the expansive applications in bioimaging because of poor stability as well as poor cell permeability in physiological environment. It is also noteworthy that the PL property and fluorescent efficiency of DNA-Ag NCs are far from satisfying. As a result, figuring out how to neutralize the negative charge on the surface of DNA strands is of great urgency for researchers. Recently, Lyu and co-workers successfully modified fluorescent DNA-Ag NCs with cationic polyelectrolytes via electrostatic force between the positively charged polyelectrolytes and the negatively charged phosphate groups of the DNA strands, leading to a threefold fluorescence intensity enhancement [7] (Fig. 5). Li et al. reported a facile strategy to make gold nanoclusters with positive charge and silver nanoclusters with negative charge form aggregates by electrostatic interactions. An incredible 40-fold fluorescence intensity enhancement was obtained. Results demonstrated that the physiological stability improved a lot and the cell permeability was also enhanced, which promises its practical applications in the future.
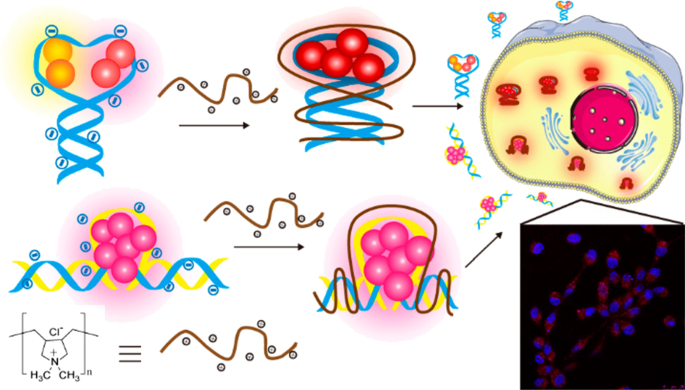
Formation of FL DNA–Ag NC–Cationic Polyelectrolyte Complexes for Cell Imaging [7]
Dye-doped fluorescent silica nanoparticles emerge with great potential for bioimaging as a novel and ideal platform for the monitoring of living cells and the whole body. The outer silica shell matrix protects fluorophores from outside chemical reaction factors as well as provides a hydrophilic shell for the inside insoluble nanoparticles, which renders the enhanced photo-stability and biocompatibility to the organic fluorescent dyes. Benefiting from the robust structure of silica matrices, dye-doped fluorescent silica nanoparticles have been presented with several superior properties including good biocompatibility, hydrophilic features, and high fluorescence intensity [107].
Jiao et al. also constructed a local hydrophobic cage in dye-doped fluorescent silica nanoparticles to improve their optical properties, which solves the problems of aggregation-caused quenching (ACQ) and poor photostability in aqueous media by organic fluorescence dyes benefiting from the robust structure of silica nanoparticles [108]. In addition, compared with free dyes, the fluorescent intensity both in water solution and living cells demonstrated a 12.3-fold enhancement due to the limitation of molecular motion, indicating a significant development for silica nanoparticles in biomedical applications. QDs have been developed for bioimaging both in vivo and vitro owing to their excellent optical qualities. However, a critical obstacle faced in QDs’ application in vivo is their poor biocompatibility. Inspired by the organic dye-conjugated silica-NPs, QDs-embedded silica-NPs have also been invented with the advantage that the excellent optical qualities of QDs can be retained, while the silica-NPs coat improves their biocompatibility to a large extent simultaneously. Darwish et al. reported that many QDs could be assembled around a central silica nanoparticle to form supra-NP assemblies. It was expected to be used for enhanced bioimaging because of their higher sensitivity and superior signal-to-background ratios [109]. There is reason to believe that silica-NPs conjugated with fluorescent nanomaterials with ideal optical properties will still be the dominant research interest in the future.
For bioimaging, the sizes of phosphors need to be controlled so that they are small enough to be integrated with living cells. Furthermore, the aggregation of particles should be avoided for biocompatibility. Hence, the control of both particle sizes and dispersity in an aqueous solution is essential for the bioimaging application of the phosphors. Atabaev et al. prepared Eu, Gd-codoped Y2 O3 phosphors which had a spherical morphology within the range 61–69 nm. Enhanced PL emission and low toxicity made these phosphors suitable for bioimgaing applications [110].
Upconversion nanomaterials are able to convert lower-energy near-infrared photons to higher-energy ones as emission. This anti-Stokes photoluminescence process will lead to low background noise, large tissue penetration depth, and low photo-damage in bioimaging applications [111]. Lanthanide-based phosphors are able to show upconversion emission owing to their photodurability and low phonon energy. Nallusamy et al. reported a NIR–NIR bioimaging system based on Er 3+ :Y2 O3 phosphors by using NIR emission at 1550 nm under 980 nm excitation, which can allow a deeper penetration depth into biological tissues than ultraviolet or visible light excitation [112]. In addition, the surface of Er 3+ :Y2 O3 was electrostatically PEGylated to improve the chemical durability and dispersion stability under physiological conditions. Thakur et al. synthesized Ho 3+ /Yb 3+ co-doped GdVO4 phosphors via a modified sol–gel method. The prepared phosphors showed brilliant red upconversion emission under NIR excitation, which may be useful in bioimaging of the biomolecules [113].
Careful selection of MOF constituents can yield crystals of ultrahigh porosity and high thermal and chemical stability, with some of them being luminescent [114]. Recently, Sava Gallis’s group described a novel multifunctional MOF material platform which showed a wide spectral region from 614 to 1350 nm covering the deep red to NIR region. Both porosity and tunable emission properties made them highly suitable for in vivo bioimaging [115]. What’s more, to overcome the obstacle of MOF’s low selectivity towards malignant tissues, Liu et al. developed a target-induced bioimaging by conjugating DNA aptamers using ZrMOF nanoparticles as quenchers [116]. Based on the quenching of ZrMOF nanoparticles, target-induced bioimaging is achieved upon binding with the target.
Since fluorescent nanomaterials can amplify the fluorescent signals significantly and be compatible with organisms, there is increasingly more research on their application in the rapid detection of biomolecules [117]. It will shorten the analysis time to a large extent if we are able to establish a real-time detection system by fluorescent nanomaterials. It has been discovered that multiple detection can be achieved by using QDs probes simultaneously [118, 119].
Pathogens have been an unignorable threat to human health for centuries and these include many types of microorganisms ranging from bacteria (pathogenic Escherichia coli, Salmonella, and Streptococcus pneumoniae ) and viruses (Coronavirus, Influenza virus and hepatitis virus ). However, conventional methods for pathogen detection still need improvement of detection limits and detection speeds. For their applications in detecting pathogens, Tan and co-workers reported a bioconjugated nanoparticle-based biodetection for in situ pathogen quantification, which cost less than 20 min [120]. Tan’s success promises that quick and convenient pathogen detection is possible and can be achieved with these ingenious nanomaterials in the future. Here, we list diverse pathogens detected by fluorescent nanomaterials as shown in Table 2 [119, 121,122,123,124,125,126,127,128,129].
Apart from pathogen detection, fluorescent nanomaterials have also aroused more and more interest of scientists in the detection of DNA. Owing to the merits that a number of biomolecules can be attached to the surface of fluorescent nanomaterials, the signal intensity of fluorescent nanomaterials in DNA detection can be enhanced significantly. Tan and co-workers developed an DNA detection method to detect gene products using bioconjugated dye-doped fluorescent silica nanoparticle with high sensitivity and photostability [130]. Although the analysis of nucleic acid has been successfully achieved by real-time nanomaterial fluorescence systems, there are still many shortcomings such as complex procedures or expensive instruments. To address these disadvantages, Wang’s group introduced a highly sensitive and visualized detection of nucleic acid by the combination of strand exchange amplification (SEA) and lateral flow assay strip (LFA) [131]. The system, which is possible to be widely used in areas requiring limited resource, is mainly characterized by integrating SEA with LFA (Fig. 6). There is no denying that the extremely high fluorescent signal for bioanalysis plays an irreplaceable role in these applications.
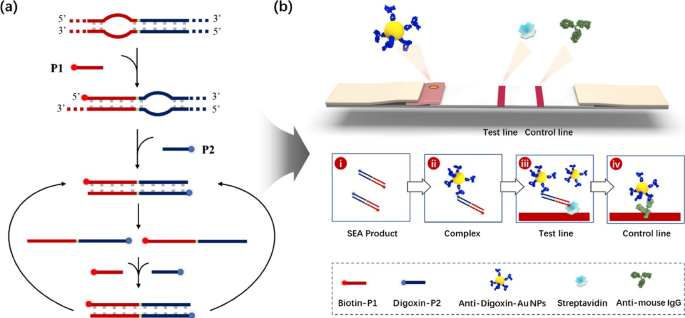
Schematic illustration of the SEA-LFA strip for the detection of nucleic acids [110]
In the field of drug analysis, a facile and low-cost analytical method is always in demand for high-speed detection of specific pharmaceutical compounds. Real-time detection of drugs can be achieved with selective and sensitive fluorescent nanomaterials owing to their outstanding optical properties. In the past decade, the modification of nanomaterials has lowered their detection limit and improved their detection accuracy significantly. Recently, it is reported that ampicillin can be detected in serum sample based on aptamer, its complementary strand (CS) and gold nanoparticles (AuNPs) [132]. The limit of detection (LOD) of this method can be as low as 29.2 pM. However, there are still many limitations in the detection of drugs or target molecules in vivo. Due to low selectivity, conventional fluorescent nanomaterials inevitably generate false positive results and adverse effects in vivo. In addition, current tracking systems can hardly realize real-time tracking because of insufficient labels and excitation sources. Considering the above limitations, a new method using up/down conversion (UC/DC) PL nanomaterials has attracted increasing attention. Seo et al. reported a single-photon-driven UC/DC system which demonstrated outstanding performance in the detection of heavy metal ion (i.e. Hg 2+ ) in mussels [133]. LOD of the nanohybrids was ca. 1 nM. This system is appealing to researchers in the field of fluorescent nanomaterials for biomedical applications.
Until now, the technology of treating cancers with high efficiency and targeting function is not perfect enough. Under most circumstances, the anticancer drugs are distributed and released extensively in the body, which endangers the healthy cells and tissues irreversibly. Currently, a large variety of carriers for drug delivery have been designed. However, we can hardly supervise the distribution and result of the whole delivery process. Benefiting from the recent development of the surface modification technique, fluorescent materials capped with polymers like polyethylene glycol (PEG) can bond with drugs strongly and firmly. Then, the loaded drugs will be released in response to certain conditions such as pH, osmotic gradient and the surrounding environment. However, it should be confirmed whether the drugs are transported to the specific site or not. It’s also necessary for us to consider more details such as how much of the drugs is released in different positions. Aside from being drug carriers, fluorescent nanomaterials can also demonstrate the consequences of intracellular uptake due to their fluorescence property. QDs have been applied to monitor some important properties, such as delivery efficiency, release rate and distribution of drug molecules in vivo, which are beneficial for scientists in order to understand the specific targeting pathways of drug delivery within living cells. Duan and co-workers reported a facile pH-responsive fluorescent CDs drug delivery system [134]. Loaded with dox which is effective for gastric cancer, intracellular drug delivery and tracking could be simultaneously realized in patients (Fig. 7). The report highlighted the ability of fluorescent CDs to label and track the drug delivery process for at least 48 h, which showed a great potential in bioimaging, biolabeling and traceable drug delivery. Duan et al. designed a pH and receptor dual-responsive drug delivery system [135]. Hyaluronic acid was covalently attached to the surface of CDs, and doxorubicin was loaded by electrostatic self-assembly. In the tumor microenvironment (pH 5.6), the drug is released rapidly from the drug delivery system, while in the normal physiological environment (pH 7.4), the drug is hardly released. Endocytosis occurs when the drug delivery system reaches CD44 which is a receptor rich in tumor cells and can bind specifically to the hyaluronic acid. In addition, carbon nanotubes can be used for drug delivery by virtue of their high loading efficiency. Strong π-π interactions play a critical role in binding therapeutic agents with carbon nanotubes, which can be broke through changing external conditions, resulting in the release of drugs in specific position. Pennetta et al. functionalized single and multi-walled carbon nanotubes with a pyrrole derived compound to form a doxorubicin stacked drug delivery system. Biological studies showed that the synthesized nano-conveyors can effectively deliver the drug into cell lines and improve the therapeutic effects of doxorubicin [136].
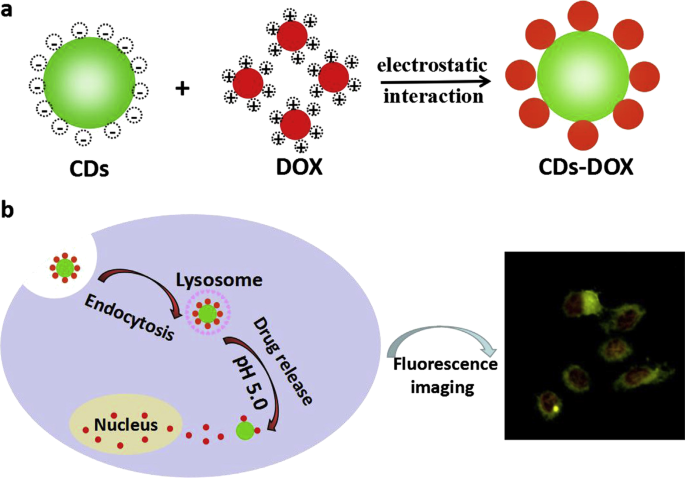
Schematic illustration of the preparation (a ) and cellular uptake (b ) of the CDs-DOX drug delivery system [113]
Photodynamic therapy (PDT) is a novel therapy method for tumors which utilizes the interaction between light and photosensitizer. In PDT, reactive oxygen species (ROS) is produced from oxygen by photosensitizers in the condition of specific wavelengths of light (mostly in the area of near infrared light). The specific mechanism is presented in Fig. 8. ROS includes singlet oxygen, superoxide radicals, hydrogen peroxide, and hydroxyl radicals that possess strong cytotoxicity which cause significant destruction of tumor cells. However, there exist many defects such as limited penetration depth [137], hydrophobic properties [138], photobleaching [139], complicated procedure [140], and tumor hypoxia. PDT agents can hardly be dissolved and they will disperse extensively in vivo once they are taken, making it impossible to be targeted and selected. Fluorescent nanomaterial based photodynamic therapy developed fast in recent years [141]. Combined with the unique properties that QDs possess, such as high fluorescent efficiency and great spectral resolution, the effect of PDT can be enhanced. Barberi-Heyob, M and coworkers significantly enhanced the photodynamic efficiency with a concentration of 8 nM because of the light dose-dependent response [142]. In addition, photodynamic therapy can sometimes do harm to the skin and eyes of patients due to its photosensitive side-effect. To alleviate these adverse effects, a novel nanoparticle-based drug carrier for photodynamic therapy is reported which can provide stable aqueous dispersion of hydrophobic photosensitizers. Meanwhile, the key step of photogeneration of singlet oxygen was preserved, which is necessary for photodynamic action [143]. It is obvious that QDs combined photodynamic therapy will replace the conventional PDT someday.
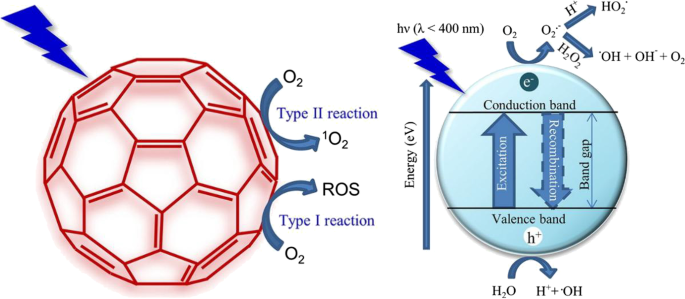
Schematic illustration of producing reactive oxygen species (ROS) for the photodynamic therapy (PDT) [119]
In the synthesis process, the diameter and size distributions of FNMs can be hardly distributed uniformly due to the agglomeration of small particles. This could be fatal to the optical properties of FNMs in biomedical application. For this reason, the applications of FNMs are still at the laboratory scale. It has been confirmed that the surface properties primarily determine the agglomeration state of the nanoparticles and their size. Therefore, surface modification is promising to achieve uniform distribution of FNMs by altering their surface properties [144]. To date, silanized QDs have been widely used because the polymerized silica coating increases the stability in buffers under physiological conditions [145]. Carbon dots synthesized by hydrothermal reaction using water-soluble base were reported to be difficult to control the size and distribution of grain boundary [146]. Khanam et al. reported a facile and novel synthetic method for the preparation of hydroxyl capped CDs using an organic base and a surfactant (Triton X-100) to modify the surface. A narrow particle size distribution at 7.2 nm was found in Raman and DLS studies, which is smaller than the majority of the particles falling within the range of below 10 nm in diameter [147].
Fluorescence quantum yield plays a crucial role for FNMs in their efficiency for on-demand light emission. Tunable and highly fluorescent CDs can be prepared with the surface functionalization approach. Nitrogen-doped FNMs are reported to have improved fluorescence quantum yield. With increasing nitrogen content, fluorescence quantum yield can be increased to as high as 56% at high synthesis temperature [148]. A facile strategy was also developed to tune the photoluminescent properties of CDs using a microwave irradiation, with citric acid and nitrogen-containing branched polyethyleneimine (b-PEI) as precursors. At intermediate levels of b-PEI, the CDs produced a high photoluminescence yield [149]. Lin et al. explored carbon dots with a high-fluorescence quantum yield rate synthesized from L-cysteine and citric acid by the microwave-assisted method. The obtained carbon dots exhibited a high-fluorescence quantum yield (up to 85%), which is due to the combination of amidogens and sulfydryl with carbon dots, and henceforth bringing the improved fluorescence property [150]. The above examples demonstrate that nitrogen or other electron-rich atoms like sulphur can obtain satisfying fluorescence quantum yield.
Fluorescent molecules can emit light with high efficiency in dilute solution. However, in concentrated solution or solid state, their fluorescence will be weakened or even disappear. This phenomenon is called Aggregation-Caused Quenching (ACQ) [151]. This problem has been puzzling scientists for almost 150 years, thus hindered the extensive application of fluorescent dyes.
In order to make effective use of fluorescent dyes, scientists have attempted many methods. Most of them focused on reducing the concentration of fluorescent dyes to prevent ACQ effect. Tang et al. discovered the phenomenon of Aggregation-Induced Emission (AIE) [152]. Based on rationally designed molecules, the fluorescence of organic molecules in solid state can be attained. Still, for more than one hundred thousand different fluorescent dyes in the world, the problem of ACQ has not been completely resolved. As long as they aggregate together, ACQ will make them lose their fluorescent properties.
It is almost impossible for high concentration or solid state FNMs to show reliable fluorescence due to fluorescence quenching. Although fluorescence quenching can be used as a sensitive signal to indicate substrate concentration in analytical chemistry, [153] in the most circumstances, however, fluorescence quenching is undesirable for FNMs because it always has considerable influence on bioimaging and biodetection. To overcome this long-standing problem, Benson et al. reported a universal solution with the discovery of a class of materials called small-molecule ionic isolation lattices (SMILES) [154]. SMILES are simple to make by mixing cationic dyes with anion-binding cyanostar macrocycles. We draw inspiration from their findings and believe that similar results can be obtained if we replace cationic dyes with cationic modified FNMs.
Although FNMs realized the great-leap-forward from in vitro imaging to in vivo imaging, the emission fluorescence of most of FNMs is distributed in ultraviolet region or short wavelength visible region, which limits the optical imaging in living organisms. Moreover, use of UV light for monitoring living processes in cells and tissues has some potential drawbacks as long‐term irradiation of living cells may cause DNA damage and cell death. Therefore, the development of FNMs in near-infrared region is urgently needed in the future. Although NIR FNMs have deep tissue penetration, NIR detectors and filters are needed as the excitation and emission wavelengths are too close to each other, which restricts their range of application.
Almost all biological tissues will produce significant autofluorescence under short wavelength, UV and visible light radiation [155]. Autofluorescence reduces the signal‐to‐background ratio and often interferes seriously with the visual effects. Some substances in the substrate of biological tissues also have great influence on the fluorescence, which reduces the selectivity of FNMs significantly. Until now, although the application of FNMs in mice showed acceptable outcomes, it is still difficult to achieve similar results in larger mammals. Much higher luminous efficiency under low power density excitation is required to avoid the background signal interference. Furthermore, temperature and pH conditions of the biological environments strongly affect the fluorescence of some substances as well. Therefore, satisfying fluorescence of FNMs at 37 °C and physiological pH should be guaranteed. It's worth noting that the pH in tumor is lower than normal tissues. Hence, fluorescence with high selectivity in acid environment will improve the efficiency of FNMs.
Biocompatibility refers to materials or systems that are nontoxic, safe and not causing physiological or immunological reactions. QDs with unique quantum confinement effect and electro-optical properties are attractive for biomedical applications. However, toxic effects of traditional semiconductor QDs made of heavy metal ions have serious safety concerns for their undesired environmental or health effects. In the purpose of circumventing this problem, core–shell structure modification of QDs by using biocompatible ligands or polymers is one way to effectively minimize toxic effects of traditional QDs. Furthermore, scientists are searching for heavy metal-free QDs formulations. Non-toxic or less toxic carbon dots and silica nanoparticles have shown their potential as the ideal FNMs for biomedical applications. Impurities brought in the process of syntheses may influence the biocompatibility of fluorescent nanomaterials. In order to reduce the influence of toxic impurities, green synthesis methods have been arousing the interest in biomedical fields. Chowdhury et al. utilized cacao extract which is a natural product as a reducing and stabilizing agent in the synthesis of gold nanoparticles [156]. Oxalic acid, as a constituent of cacao, can reduce Au 3+ in HAuCl4 to metallic gold and stabilize the resultant nanoparticle colloidal solution. In vitro studies suggested that the cacao derived gold nanoparticles are biocompatible and suitable for biomedical applications. For MOFs, appropriate metal ions and ligands must be selected to lower the toxicity. Wang et al. employed Fe, Ti and Zr as constituents of MOFs, which are harmless and even beneficial elements to the body [157]. In vitro studies indicate that the proposed material has good biocompatibility and safety in biomedical application. What’s more, it is necessary to consider whether the difference in composition, surface charge, or modified group will have different biological effects. Taking these factors into account, we can improve the biocompatibility of FNMs with rational design.
Benefiting from the unique properties of fluorescent nanomaterials, some limitations and barriers of conventional materials and methods in biomedical applications can be broken through. In this review, we comprehensively present the synthesis methods and applications of fluorescent nanomaterials. The advanced synthesis methods can offer us the fluorescent nanomaterials with ideal morphology, size ranges and structures. Meanwhile, the more convenient syntheses can lower the manufacturing cost of fluorescent nanomaterials, which is critical to their widespread applications in biomedical fields. Based on the improved synthesis techniques, the performance of fluorescent nanomaterials is bound to leap in their applications. With the development of fluorescent nanomaterials, bioimaging, biodection, drug delivery and photodynamic therapy will be more widely applied in the diagnosis and treatment of diseases. Finally, challenges in synthesis and biomedical applications point out exiting questions and developing direction. We hope that this review can bring some new insights to the development of fluorescent nanomaterials.
All data and materials are available without restrictions.
Fluorescent nanomaterials
Photoluminescence
Carbon dots
Quantum dots
Branched polyethyleneimine
Single-walled carbon nanotubes
Carbon quantum dots
Graphene quantum dots
Nitrogen-doped carbon quantum dots
Nitrogen and sulfur doped carbon dots
Quantum yield
Multi-doped carbon dots
Multi-walled carbon nanotubes
Graphene oxide
Reduced graphene oxide
Chemical vapor deposition
Gold nanoparticles
Ag nanoclusters
Cu nanoclusters
Nanoparticles
Tetraethylorthosilicate
Magnetic resonance
Covalent-organic frameworks
2,4,6-Trinitrophenol
Metal organic frameworks
Aggregation-caused quenching
Near infrared
Strand exchange amplification
Lateral flow assay strip
Complementary strand
Limit of detection
Upconversion
Downconversion
Photodynamic therapy
Reactive oxygen species
Aggregation-induced emission
Small-molecule ionic isolation lattices
나노물질
캘리포니아 및 해외 가구 제조업체는 이러한 변화를 활용하기 위해 새로운 가구 산업 환경을 형성하는 새로운 트렌드를 인식해야 합니다. 라이프스타일의 변화로 인한 미국 소비자의 구매 선호도의 근본적인 변화는 가구 제조업체에 새로운 도전 과제가 될 수 있지만 적응하려는 사람들에게는 새로운 기회의 문을 열 수도 있습니다. 이러한 변화하는 산업 동향을 이해함으로써 가구 제조업체는 행동 변화를 활용하여 비즈니스를 성공으로 이끌 수 있습니다. 빠른 링크: 현재 가구 제조 산업 분석 최신 가구 제조 과제 가구 제조업체를 위한 솔루션 CMTC로
3D 레진 프린팅은 모든 유형의 사용자가 사용할 수 있을 때까지 3D FDM 프린팅과 동일한 방식으로 발전했습니다. 3D 레진 프린터 사용을 통한 이러한 새로운 움직임은 광범위한 레진 개발로 이어졌습니다. 매우 다양한 특성과 용도를 가지고 있습니다. 이 기사에서는 기존 수지의 유형 및 용도를 설명하고 명확히 하려고 합니다. 3D 수지 프린터용(SLA, DLP, LED/LCD, LFS 등). 수지의 종류 대부분의 사용자는 FDM 기술 내의 재료 유형에 대해 잘 알고 있지만 3D 레진 프린팅을 시작할 때 일반적으로 레진 유형에 대한