샘플의 결정 구조는 10° ~ 80°의 2θ 범위에 걸쳐 실온에서 X선 회절(XRD, UltimaIII, 회절계 Cu-Kα 방사선, 40kV, 40mA, 일본 리가쿠)에 의해 스캐닝을 통해 확인되었습니다. 8° 분의 속도
−1
. LiCrx의 형태 Ni0.5−0.5x Mn1.5−0.5x O3.95 F0.05 시료는 주사전자현미경(SEM, Hitachi, S-3400N, Japan)으로 측정하였다. 얻어진 물질의 미세구조 및 원소 조성은 EDS(Energy Dispersive Spectroscopy)가 장착된 투과전자현미경(TEM, Tecnai G2 F20, FEI)으로 관찰하였다.
결과 및 토론
그림 1은 LiNi0.5의 XRD 패턴을 보여줍니다. Mn1.5 O4 및 LiCrx Ni0.5−0.5x Mn1.5−0.5x O3.95 F0.05 (x =0.025, 0.05, 0.075) 재료. 패턴은 Cr
3+
및 F
-
화합물이 도핑된 물질은 도핑되지 않은 샘플과 동일한 회절 피크를 나타내어 샘플이 불순물 상 없이 합성되었으며 Cr
3+
및 F
-
복합 도핑은 스피넬 결정 구조를 변경하지 않습니다. 불순물 피크 또는 상부 구조 피크가 발견되지 않아 Ni
2+
, Mn
4+
, Mn
3+
, 그리고 O
2−
스피넬 상의 원자가 Cr
3+
으로 성공적으로 대체되었습니다. 및 F
-
. Cr
3+
의 회절 피크 강도 -도핑된 LiCrx Ni0.5−0.5x Mn1.5−0.5x O3.95 F0.05 샘플이 감소하고 과도한 도펀트 농도가 결정화도에 영향을 미쳤습니다. LiNi0.5의 격자 매개변수 Mn1.5 O4 및 LiCrx Ni0.5−0.5x Mn1.5−0.5x O3.95 F0.05 (x =0.025, 0.05, 0.075) 재질은 Jade5.0으로 계산하였으며, 그 결과는 Table 1과 같다.
<그림><그림><소스 유형="이미지/webp" srcset="//media.springerature.com/lw685/springer-static/image/art%3A10.1186%2Fs11671-017-2172-z/MediaObjects/ 11671_2017_2172_Fig1_HTML.gif?as=webp"> 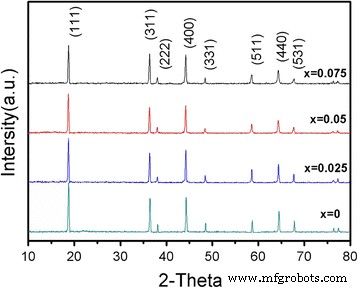
LiNi0.5의 XRD 패턴 Mn1.5 O4 및 LiCrx Ni0.5−0.5x Mn1.5−0.5x O3.95 F0.05 (x =0.025, 0.05, 0.075)
<그림>
그림 2는 LiNi0.5의 SEM 이미지를 보여줍니다. Mn1.5 O4 및 LiCrx Ni0.5−0.5x Mn1.5−0.5x O3.95 F0.05 (x =0.025, 0.05, 0.075) x10000 배율. LiNi0.5 Mn1.5 O4 샘플은 균일한 서브미크론 크기의 입자로 구성되며 결정은 준팔면체 모양을 갖습니다. Cr
3+
이후 및 F
-
복합 도핑, LiCrx Ni0.5−0.5x Mn1.5−0.5x O3.95 F0.05 (x =0.025, 0.05, 0.075) 시료는 높은 결정성 입자와 팔면체 모양과 날카로운 모서리와 모서리를 가진 전형적인 스피넬을 나타냈습니다.
<그림><그림><소스 유형="이미지/webp" srcset="//media.springerature.com/lw685/springer-static/image/art%3A10.1186%2Fs11671-017-2172-z/MediaObjects/ 11671_2017_2172_Fig2_HTML.gif?as=webp"> 
LiCrx의 SEM 이미지 Ni0.5−0.5x Mn1.5−0.5x O3.95 F0.05 .(아 ) x =0, (b ) x =0.025, (c ) x =0.05, (d ) x =0.075
스피넬 LiCr0.05에 크롬과 불화물의 존재 Ni0.475 Mn1.475 O3.95 F0.05 화합물은 그림 3과 같이 EDS로 확인되었습니다. 결정 형태와 격자 무늬의 TEM 및 고해상도 TEM(HRTEM) 이미지는 그림 4에 나와 있습니다. 두 LiNi0.5 Mn1.5 O4 및 LiCr0.05 Ni0.475 Mn1.475 O3.95 F0.05 유사한 표면 형태를 보였다. LiNi0.5에 대한 격자 무늬 사이의 거리 Mn1.5 O4 스피넬의 (111) 평면에 해당하는 0.4835nm로 측정되었습니다. 도핑 후, 그림 4d의 격자 간격은 0.4811nm의 값을 나타내며, 이는 Cr-O의 더 높은 결합 에너지가 스피넬 프레임워크를 수축시킬 수 있음을 나타냅니다. 따라서 LiCr0.05 Ni0.475 Mn1.475 O3.95 F0.05 리튬 저장을 위한 우수한 전기화학적 특성을 가질 것으로 예상됩니다.
<그림><그림><소스 유형="이미지/webp" srcset="//media.springerature.com/lw685/springer-static/image/art%3A10.1186%2Fs11671-017-2172-z/MediaObjects/ 11671_2017_2172_Fig3_HTML.gif?as=webp"> 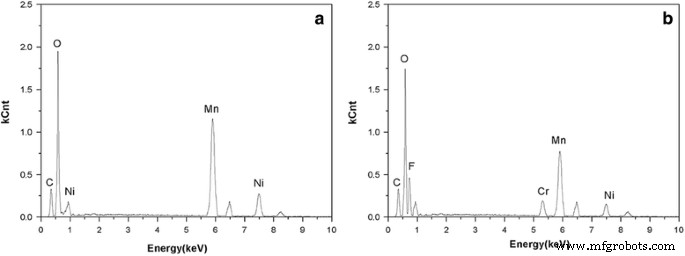
LiNi0.5의 EDS 패턴 Mn1.5 O4 (아 ) 및 LiCr0.05 Ni0.475 Mn1.475 O3.95 F0.05 (b )
<그림><그림><소스 유형="이미지/webp" srcset="//media.springerature.com/lw685/springer-static/image/art%3A10.1186%2Fs11671-017-2172-z/MediaObjects/ 11671_2017_2172_Fig4_HTML.gif?as=webp"> 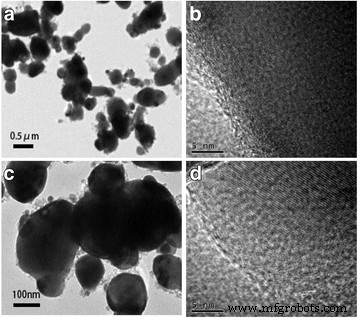
LiNi0.5의 TEM 및 HRTEM 이미지 Mn1.5 O4 (아 그리고 b ) 및 LiCr0.05 Ni0.475 Mn1.475 O3.95 F0.05 (ㄷ 그리고 d )
그림 5는 LiNi0.5의 충방전 곡선을 보여줍니다. Mn1.5 O4 및 LiCrx Ni0.5−0.5x Mn1.5−0.5x O3.95 F0.05 (x =0.025, 0.05, 0.075) 샘플, 여기서 셀은 0.1C의 비율로 3.5–5.0V의 전위 범위에서 테스트되었습니다. LiNi0.5의 방전 비 용량 Mn1.5 O4 및 LiCrx Ni0.5−0.5x Mn1.5−0.5x O3.95 F0.05 (x =0.025, 0.05, 0.075) 샘플은 141.59, 139.38, 134.18 및 124.47mAh g
−1
였습니다. 각각 0.1C에서 도핑된 샘플의 충전/방전 곡선은 약 4.7 및 4.1V에서 두 개의 명백한 전압 안정기로 구성되었습니다. 약 4.7V에서 전압 안정기는 Ni
2+
에 기인합니다. /Ni
4+
산화환원 커플, 약 4.1V의 작은 전압 안정기는 F
-
의 대체로 인한 것일 수 있습니다. O
2−
용 , 음전하의 양을 줄이고 전이 금속의 원자가를 변경했습니다(Mn
4+
Mn
3+
으로 감소했습니다. ) 전하 균형을 유지하기 위해.
<그림><그림><소스 유형="이미지/webp" srcset="//media.springerature.com/lw685/springer-static/image/art%3A10.1186%2Fs11671-017-2172-z/MediaObjects/ 11671_2017_2172_Fig5_HTML.gif?as=webp"> 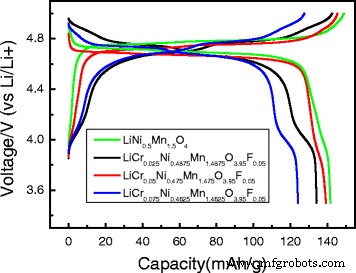
LiNi0.5의 충전/방전 곡선 Mn1.5 O4 및 LiCrx Ni0.5−0.5x Mn1.5−0.5x O3.95 F0.05 (x =0.025, 0.05, 0.075) 0.1C
속도 기능은 리튬 이온 배터리에서 매우 중요합니다. LiNi0.5의 사이클링 성능 곡선 Mn1.5 O4 및 LiCrx Ni0.5−0.5x Mn1.5−0.5x O3.95 F0.05 (x =0.025, 0.05, 0.075) 다양한 속도의 샘플이 그림 6에 나와 있습니다. 0.1 C에서 가장 높은 비방전 용량은 LiNi0.5에서 관찰되었습니다. Mn1.5 O4 (141.59mAh g
−1
), 두 번째로 높은 방전 용량은 LiCr0.025에서 관찰되었습니다. Ni0.4875 Mn1.4875 O3.95 F0.05 (139.38mAh g
−1
). 그러나 0.5, 2, 5 및 10C의 다른 높은 비율에서 LiCr0.05의 비방전 용량 Ni0.475 Mn1.475 O3.95 F0.05 128.70, 123.62, 119.63, 97.68mAh g
−1
가 가장 높았습니다. , 각각. 도핑되지 않은 경우 LiNi0.5 Mn1.5 O4 2C의 속도로 방전되면 특정 방전 용량의 감쇠가 더 분명합니다. 방전율 5C에서는 재료의 구조가 심하게 손상될 수 있습니다. Cr
3+
의 도핑량 및 치환 증가하면 사이클링 안정성이 증가합니다. 도핑량이 많을수록 재료의 비방전 용량이 줄어들어 4.1V 안정기가 더 명확해지고 배터리의 에너지 밀도가 감소합니다. 한편, 낮은 레이트에서 작은 편광으로 인해 편광 효과는 도핑 전후에 거의 차이를 보이지 않았다. 그러나 도핑 후 활물질의 양이 감소하여 비용량이 감소하였다. 한편, 고속에서 큰 분극과 향상된 리튬 이온 확산 계수로 인해 도핑된 LiNi0.5 Mn1.5 O4 음극은 더 높은 비용량을 나타냈다. 이 결과는 적절한 양의 Cr
3+
, F
−
공동 도핑은 우수한 사이클링 안정성과 속도 용량으로 이어질 수 있습니다.
<그림><그림><소스 유형="이미지/webp" srcset="//media.springerature.com/lw685/springer-static/image/art%3A10.1186%2Fs11671-017-2172-z/MediaObjects/ 11671_2017_2172_Fig6_HTML.gif?as=webp"> 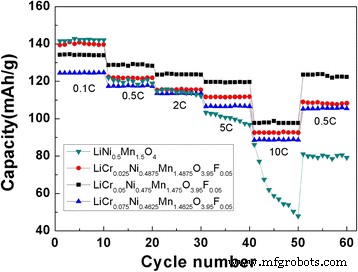
LiNi0.5의 사이클링 성능 Mn1.5 O4 및 LiCrx Ni0.5−0.5x Mn1.5−0.5x O3.95 F0.05 (x =0.025, 0.05, 0.075) 다른 비율
그림 7은 LiNi0.5의 사이클링 성능을 명확하게 보여줍니다. Mn1.5 O4 및 LiCr0.05 Ni0.475 Mn1.475 O3.95 F0.05 2C에서 50주기 후 샘플. LiCr0.05의 초기 방전 용량 Ni0.475 Mn1.475 O3.95 F0.05 및 LiNi0.5 Mn1.5 O4 123.62 및 114.77 mAh g
−1
, 각각 LiCr0.05 Ni0.475 Mn1.475 O3.95 F0.05 도핑되지 않은 LiNi0.5보다 초기 방전 용량이 더 높음 Mn1.5 O4 . 결과적으로 LiCr0.05 Ni0.475 Mn1.475 O3.95 F0.05 121.02mAh g
−1
의 가역 방전 용량을 제공할 수 있습니다. LiNi0.5 동안 50 사이클 후 97.9%의 용량 유지 Mn1.5 O4 가역 방전 용량만 106.24mAh g
−1
유지 92.6%의 용량 유지. LiCr0.025의 용량 보유 Ni0.4875 Mn1.4875 O3.95 F0.05 및 LiCr0.075 Ni0.4625 Mn1.4625 O3.95 F0.05 각각 95.0과 94.5%로 LiCr0.05 Ni0.475 Mn1.475 O3.95 F0.05 모든 샘플 중에서 높은 비율로 우수한 용량 유지력을 가지고 있습니다. 도핑된 물질은 Ni-O와 Mn-O의 결합 에너지보다 강하고 스피넬 구조를 안정화시키는 Cr-O의 결합 에너지로 인해 더 높은 용량 유지율을 갖는다. 또한, F
-
의 전자 용량을 점유 Ni, Mn, Cr과 결합한 후 더 강하고 안정하여 스피넬 구조의 안정성을 향상시켰다. 한편, 도핑은 또한 전해질 용액에서 HF에 의한 재료의 부식과 사이클링 과정에서 활성 물질의 비가역적 손실을 감소시켰다. Wang et al. [30] LiNi0.4 Cr0.15 Mn1.45 O4 139.7mAh g
−1
의 가역 방전 용량을 제공할 수 있습니다. 40주기 후 97.08%의 용량 유지에 해당합니다. Li et al. [31] LiNi0.5의 초기 방전 용량 보고 Mn1.5 O3.9 F0.1 0.1, 0.5, 1, 2, 5 C에서 129.07, 123.59, 118.49, 114.49, 92.57mAh g
−1
, 각각.
<그림><그림><소스 유형="이미지/webp" srcset="//media.springerature.com/lw685/springer-static/image/art%3A10.1186%2Fs11671-017-2172-z/MediaObjects/ 11671_2017_2172_Fig7_HTML.gif?as=webp"> 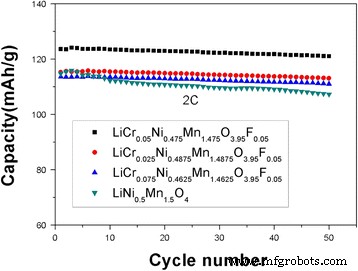
LiNi0.5의 사이클링 성능 Mn1.5 O4 및 LiCrx Ni0.5−0.5x Mn1.5−0.5x O3.95 F0.05 (x =0.025, 0.05, 0.075) 2C
전기화학적 성능에 대한 보다 자세한 분석은 CV 및 EIS에 의해 수행되었습니다. 그림 8은 LiCr0.05의 CV 곡선을 보여줍니다. Ni0.475 Mn1.475 O3.95 F0.05 및 순수상 LiNi0.5 Mn1.5 O4 . 이 두 재료의 전위차는 0.298V였습니다. LiNi0.5 Mn1.5 O4 산화 피크 전위는 4.861V인 반면 환원 피크 전위는 4.563V였습니다. 산화 피크 전류(I 아빠 )는 2.242mA이고 감소 피크 전류(I PC )는 2.288mA이므로 I 아빠 /나 PC 비율은 0.9799였습니다. LiCr0.05 Ni0.475 Mn1.475 O3.95 F0.05 산화 피크 전위는 4.864V, 환원 피크 전위는 4.578V, 전위차는 0.286V였습니다. I 아빠 1.273 mA, I PC 1.277mA 이고 I 아빠 /나 PC 비율은 0.9968(약 1)이었습니다. 위의 결과는 공동 도핑된 물질이 리튬 이온 삽입/방출의 가역성이 우수하고 쿨롱 효율이 향상되었음을 나타냅니다.
<그림><그림><소스 유형="이미지/webp" srcset="//media.springerature.com/lw685/springer-static/image/art%3A10.1186%2Fs11671-017-2172-z/MediaObjects/ 11671_2017_2172_Fig8_HTML.gif?as=webp"> 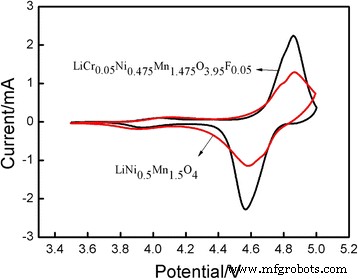
LiNi0.5의 순환 전압전류도 Mn1.5 O4 및 LiCr0.05 Ni0.475 Mn1.475 O3.95 F0.05
그림 9는 샘플의 EIS 패턴을 보여줍니다. 그림의 모든 EIS 스펙트럼은 고주파에서 중간 주파수 영역의 두 개의 반원과 저주파 영역의 경사선으로 구성됩니다. 고주파 영역의 반원은 전해질 표면 저항(R)을 통과하는 리튬 이온에 해당합니다. s ). 중간 주파수 영역의 반원은 전하 이동 저항(R ct ), 저주파 영역의 경사선은 Warburg 임피던스(Z w ), 이는 재료의 리튬 이온 확산과 관련이 있습니다. 그림 7에서 볼 수 있듯이 도핑은 R s , 리튬 이온의 확산성, 전도도 및 재료의 속도 능력 향상에 기여했습니다.
<그림><그림><소스 유형="이미지/webp" srcset="//media.springerature.com/lw685/springer-static/image/art%3A10.1186%2Fs11671-017-2172-z/MediaObjects/ 11671_2017_2172_Fig9_HTML.gif?as=webp"> 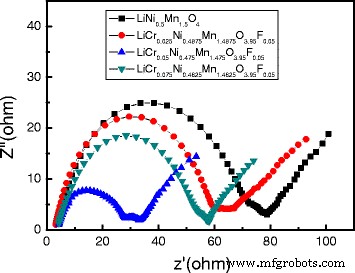
LiNi0.5의 EIS 패턴 Mn1.5 O4 및 LiCrx Ni0.5−0.5x Mn1.5−0.5x O3.95 F0.05 (x =0.025, 0.05, 0.075)
ZsimpWin 소프트웨어에 의해 장착된 등가 회로 아날로그의 Nyquist 플롯은 그림 10에 나와 있습니다. 이 회로에서 R e 및 R s SEI 필름의 전해질 저항 및 입자 간 계면 접촉 저항을 나타냅니다. R ct 는 전하 이동 저항이고 Z w 리튬 이온의 확산으로 인한 Warburg 임피던스를 나타냅니다. CPE와 CPEdl은 각각 고체전해질막의 정상소자이며, 전극-전해질 계면의 이중층 정전용량이다[32]. 등가 회로 아날로그의 피팅 매개변수는 표 2에 요약되어 있습니다.
<그림><그림><소스 유형="이미지/webp" srcset="//media.springerature.com/lw685/springer-static/image/art%3A10.1186%2Fs11671-017-2172-z/MediaObjects/ 11671_2017_2172_Fig10_HTML.gif?as=webp"> 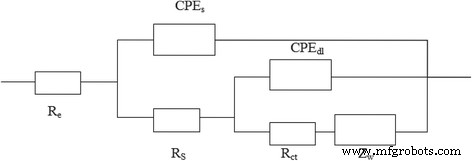
Nyquist 플롯의 등가 회로
<그림>
이전 연구에서는 리튬 이온의 확산 계수가 Warburg 계수와 관련이 있다고 제안했는데, 이는 저주파 영역의 경사선으로 계산할 수 있습니다. 리튬 이온 확산 계수는 다음 방정식을 사용하여 Fick의 규칙에 의해 계산되었습니다. [33]
$$ D=\frac{R^2{T}^2}{2{A}^2{n}^4{F}^4{C}^2{\sigma}^2} $$ (1)
여기서 D 는 리튬 이온 확산 계수, T 절대 온도, R 는 기체 상수, A 는 전극의 표면적, n 전자 전달 번호, F 패러데이 상수, C 는 리튬 이온의 몰 농도이고 σ는 Warburg 인자로 그림 7의 경사선 기울기입니다.
표 2에서 볼 수 있듯이 R s 도핑된 샘플의 값은 도핑되지 않은 샘플에 비해 크게 감소했으며 R s LiCr0.05 값 Ni0.475 Mn1.475 O3.95 F0.05 크게 감소했습니다. R 감소 s 값은 Cr
3+
임을 나타냅니다. , F
−
공동 도핑은 SEI 필름의 성장을 어느 정도 억제할 수 있으며 이는 F
-
전극 물질과 전해액 사이의 부반응. 전하 이동 저항 값이 낮을수록 전기화학적 분극이 낮아져 속도 기능과 사이클링 안정성이 높아집니다. LiCr0.05 Ni0.475 Mn1.475 O3.95 F0.05 가장 낮은 R ct 값(24.9Ω) 및 가장 높은 리튬 확산 계수(1.51 × 10
−10
) cm
2
s
−1
) 모든 샘플 중에서 전기화학적 분극이 가장 낮고 리튬 이온 이동도가 LiNi0.5임을 나타냅니다. Mn1.5 O4 음이온-양이온 화합물 치환에 의해 효과적으로 개선될 수 있다. EIS는 또한 전자 전도도의 크기를 비교하는 데 사용할 수 있습니다. Cr
3+
의 더 작은 전하 이동 저항 및 F
-
LiNi0.5 공동 도핑 Mn1.5 O4 깨끗한 LiNi보다 더 큰 전자 전도도를 나타냅니다0.5 Mn1.5 O4 . LiNi0.5의 전자 전도도 Mn1.5 O4 약 3.88 × 10
−5
입니다. S cm
−1
, LiCrx의 전자 전도도 Ni0.5−0.5x Mn1.5−0.5x O3.95 F0.05 (x =0.025, 0.05, 0.075) 샘플은 6.19 × 10−
5
S cm
-1
, 1.25 × 10
-4
S cm
−1
및 5.98 × 10
−5
S cm
−1
, 각각. 실제로 LiCr0.05 Ni0.475 Mn1.475 O3.95 F0.05 네 가지 샘플 모두에서 최고의 전기 화학적 성능을 가지고 있습니다. R 감소 ct D 증가 적절한 양의 Cr
3+
을 나타냅니다. , F
−
co-doping은 물질의 전기화학적 반응 활성에 긍정적인 영향을 미칩니다.
결론
Cr
3+
, F
−
LiNi0.5의 동시 도핑된 아날로그 Mn1.5 O4 (LiCrx Ni0.5−0.5x Mn1.5−0.5x O3.95 F0.05 (x =0.025, 0.05, 0.075))는 고온고체법으로 합성하였다. 재료의 XRD 패턴은 Cr
3+
및 F
-
Ni
2+
의 일부를 성공적으로 대체했습니다. , Mn
4+
, Mn
3+
, 및 O
2-
스피넬 물질에 원자가 존재하고 불순물 피크가 존재하지 않았습니다. LiCr0.05의 특정 방전 용량 Ni0.475 Mn1.475 O3.95 F0.05 0.1, 0.5, 2, 5, 10C에서 134.18, 128.70, 123.62, 119.63, 97.68mAh g
−1
, 각각. 특정 방전 용량은 121.02mAh g
−1
였습니다. 초기 방전 용량의 97.9%인 2C에서 50사이클 후. LiCr0.05의 용량 유지율 Ni0.475 Mn1.475 O3.95 F0.05 표본 중 가장 컸다. 재료의 결정성이 양호하고 팔면체 스피넬이 가장 많이 분포되어 있었다. Cr
3+
, F
−
공동 도핑된 재료는 더 높은 속도로 비방전 용량을 크게 개선하고, 사이클링 안정성을 개선하고, 리튬 이온의 가역성을 향상시키고, 임피던스 값을 감소시켰습니다.













